
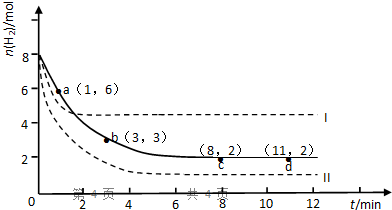
| ||
| 1min |
| ||
| 3min-1min |
| ||
| 8min-3min |


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
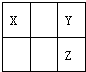
| A、原子的半径:Y大于X |
| B、氢化物的稳定性:X大于Y |
| C、最高价氧化物水化物的酸性:Z强于Y |
| D、Z原子比Y原子多一个电子层 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验序号 | H2O2溶液浓度/% | H2O2溶液体积/mL | 温度/℃ | MnO2用量/g | 收集O2的体积/mL | 反应所需时间/s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| ? | 30 | 5 | 35 | 2 | 49.21 | |
| ④ | 30 | 5 | 55 | 2 | 10.76 |
查看答案和解析>>
科目:高中化学 来源: 题型:
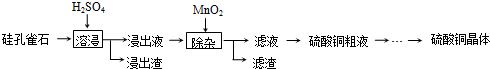
| 焙烧 |
| 还原 |
| 电解精炼 |
| ||
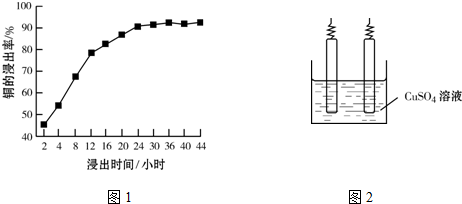
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、增加SO2的浓度,正反应速率先增大,后逐渐减小最后保持不变 |
| B、增加O2的浓度,正反应速率逐渐增大 |
| C、增加SO2的浓度,平衡常数增大 |
| D、若平衡时SO2的浓度比原来大,则平衡常数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①④⑤⑥ | B、①②③⑤ |
| C、②③④⑥ | D、以上全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
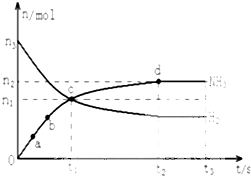 氨气主要用作致冷剂及制取铵盐和氨肥
氨气主要用作致冷剂及制取铵盐和氨肥查看答案和解析>>
科目:高中化学 来源: 题型:
| A、干冰能用作冷冻剂 |
| B、氯化钠可用作净水剂 |
| C、味精可用作食品调味剂 |
| D、小苏打是一种膨松剂,可用于制作馒头和面包 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com