
【题目】一定条件下,可逆反应N2+3H2![]() 2NH3 △H<0达到平衡后,只改变一个条件,下列叙述错误的是
2NH3 △H<0达到平衡后,只改变一个条件,下列叙述错误的是
A. 加催化剂,v正、v逆都发生变化,且变化的倍数相等
B. 加压,v正、v逆都增大,且v正增大的倍数大于v逆增大的倍数
C. 增大氮气的浓度,N2的平衡转化率减小,H2的平衡转化率增大
D. 降温,v正、v逆都减小,且v正减小的倍数大于v逆减小的倍数
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各2 mol充入某10 L恒容密闭容器中,发生反应X(g)+Y(g) ![]() 2Z(g) △H<0,—段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) △H<0,—段时间后达到平衡。反应过程中测定的数据如下表:
t/min | 2 | 4 | 10 | 12 |
n(Y)/mol | 1.40 | 1.10 | 0.40 | 0.40 |
下列说法正确的是
A. 反应前2 min 的平均速率v(Z)=3.0xl0-2 mol L-1min-1
B. 该温度下此反应的平衡常数K=64
C. 平衡后其他条件不变,再充入2 mol Z,新平衡时X的体积分数增大
D. 反应进行到10 min时保持其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是石蜡油在炽热碎瓷片的作用下产生C2H4并检验C2H4性质的实验。请回答下列问题:
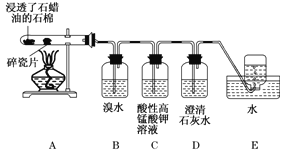
(1)A中碎瓷片的作用是____________。
(2)B装置中反应的化学方程式为___________。
(3) C装置中的实验现象______________ 。
(4) 查阅资料,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置________(填装置字母)中的实验现象可判断该资料是否真实。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)从樟科植物枝叶提取的精油中含有下列甲、乙、丙三种成分:

丙
分子式 | C16H14O2 |
部分性质 | 能使Br2/CCl4褪色 |
能在稀H2SO4中水解 |
(1)甲中含氧官能团的名称为________。
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):

其中反应Ⅰ的反应类型为________,反应Ⅱ的化学方程式为_______________(注明反应条件)。
(3)已知:RCH===CHR′![]() RCHO+R′CHO;2HCHO
RCHO+R′CHO;2HCHO![]() HCOOH+CH3OH
HCOOH+CH3OH
由乙制丙的一种合成路线图如下(A~F均为有机物,图中Mr表示相对分子质量):

①下列物质不能与C反应的是________(选填序号)。
a.金属钠 b.HBr c.Na2CO3溶液 d.乙酸
②写出F的结构简式__________________________________。
③丙有多种同分异构体,写出能同时满足下列条件的同分异构体________。
a.苯环上连接三种不同官能团
b.能发生银镜反应
c.能与Br2/CCl4发生加成反应
d.遇FeCl3溶液显示特征颜色
④综上分析,丙的结构简式为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从能量的变化和反应的快慢等角度研究反应:![]() 。
。
(1)为了加快正反应速率,可以采取的措施有________(填序号)。
A.使用催化剂 B.适当提高氧气的浓度 C.适当提高反应的温度
(2)下图能正确表示该反应中能量变化的是________(填序号)。
A. 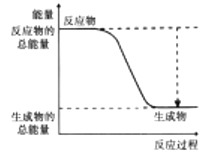 B.
B. 
(3)从断键和成键的角度分析上述反应中能量的变化。
化学键 | H—H | O=O | H—O |
键能 | 436 KJ·mol-1 | 496 KJ·mol-1 | 463 KJ·mol-1 |
请填写下表:_______________
化学键 | 填“吸收热量”或“放出热量” | 能量变化(KJ) |
拆开2molH2和1molO2中的化学键 | ①_________________ | ② KJ |
形成4molH-O键 | ③ | ④ KJ |
总能量变化 | ⑤ | ⑥ KJ |
(4)氢氧燃料电池的总反应方程式为![]() 。其中,氢气在________极发生________(“氧化”或“还原”)反应。
。其中,氢气在________极发生________(“氧化”或“还原”)反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 密闭容器中2 mol NO与1 mol O2充分反应,产物分子的数目为2NA
B. 25℃,pH=13的NaOH溶液中含有OH-的数目为 0.1NA
C. 标准状况下,22.4LN2与CO混合气体的质量为28g
D. 标准状况下,22.4 L CCl4含CCl4分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中正确的是( )
A.硫酸型酸雨的形成会涉及反应:![]()
B.用苛性钠溶液吸收过量SO2:![]()
C.足量氯水和碘化亚铁溶液的反应:![]()
D.工业上氯气和石灰乳反应制漂白粉:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、X是中学化学中常见的4种物质,它们均由短周期元素组成,转化关系如图所示。请针对以下三种情况回答下列问题。

(1)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,将A、C的水溶液混合可得白色胶状沉淀B。
①A中含有的金属元素为__________(填元素名称)
② 该金属元素的单质与某氧化物在高温下反应,可用于焊接铁轨及定向爆破,反应的化学反应方程式是_______________
(2)若A为固态非金属单质,A与X同周期,常温常压下C 为 白色固体,B分子中各原子最外层均为8电子结构。
① B的电子式为_____________。
② C与水剧烈反应,生成两种常见酸,反应的化学方程式为___________________。
(3) 若A、B、C的焰色反应均呈黄色,水溶液均为碱性。
① A中所含有的化学键是_____________。
② 自然界中存在B、C和H2O按一定比例结晶而成的固体。取一定量该固体溶于水配成100mL溶液,测得溶液中金属阳离子的浓度为0.5 mol/L。若取相同质量的固体加热至恒重,剩余固体的质量为__________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com