
【题目】不同温度下,水溶液中c(H+)与c(OH-)的关系如图所示。下列有关说法不正确的是( )
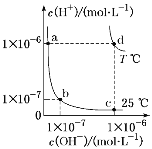
A. d点对应的食盐水pH=6,呈中性
B. 向a点对应的CH3COOH溶液中滴加NaOH溶液至b点,此时c(Na+)=c(CH3COO-)
C. a点对应的稀硫酸与c点对应的CH3COONa溶液中水的电离程度相同
D. 温度为T ℃时,0.05 mol·L-1Ba(OH)2溶液的pH=11
【答案】C
【解析】
A、d点所在温度下,水的离子积为10-12,而食盐水溶液显中性,则d点对应的食盐水pH=6,A正确;
B、向a点对应的醋酸溶液中滴加氢氧化钠溶液至b点,溶液显中性,即c(H+)=c(OH-),根据电荷守恒可知c(H+)+c(Na+)=c(OH-)+c(CH3COO-),故c(Na+)=c(CH3COO-),B正确;
C、酸对水的电离有抑制作用,盐的水解对水的电离有促进作用,故a点对应的稀硫酸溶液中水的电离程度小于c点对应的CH3COONa溶液中水的电离程度,C错误;
D、T℃时,水的离子积为10-12,0.05mol/L氢氧化钡溶液中氢氧根离子的浓度是0.1mol/L,则溶液中氢离子浓度是10-11mol/L,因此溶液的pH=11,D正确;
答案选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数用NA表示,气体摩尔体积用Vm表示,物质的质量用m表示,请回答下列问题:
(1)n=![]() =
=![]() =
=![]() ,①②③处分别补充为___、___、___。
,①②③处分别补充为___、___、___。
(2)一个铜原子的质量为m’g,铜的相对原子质量为M’,则阿伏加德罗常数NA=___mol-1。(列出表达式,下同)
(3)常温下20滴水约为1mL,水的密度为1g·mL-1,每滴水中约含a个水分子,则阿伏加德罗常数NA=___mol-1。
(4)bgH2中含N个氢分子,则阿伏加德罗常数NA=___mol-1。
(5)在标准状况下,VLO2中含有N个氧原子,则阿伏加德罗常数NA=___mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列试剂的保存或使用正确的是( )
A.漂白粉比氯水稳定,可露置在空气中
B.实验室的氯水需要保存在棕色试剂瓶中
C.用饱和Na2CO3溶液除去CO2中含有的少量HCl
D.金属钠可保存在煤油、四氯化碳(密度大于水)等有机溶剂中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用下列装置进行有关Cl2的实验。下列说法不正确的是( )
A.  图中:实验现象证明氯气无漂白作用,氯水有漂白作用
图中:实验现象证明氯气无漂白作用,氯水有漂白作用
B.  图中:收集氯气
图中:收集氯气
C.  图中:生成棕黄色的烟,加少量水溶解得到蓝绿色溶液
图中:生成棕黄色的烟,加少量水溶解得到蓝绿色溶液
D.  图中:若气球干瘪,证明可与NaOH溶液反应
图中:若气球干瘪,证明可与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t ℃时,在体积不变的密闭容器中发生反应:X(g)+3Y(g)![]() 2Z(g),各组分在不同时刻的浓度如下表,下列说法正确的是
2Z(g),各组分在不同时刻的浓度如下表,下列说法正确的是
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
2 min末浓度/mol·L-1 | 0.08 | a | b |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
A. 平衡时,X的转化率为20%
B. t ℃时,该反应的平衡常数为40
C. 前2 min内,用Y的变化量表示的平均反应速率v(Y)="0.03" mol·L-1·min-1
D. 增大平衡后的体系压强,v正增大,v逆减小,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,根据表中序号对应元素回答有关问题:
族 周期 | IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
4 | ⑨ | ⑩ |
(1)表中元素,化学性质最不活泼的是___,只有负价而无正价的是___,原子半径最大的是___;(填写元素符号);
(2)表中能形成两性氢氧化物的元素是___(填元素符号),分别写出该元素的氢氧化物与⑥、⑨的最高价氧化物对应水化物反应的离子方程式分别是___、___。
(3)元素①组成的单质的电子式为___;用电子式表示⑥的氢化物的形成过程___。
(4)②和③的单质加热时反应生成物质X,其化学式为___,该物质中含有的化学键的类型为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】断开1molH-H键、1molN-H键、1molN≡N键分别需要吸收的能量为436kJ、391kJ、946kJ,求:生成1molNH3需要___(填“吸收”或“放出”)能量___kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值,下列说法正确的是( )
A. 1 mol HNO3见光分解,转移电子数4NA
B. 含0.2 mol H2SO4的浓硫酸与足量Cu反应,生成SO2的分子数为0.1NA
C. 100 mL 0.5 mol/L的(NH4)2SO4溶液中,含有0.1NA个NH4+
D. 1 mol Na2O2晶体含有NA个阴离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:
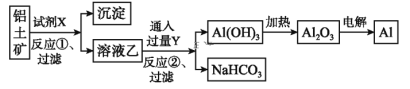
下列叙述正确的是( )
A. 试剂X可以是氢氧化钠溶液,也可以是盐酸
B. 反应①过滤后所得沉淀为氢氧化铁
C. 图中所示转化反应都不是氧化还原反应
D. 反应②的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com