
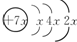 ,B是同周期除稀有气体外半径最大的元素,C的最外层有三个单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期除稀有气体外半径最大的元素,C的最外层有三个单电子,E的外围电子排布式为3d64s2.回答下列问题: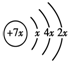 ,则x=2,故A为Si元素,A、B、C同周期,处于第三周期,B是同周期除稀有气体外半径最大的元素,则B为Na元素,C的最外层有三个成单电子,外围电子排布为3s23p3,故C为P元素,C、D同主族,故D为N元素;E是过渡元素,E的外围电子排布式分别为3d64s2,则F为Fe元素,据此解答.
,则x=2,故A为Si元素,A、B、C同周期,处于第三周期,B是同周期除稀有气体外半径最大的元素,则B为Na元素,C的最外层有三个成单电子,外围电子排布为3s23p3,故C为P元素,C、D同主族,故D为N元素;E是过渡元素,E的外围电子排布式分别为3d64s2,则F为Fe元素,据此解答. ,则x=2,故A为Si元素,A、B、C同周期,处于第三周期,B是同周期除稀有气体外半径最大的元素,则B为Na元素,C的最外层有三个成单电子,外围电子排布为3s23p3,故C为P元素,C、D同主族,故D为N元素;E是过渡元素,E的外围电子排布式分别为3d64s2,则F为Fe元素,
,则x=2,故A为Si元素,A、B、C同周期,处于第三周期,B是同周期除稀有气体外半径最大的元素,则B为Na元素,C的最外层有三个成单电子,外围电子排布为3s23p3,故C为P元素,C、D同主族,故D为N元素;E是过渡元素,E的外围电子排布式分别为3d64s2,则F为Fe元素,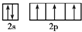 ,故答案为:N;
,故答案为:N; ;
; ,故答案为:
,故答案为: .
.


科目:高中化学 来源: 题型:
| 物质 | H2 | CO | CH4 |
| 燃烧热kJ?mol-1 | 285.8 | 283.0 | 890.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol氦气分子中含2NA个氦原子 |
| B、25℃时,l L pH=13的Ba(OH)2 溶液中含有OH-的数目为0.1NA |
| C、1.8 g重水(21H2O)中所含质子的个数为NA |
| D、1L 0.2mol/L的FeCl3溶液中Fe3+的数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石墨不如金刚石稳定 |
| B、等质量的石墨与金刚石相比,石墨具有的能量高 |
| C、等物质的量的石墨与金刚石完全燃烧,金刚石放出的能量多 |
| D、等物质的量的石墨与金刚石完全燃烧,石墨放出的能量多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、w=
| ||
B、w=
| ||
C、C=
| ||
D、b=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
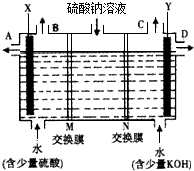
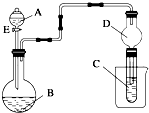 用如图所示装置(夹持仪器省略)进行实验,将液体A逐滴加入到固体B中,回答下列问题:
用如图所示装置(夹持仪器省略)进行实验,将液体A逐滴加入到固体B中,回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com