
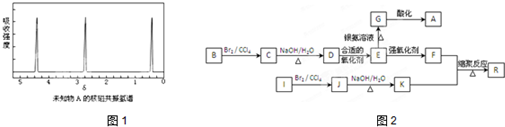
| 2×4+2-6 |
| 2 |
 ,E遇强氧化剂时,醛基和羟基均被氧化,故F为
,E遇强氧化剂时,醛基和羟基均被氧化,故F为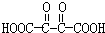 .烃I的相对分子质量为28,说明I为CH2=CH2,加成产物J为BrCH2CH2Br,J的水解产物为K为HOCH2CH2OH,代入经验证合理,F与发生缩聚反应生成R为
.烃I的相对分子质量为28,说明I为CH2=CH2,加成产物J为BrCH2CH2Br,J的水解产物为K为HOCH2CH2OH,代入经验证合理,F与发生缩聚反应生成R为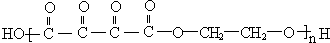 ,据此解答.
,据此解答.| 2×4+2-6 |
| 2 |
 ,E遇强氧化剂时,醛基和羟基均被氧化,故F为
,E遇强氧化剂时,醛基和羟基均被氧化,故F为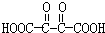 .烃I的相对分子质量为28,说明I为CH2=CH2,加成产物J为BrCH2CH2Br,J的水解产物为K为HOCH2CH2OH,代入经验证合理,F与发生缩聚反应生成R为
.烃I的相对分子质量为28,说明I为CH2=CH2,加成产物J为BrCH2CH2Br,J的水解产物为K为HOCH2CH2OH,代入经验证合理,F与发生缩聚反应生成R为 ,
,| 水 |
| △ |
| △ |
| 浓硫酸 |
| △ |
 +(2n-1)H2O,
+(2n-1)H2O,| 水 |
| △ |
| △ |
| 浓硫酸 |
| △ |
 +(2n-1)H2O;
+(2n-1)H2O; )的同分异构体M满足下列三个条件:
)的同分异构体M满足下列三个条件: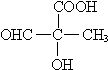 或
或 或
或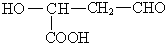 或
或 ,
, 或
或 或
或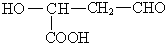 或
或 .
.


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 相关信息 |
| X | X的基态原子L层电子数是K层电子数的2倍 |
| Y | Y形成的多种单质,其中之一是地球生物的“保护伞” |
| Z | Z的基态原子核外p能级总电子数比s能级总电子数少一个 |
| M | M存在质量数为27,中子数为14的核素 |
| W | W有多种化合价,其白色氢氧化合物在空气中会迅速变成灰绿色,最后变成红褐色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
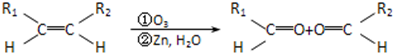
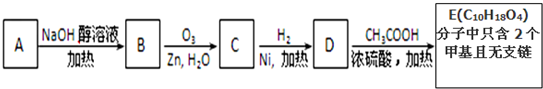
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使甲基橙变红的溶液中:Cr2O72-、Fe2+、SO42-、K+ |
| B、无色强酸性溶液中:Na+、Cl-、SO42-、[Cu(NH3)4]2+ |
| C、加入过量氨水溶液仍然澄清的溶液中:Cu2+、Ag+、NO3-、NH4+ |
| D、能使碘化钾淀粉试纸变蓝的溶液中:Na+、NH4+、S2-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:
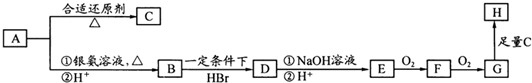
查看答案和解析>>
科目:高中化学 来源: 题型:
| 阳离子 | Na+ H+ Ba2+ |
| 阴离子 | OH- CO32- SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
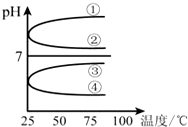 (1)稀释0.1mol?L-1氨水时,随着水量的增加而减小的是
(1)稀释0.1mol?L-1氨水时,随着水量的增加而减小的是| c(NH3?H2O) |
| c(OH-) |
| c(OH-) |
| c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com