
【题目】(1)计算调控值:
室温下,当溶液中c(Mg2+)=c(Cu2+)=0.1mol·L-1时,Mg2+、Cu2+开始沉淀至沉淀完全的pH范围分别为__。已知:Ksp[Mg(OH)2]=10-9、Ksp[Cu(OH)2]=10-15,当c(Mg2+)≤1×10-5mol·L-1时视为沉淀完全。
(2)选择调控值
铝灰的回收利用方法很多,现用含有Al2O3、SiO2和少量FeO·xFe2O3的铝灰制备Al2(SO4)3·18H2O,工艺流程如下:
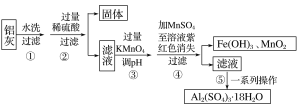
已知步骤③中所得溶液生成氢氧化物沉淀的pH如表所示:
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
开始沉淀时的pH | 3.4 | 6.3 | 1.5 |
完全沉淀时的pH | 4.7 | 8.3 | 2.8 |
在该浓度下除去铁的化合物,调节pH的最大范围为___。
(3)如何调控
接问题(2),步骤③中调pH时最佳试剂为___。
(4)突破应用
为分析某铜合金的成分,用酸将其完全溶解后,用NaOH溶液调节pH,当pH=3.4时开始出现沉淀,分别在pH为7.0、8.0时过滤沉淀。
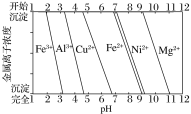
结合题图信息推断该合金中除铜外一定含有__。
【答案】10~12、7~9 2.8~3.4 Al2O3或Al(OH)3 Al、Ni
【解析】
注意分析流程中的物质变化,结合图表中的数据进行分析,根据浓度积的表达式进行相关计算。
(1)室温下,当溶液中c(Mg2+)=c(Cu2+)=0.1mol·L-1时,由Ksp[Mg(OH)2]=c(Mg2+)·c2(OH-),所以c(OH-)=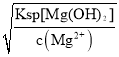 ,开始沉淀时,c(OH-)=
,开始沉淀时,c(OH-)=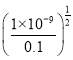 mol·L-1=10-4mol·L-1,所以c(H+)=
mol·L-1=10-4mol·L-1,所以c(H+)=![]() mol·L-1,此时pH=10;当Mg2+完全沉淀时,c(OH-)=
mol·L-1,此时pH=10;当Mg2+完全沉淀时,c(OH-)=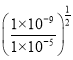 mol·L-1=10-2 mol·L-1,c(H+)=
mol·L-1=10-2 mol·L-1,c(H+)=![]() mol·L-1=1×10-12mol·L-1,此时pH=12。由Ksp[Cu(OH)2]=c(Cu2+)·c2(OH-),所以c(OH-)=
mol·L-1=1×10-12mol·L-1,此时pH=12。由Ksp[Cu(OH)2]=c(Cu2+)·c2(OH-),所以c(OH-)=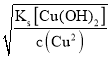 ,开始沉淀时c(OH-)=
,开始沉淀时c(OH-)=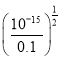 mol·L-1=10-7mol·L-1,c(H+)=
mol·L-1=10-7mol·L-1,c(H+)=![]() mol·L-1=10-7mol·L-1,此时该溶液的pH=7;当Cu2+完全沉淀时,c(OH-)=
mol·L-1=10-7mol·L-1,此时该溶液的pH=7;当Cu2+完全沉淀时,c(OH-)=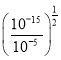 mol·L-1=10-5 mol·L-1,c(H+)=
mol·L-1=10-5 mol·L-1,c(H+)=![]() mol·L-1=10-9 mol·L-1,此时溶液的pH=9。所以Mg2+开始沉淀至完全沉淀的pH范围为10~12,Cu2+开始沉淀至完全沉淀的pH范围为7~9。
mol·L-1=10-9 mol·L-1,此时溶液的pH=9。所以Mg2+开始沉淀至完全沉淀的pH范围为10~12,Cu2+开始沉淀至完全沉淀的pH范围为7~9。
(2)Fe2+已完全转化为Fe3+,由表中数据可知,Fe3+完全沉淀时pH=2.8,而Al3+开始沉淀时pH=3.4,故Fe3+完全沉淀、而Al3+没有开始沉淀的pH调控范围为2.8~3.4。
(3)考虑到调节pH时不能引入杂质,故选用Al2O3、Al(OH)3最好,而选用其他试剂,则引入杂质离子,对产品的纯度或生产带来影响。
(4)能够溶解铜合金的酸应为过量的强氧化性的酸,因此溶解后的混合液中一定不含亚铁离子,根据题中信息及图片信息可知,pH=3.4时开始出现沉淀,则原溶液中一定有铝离子,一定不含铁离子,pH=7.0时过滤沉淀,此时过滤出来的物质为氢氧化铜和氢氧化铝,pH=8.0时再次进行过滤,说明在此pH区间内又有沉淀生成,在此区间内沉淀的物质只可能为Ni2+。故该合金中除含铜外,还含Al、Ni。


科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法不正确的是( )
A.1mol CH3COONa与少量CH3COOH溶于水所得的中性溶液中,CH3COO﹣数目为NA
B.标准状况下,2.24 L甲醇中C﹣H键的数目为0.3NA
C.4.6gNa与100mL1.0mol/L的盐酸溶液反应,转移电子数目为0.2NA
D.NA个D2 16O分子中含有10NA个中子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】左旋多巴![]() 是一种抗震颤麻痹药,合成路线如下。
是一种抗震颤麻痹药,合成路线如下。
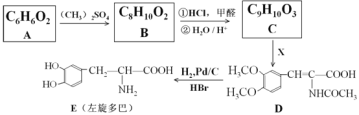
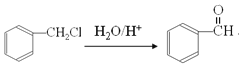
已知:Ⅰ.![]() +HCl+
+HCl+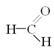 →
→
Ⅱ.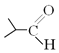
![]()
![]() →
→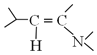 +H2O
+H2O
回答下列问题:
(1)化合物X的结构简式___。
(2)下列说法不正确的是___。
A.化合物A、E在空气中容易变质
B.化合物D→E可发生取代反应、加成反应
C.化合物D不能发生氧化反应,但能发生还原反应
D.溴水中分别加入化合物D、E都能产生溴水褪色的实验现象,且原理相同
(3)写出A→B在一定条件下发生反应的化学方程式:___。
(4)化合物C有多种同分异构体,写出至少三种满足下列条件的同分异构体___。
①分子中有苯环;②1H-NMR谱表明分子中有4种氢原子;③能发生水解反应
(5)设计以苯和氨基乙酸(![]() )为原料制备
)为原料制备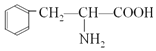 的合成路线(用流程图表示,无机试剂任选)___。
的合成路线(用流程图表示,无机试剂任选)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
A.能使甲基橙变红的溶液中:K+、Mg2+、NO3-、I-
B.c(HCO3-)=1 mol·L-1溶液中:Na+、Al3+、SO42-、Cl-
C.无色透明的溶液中:Fe3+、Al3+、NO3-、SO42-
D.常温下,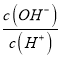 =10-10的溶液中:K+、Na+、I-、SO42-
=10-10的溶液中:K+、Na+、I-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以![]() 和
和![]() 为原料,通过反应:
为原料,通过反应:![]() 合成尿素。该反应的平衡常数和温度关系如下表;在一定温度和压强下,若原料气中的
合成尿素。该反应的平衡常数和温度关系如下表;在一定温度和压强下,若原料气中的![]() 和
和![]() 物质的量之比
物质的量之比![]() 氨碳比
氨碳比![]() 与
与![]() 平衡转化率
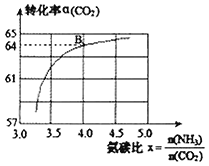
平衡转化率![]() 的关系如图,下列说法正确的是
的关系如图,下列说法正确的是
| 165 | 175 | 185 | 195 |
K |
|
|
|
|
A.如图点B处![]() 的平衡转化率为
的平衡转化率为![]()
B.该反应平衡常数的表达式为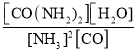
C.该反应中反应物的总键能大于生成物的总键能
D.氨碳比越高,合成![]() 时
时![]() 的转化率越高
的转化率越高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y同族,Z与X形成的离子化合物的水溶液呈中性。下列说法正确的是( )
A.简单离子半径:![]()
B.W与X形成的化合物溶于水后溶液呈碱性
C.气态氢化物的热稳定性:![]()
D.最高价氧化物的水化物的酸性:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向 2.0 L 浓度均为 1.0 mol·L1 的 CuSO4、Fe2(SO4)3 和 H2SO4 的混合液中加入足量的铁粉,反应停止后,铁粉有剩余,此时溶液中 Fe2+ 的物质的量浓度是(溶液的体积变化忽略不计)
A. 1.5 mol·L1 B. 2.0 mol·L1 C. 3.0 mol·L1 D. 5.0 mol·L1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年9月我国科学家对于可充放电式锌一空气电池研究取得重大进展。电池装置如图所示,该电池的核心是驱动氧化还原反应(ORR)和析氧反应(OER),KOH溶液为电解质溶液,放电的总反应方程式为2Zn+O2+40H-+2H2O=2Zn(OH)2。下列有关说法正确的是( )

A. 可逆锌一空气电池实际上是二次电池,放电时电解质溶液中K+向负极移动
B. 在电池产生电力的过程中,空气进入电池,发生ORR反应,并释放OH-
C. 发生OER反应的电极反应式为2H2O-4e-=O2+4H+
D. 放电时,电路中通过2mol电子,消耗氧气22.4L(标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度相同,浓度均为0.1 mol·L-1的:①(NH4)2CO3,②(NH4)2Fe(SO4)2,③氨水,④NH4NO3,⑤ NH4HSO4溶液,它们中的c(NH![]() )由大到小的排列顺序是( )
)由大到小的排列顺序是( )
A. ②⑤④①③ B. ③⑤②④①
C. ②①⑤④③ D. ⑤②①④③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com