
【题目】下列对实验事实的解释错误的是( )
选项 | 实验事实 | 解释 |
A | 实验室用粗锌与稀盐酸反应制H2比纯锌快 | 粗锌与稀盐酸构成原电池 |
B | 浓硝酸保存在棕色试剂瓶中 | 4HNO3 |
C | 向10mL0.2mol·L-1ZnSO4,溶液中加入10mL0.4mol·L-1Na2S溶液,产生白色沉淀,再滴加CuSO4溶液,沉淀变黑 | Ksp(CuS)<Ksp(ZnS) |
D | 做过银镜反应的试管可用铁盐溶液洗涤,加入稀盐酸,清洗效果更好 | Fe3++Ag |
A.AB.BC.CD.D
【答案】C
【解析】
A. 实验室用粗锌与稀盐酸反应制H2比纯锌快,粗锌与稀盐酸构成原电池,原电池加快反应速率,故A正确;
B. 浓硝酸保存在棕色试剂瓶中,主要是浓硝酸在光照或加热条件下反应生成H2O、NO2和O2,故B正确;
C. 向10mL 0.2 molL1 ZnSO4溶液中加入10mL 0.4 molL1 Na2S溶液,产生白色沉淀,溶液中剩余Na2S溶液,再滴加CuSO4溶液,生成CuS黑色沉淀,不能得出Ksp(CuS)<Ksp(ZnS),故C错误;
D. 做过银镜反应的试管可用铁盐溶液洗涤,Fe3++Ag![]() Fe2++Ag+,加入盐酸,Ag+与Cl-结合成氯化银沉淀,平衡右移,因此清洗效果更好,故D正确。
Fe2++Ag+,加入盐酸,Ag+与Cl-结合成氯化银沉淀,平衡右移,因此清洗效果更好,故D正确。
综上所述,答案为C。


科目:高中化学 来源: 题型:
【题目】现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的还原产物,设计了如图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题:
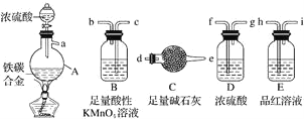
(1)该装置的连接顺序a___(填接口字母),连接好装置后,首先应进行的操作是____。
(2)mg铁碳合金中加入浓H2SO4,点燃酒精灯一段时间后,用滴管吸取A中的溶液滴入到适量水中作为试样,试样中所含金属离子的成分有以下三种可能:A:只含有Fe3+;B:只含有Fe2+;C:____,若为A,则A中反应的化学方程式为___,验证C种可能的实验方法___。
(3)待A中不再逸出气体时,停止加热,拆下C并称重,C增重bg。铁碳合金中铁的质量分数____(写表达式)。
(4)某同学认为利用此装置测得铁的质量分数偏大,请你写出可能的原因:_____。
(5)随着反应的进行,A中还可能发生某些离子反应。写出相应的离子方程式____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在沸水中逐滴加入5~6滴FeCl3饱和溶液,继续煮沸至溶液呈红褐色。下列正确的是
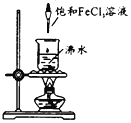
A.在暗处用激光笔照射液体,会出现一条光亮的通路
B.可用滤纸分离提纯得到氢氧化铁胶体
C.所得胶体中分散质的粒子直径大于100nm
D.取适量液体置于U型管,并通直流电,阳极颜色加深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学为了测定工业纯碱的纯度,进行了一系列实验。
(1)和索氏制碱法相比,侯氏制碱法的优势有___________________________________;
(2)工业纯碱中常含有少量NaCl杂质,解释原因__________________________,检验是否含有氯化钠杂质的方法为__________________________________________________________;
(3)使用重量法测定纯碱的纯度,用到的试剂有__________________________________;
(4)使用滴定法测定纯碱的纯度,用_________________(填仪器名称)称量1.200g工业纯碱样品,溶解,用1mol/L盐酸做标准液,滴定过程中溶液pH变化和生成CO2的量如图所示,A点溶液呈碱性的原因______________________________________________________,计算该工业纯碱样品的质量分数_______________。(计算结果保留两位小数)
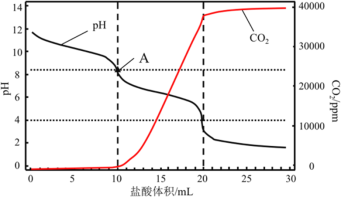 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体NH4Br置于密闭容器中,在某温度下,发生反应:NH4Br(s)![]() NH3(g)+HBr(g),2HBr(g)
NH3(g)+HBr(g),2HBr(g)![]() Br2(g)+H2(g),2 min后,测知H2的浓度为0.5 mol·L-1,HBr的浓度为4 mol·L-1,若上述反应速率用v(NH3)表示,则下列速率正确的是( )
Br2(g)+H2(g),2 min后,测知H2的浓度为0.5 mol·L-1,HBr的浓度为4 mol·L-1,若上述反应速率用v(NH3)表示,则下列速率正确的是( )
A. 0.5 mol·L-1·min-1B. 2.5 mol·L-1·min-1
C. 2 mol·L-1·min-1D. 1.25 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为淡黄色固体,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀。
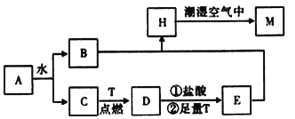
(1)物质D的化学式为 ________。
(2)A和水反应生成B和C的离子方程式为____________________,列出A的一种重要用途_________________。
(3)H在潮湿空气中变成M的实验现象是______________________。
(4)反应①的离子方程式为_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国许多城市为了减少燃煤造成的大气污染,对煤做了多方面的改进:
(1)为了除去煤中的含硫化合物,采用FeCl3脱硫,即用FeCl3溶液浸洗煤粉,发生反应如下:FeS2+14FeCl3+8H2O====2FeSO4+13FeCl2+16HCl(已知FeS2中硫元素的化合价为-1价)。
①该反应的氧化剂是____,若有1 mol FeS2被除去,则发生转移的电子的物质的量是___________。
②为了充分利用Fe2+并减少酸(HCl)污染,本方法中可利用工业废铁屑和Cl2让废液重新生成FeCl3。请写出这一过程中有关的离子方程式:______________;_____________________。
(2)“保护环境,就是保护人类自己”。飘尘是物质燃烧时产生的粒状漂浮物,颗粒很小,不易沉降,它与空气的污染物二氧化硫(SO2)接触时,二氧化硫(SO2)会部分转化为三氧化硫(SO3),其污染更加严重。
①飘尘所起的作用可能是______________.
A. 氧化剂B.还原剂C.催化剂D.载体
发生反应的化学方程式为________________________________________________.(如果是氧化还原反应,请用双线桥标出电子转移的方向和数目)
②冶金工业中常用高压电对气溶胶作用,以除去飘尘,减少对空气的污染,这种做法的依据是___.
A. 布朗运动 B.丁达尔现象 C. 渗析 D. 电泳。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2的资源化利用能有效减少CO2排放,又能缓解能源危机。实现CO2资源化再利用的研究工作正在不断进行中。
(1)CO2和H2,合成CH3OH,用非金属催化剂实现CO2电催化还原制备甲醇的反应历程如图所示:
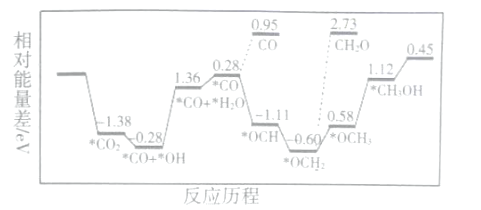
上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中___ (填字母)的能量变化。
A.*CO+*OH→*CO+*H2O B.*CO→*OCH
C. *OCH2→*OCH3 D.*OCH3→*CH3OH
(2)CO2和H2合成甲酸(HCOOH)其反应为:H2(g)+CO2(g)![]() HCOOH(g)。一定温度下,恒容密闭容器中进行上述反应,测得v正(CO2)随反应时间(t)的变化如图所示。
HCOOH(g)。一定温度下,恒容密闭容器中进行上述反应,测得v正(CO2)随反应时间(t)的变化如图所示。
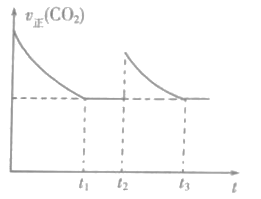
①t2时,改变的条件是充入amolCO2,同时___。
②下列关于t1、t3时刻的说法,正确的是___。
a.平衡常数:K1>K3
b.混合气的平均分子量:![]() <
<![]()
c.混合气中HCOOH的体积分数:V1=V3
③标准平衡常数Kθ=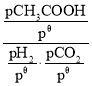 ,其中pθ为标准压强(1×105Pa),pH2、pCO2和pHCOOH为各组分的平衡分压,如pCO2=pxCO2,p为平衡总压,xCO2为平衡系统中CO2的物质的量分数。在标准压强下,向上述容器充入等物质的量的H2和CO2进行反应,测得HCOOH的平衡产率为w,则K=___(用含w字母表示)。
,其中pθ为标准压强(1×105Pa),pH2、pCO2和pHCOOH为各组分的平衡分压,如pCO2=pxCO2,p为平衡总压,xCO2为平衡系统中CO2的物质的量分数。在标准压强下,向上述容器充入等物质的量的H2和CO2进行反应,测得HCOOH的平衡产率为w,则K=___(用含w字母表示)。
(3)O2辅助的Al~CO2电池工作原理如图所示。该电池电容量大,能有效利用CO2,电池反应产物Al2(C2O4)3是重要的化工原料。
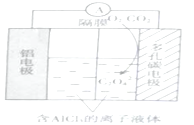
电池正极区发生的反应:①O2+e-=O2-;②___,O2的作用是___。
(4)CH4超干重整CO2得到的CO经偶联反应可制得草酸(H2C2O4)。常温下,向某浓度的草酸溶液中加入一定浓度的KOH溶液,所得溶液的pH=3,则![]() =___。
=___。
(已知常温下H2C2O4的Ka1=6×10-2,Ka2=6×10-5)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是一种黄绿色到橙黄色的气体,是国际上公认的安全、无毒的绿色消毒剂。已知:工业上制备二氧化氯的方法之一是用甲醇在酸性介质中与氯酸钠反应。二氧化氯能与许多化学物质发生爆炸性反应,遇水则生成次氯酸、氯气和氧气。
完成下列填空:
(1)将二氧化氯通入品红试液中,看到的现象是__;理由是__。
(2)请配平下列反应的化学方程式(CH3OH中H为+1价,O为-2价):
___CH3OH+__NaClO3+__→__CO2↑+__C1O2↑+__Na2SO4+__□__
(3)该反应中,被氧化的元素是__。还原产物与氧化产物的物质的量之比是__。
(4)根据上述反应可推知__。
a.氧化性:C1O2>NaClO3 b.氧化性:NaClO3>CH3OH
c.还原性:CH3OH>ClO2 d.还原性:CH3OH>Na2SO4
(5)若转移的电子数目为0.3NA(NA为阿伏加德罗常数),则反应产生气体(标准状况)为__升。
(6)消毒效率常以单位质量的消毒剂得到的电子数表示。ClO2的消毒效率是Cl2的__倍。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com