
【题目】常温下,等体积、pH均为3的HA和HB溶液分别加水稀释,溶液pH值的变化如下图所示,下列说法正确的是( )

A. 向HB溶液中滴加NaOH溶液的过程中,水的电离程度一直增大
B. 用pH为11的某碱与pH为3的HB溶液等体积混合后,溶液不可能显碱性
C. 氨水与HA溶液混合后的溶液中可能存在:c(NH4+ )>c(A+)>c(H+)>c(OH-)
D. 完全中和等体积等pH的HA、HB两溶液时,消耗同浓度NaOH溶液的体积:HA<HB
【答案】D
【解析】pH相同的一元酸用水稀释相同的倍数,弱酸的pH变化程度小,由图示可知HB的酸性比HA弱;A.向HB溶液中滴加NaOH溶液的过程中,最初因生成的NaB水解,促进水的电离,但当NaOH过量后,过量的NaOH将抑制水的电离,故A错误;B.常温下,pH之和等于14的酸和碱等体积混合,混合液的酸碱性是“谁弱显谁性,双强显中性”,如果等常浓度碱的电离程度比HB还小,则混合液显碱性,故B错误;C.氨水与HA溶液混合后的溶液中肯定存在的电荷守恒式是c(NH4+ )+c(H+)=c(A-)+c(OH-),,则c(NH4+ )>c(A-)>c(H+)>c(OH-)肯定不成立,故C错误;D.因HB比HA弱,pH相等的HA和HB中未电离的HB的物质的量比HA的物质的量大,则完全中和等体积等pH的HA、HB两溶液时,消耗同浓度NaOH溶液的体积是HA<HB,故D正确;答案为D。


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.12 g 金刚石中含有的共用电子对数为NA
B.1 mol AlCl3在熔融时离子总数为0.4NA
C.0.2 mol MnO2与足量浓盐酸反应转移的电子数小于 0.4NA
D.1 L 0.1 mol·Lˉ1 Na2CO3溶液中含有阴离子数大于 0.1 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]
有机物F是有机合成工业中一种重要的中间体。以甲苯和丙烯为起始原料合成F的工艺流程如下:
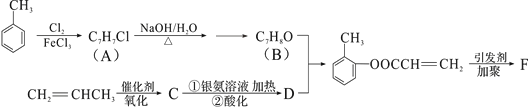
回答下列问题:
(1)化合物B中含氧官能团名称是_________F的结构简式__________________
(2)写出C与银氨溶液共热的化学反应方程式:_______________________
(3)化合物D不能发生的反应有__________________(填序号)。
①加成反应②取代反应③消去反应④氧化反应⑤水解反应
(4)B的含苯环结构的同分异构体还有__________种,其中一种的核磁共振氢谱中出现4个峰且不与FeCl3溶液发生显色反应的是____________(填结构简式)。
(5)B与D发生反应的类型________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中存在如下反应:2A(g)+B(g)![]() 3C(g)+D(s)△H<0,在其他条件不变时,改变某一条件对上述反应的影响,下列分析不正确的是
3C(g)+D(s)△H<0,在其他条件不变时,改变某一条件对上述反应的影响,下列分析不正确的是
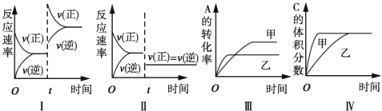
A. 图I表示增加反应物浓度对该平衡的影响
B. 图II表示减小压强对该平衡的影响
C. 图Ⅲ表示温度对该平衡的影响,温度:乙>甲
D. 图IV表示催化剂对该平衡的影响,催化效率:甲>乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ToC下,向体积为2 L的恒容密闭容器中通入NO2和O2,发生反应:4NO2(g)+O2(g)![]() 2N2O5(g)ΔH<0,部分实验数据如下表。下列说法不正确的是
2N2O5(g)ΔH<0,部分实验数据如下表。下列说法不正确的是
时间/s | 0 | 5 | 10 | 15 |
n(NO2)/mol | 8.00 | n1 | n2 | 4.00 |
n(O2)/mol | 2.00 | 1.25 | 1.00 | n3 |
A. 5s内NO2的平均反应速率为0.3 mol/(Ls)
B. 若10 s时,再向容器中充入2 mol N2O5(g),则新平衡下,NO2的体积分数将增大
C. 若5 s 时,改在绝热恒容下达平衡,新平衡下的平衡常数比原平衡的小
D. ToC,该反应的平衡常数为0.125,反应物的平衡转化率均为50%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个容积均为2L的恒容密闭容器中,起始时均充入a molH2S,以温度、Al2O3催化剂为实验条件变量,进行H2S的分解实验[反应为2H2S![]() 2H2(g)+S2(g)]。测得的结果如图所示。(曲线Ⅱ、Ⅲ表示经过相同时间且未达到化学平衡时H2S的转化率)
2H2(g)+S2(g)]。测得的结果如图所示。(曲线Ⅱ、Ⅲ表示经过相同时间且未达到化学平衡时H2S的转化率)

下列说法正确的是
A. 温度升高,H2S分解的速率增大,S2的含量减少
B. 由曲线Ⅱ、Ⅲ可知,加入Al2O3可提高H2S的平衡转化率
C. 900°C时,ts后达到平衡,则H2的生成速率为![]() mol·L-1·s-1
mol·L-1·s-1
D. 约1100°C,曲线Ⅱ、Ⅲ几乎重合,说明Al2O3可能几乎失去催化活性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为2L的恒容密闭容器中加入![]() 和一定量的CO后,发生反应:
和一定量的CO后,发生反应:![]() ,CO和
,CO和![]()
![]() 的物质的量随时间的变化如下表表示:则下列说法错误的是( )
的物质的量随时间的变化如下表表示:则下列说法错误的是( )
| 0 | 3 | 10 | 12 |
| 2 | 1 |
|
|
| 0 | 1 |
|
|
A.在![]() 内,用
内,用![]() 表示的平均反应速率为
表示的平均反应速率为![]()
B.在该条件下,上述反应的平衡常数为3
C.反应达平衡时,![]()
![]() 的体积分数为
的体积分数为![]()
D.要增大反应速率且增大![]()
![]() 在混合物中的体积分数,可采用压缩体积,增大体系压强的措施
在混合物中的体积分数,可采用压缩体积,增大体系压强的措施
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.加入过量氨水,有白色沉淀生成,则原溶液一定有Al3+
B.加入NaHCO3溶液,产生白色沉淀,则原溶液-定有Al3+
C.加入盐酸酸化的BaCl2溶液,有白色沉淀生成,则原溶液一定有SO![]()
D.加入NaOH溶液,产生的气体能使湿润的红色石蕊试纸变蓝,则原溶液中一定有NH![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以菱镁矿![]() 主要成分为
主要成分为![]() ,含少量
,含少量![]()
![]() 为原料制备高纯氧化镁的实验流程如下:
为原料制备高纯氧化镁的实验流程如下:

![]() 滤液P中含有的阳离子有 ______。
滤液P中含有的阳离子有 ______。
![]() 过程Ⅱ中发生的氧化还原反应的离子方程式是 ______ 。
过程Ⅱ中发生的氧化还原反应的离子方程式是 ______ 。
![]() 已知:
已知:
|
|
| |
开始沉淀的pH |
|
|
|
沉淀完全的pH |
|
|
|
过程Ⅲ中加入![]() 调节溶液pH约为4,其目的是 ______ 。
调节溶液pH约为4,其目的是 ______ 。
![]() 过程Ⅳ在
过程Ⅳ在![]() 煅烧
煅烧![]() ,发生多个反应,产物除MgO外,还有
,发生多个反应,产物除MgO外,还有![]() 、
、![]() 、CO、S等气体产物,利用右图装置判断煅烧产生的气体。
、CO、S等气体产物,利用右图装置判断煅烧产生的气体。
![]() 中试管壁附着有淡黄色固体,该固体的化学式是 ______ 。
中试管壁附着有淡黄色固体,该固体的化学式是 ______ 。
![]() 中盛放的溶液是
中盛放的溶液是![]() 填字母
填字母![]() ______ 。
______ 。
![]() 溶液
溶液![]() 溶液
溶液 ![]() 稀硝酸
稀硝酸![]() 溶液
溶液
![]() 写出
写出![]() 煅烧
煅烧![]() ,产生气体产物是S和CO的化学方程式 ______ 。
,产生气体产物是S和CO的化学方程式 ______ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com