
【题目】硫酸亚铁(FeSO4·7H2O)是一种重要的食品和饲料添加剂。实验室通过如下实验由废铁屑制备FeSO4·7H2O晶体:
①将5%Na2CO3溶液加入到盛有一定量废铁屑的烧杯中,加热数分钟,用倾析法除去Na2CO3溶液,然后将废铁屑用水洗涤2~3遍;
②向洗涤过的废铁屑中加入过量的稀硫酸,控制温度在50~80℃之间至铁屑耗尽;
③ ,将滤液转入到密闭容器中,静置、冷却结晶;
④待结晶完毕后,滤出晶体,用少量冰水洗涤2~3次,再用滤纸将晶体吸干;
⑤将制得的FeSO4·7H2O晶体放在一个小广口瓶中,密闭保存.
请回答下列问题:
(1)实验步骤①的目的是___________________________________________。
(2)写出实验步骤②中的化学方程式__________________________________________。
(3)补全实验步骤③的操作名称_________________________。
(4)实验步骤④中用少量冰水洗涤晶体,其目的是_______________________________。
(5)乙同学认为甲的实验方案中存在明显的不合理之处,你______(填“是”或“否”)同意乙的观点
(6)丙同学经查阅资料后发现,硫酸亚铁在不同温度下结晶可分别得到FeSO4·7H2O、FeSO4·4H2O和FeSO4·H2O.硫酸亚铁在不同温度下的溶解度和该温度下析出晶体的组成如下表所示(仅在56.7℃、64℃温度下可同时析出两种晶体).
硫酸亚铁的溶解度和析出晶体的组成
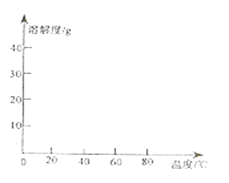
请根据表中数据画出硫酸亚铁的溶解度曲线示意图。__
(7)若需从硫酸亚铁溶液中结晶出FeSO4·4H2O,应控制的结晶温度(t)的范围为________________。
(8)取已有部分氧化的绿矾固体(硫酸亚铁的相对原子质量用M表示)wg,配制成100 mL用c mol/L KMnO4标准溶液滴定,终点时消耗标准液的体积为VmL,则:若在滴定终点读取滴定管读数时,俯视滴定管液面,使测定结果________(填“偏高”、“偏低”或“无影响”)
【答案】去除油污或利用碳酸钠水解后显碱性的性质除去表面油污 Fe+H2SO4(稀) ![]() FeSO4+H2↑ 趁热过滤 洗去杂质,降低洗涤过程中FeSO4·7H2O的损耗 是
FeSO4+H2↑ 趁热过滤 洗去杂质,降低洗涤过程中FeSO4·7H2O的损耗 是 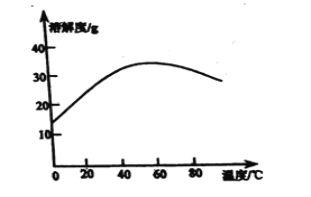 56.7℃<t<64℃ 偏低
56.7℃<t<64℃ 偏低
【解析】
(1)Na2CO3溶液显碱性,铁屑表面含有油脂,油脂在碱性条件下,水解成可溶水的物质,步骤①的目的是除去铁屑表面的油污;
(2)发生化学方程式为Fe+H2SO4![]() FeSO4+H2↑;
FeSO4+H2↑;
(3)步骤③将滤液转入到密闭容器,冷却结晶,因此步骤③的操作名称为趁热过滤;
(4)一般温度低,晶体的溶解度低,冰水洗涤的目的是洗去表面的杂质,减少FeSO4·7H2O的损耗;
(5)步骤②中铁屑耗尽,铁转化成Fe2+,Fe2+容易被氧化成Fe3+,即同意乙同学的观点;
(6)根据表格中的数据,得出: ;
;
(7)根据表格中的数据,得到FeSO4·4H2O,在56.7℃、64℃同时析出两种晶体,因为温度控制在高于56.7℃,低于64℃,范围是56.7℃<t<64℃;
(8)根据得失电子数目,推出FeSO4·7H2O的质量分数为![]() ,根据滴定管从上到下刻度增大,俯视读数,V偏小,即所测结果偏低。
,根据滴定管从上到下刻度增大,俯视读数,V偏小,即所测结果偏低。


科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、M、R五种元素中,原子序数依次增大,其结构或性质信息如下表。请根据信息回答有关问题:
元素 | 结构或性质信息 |
X | 原子的L层上s电子数等于p电子数 |
Y | 原子核外的L层有3个未成对电子 |
Z | 在元素周期表的各元素中电负性仅小于氟 |
M | 单质常温、常压下是气体,原子的M层上有1个未成对的p电子 |
R | 第四周期过渡元素,其价电子层各能级处于半充满状态 |
(1)元素M的原子核外有 ______ 种不同运动状态的电子;
(2)五种元素中第一电离能最高的是_______写元素符号;
(3)在Y形成的单质中,![]() 键与
键与![]() 键数目之比为______,在
键数目之比为______,在![]() 中Z原子的杂化方式为_____,其分子的空间构型为 ______;
中Z原子的杂化方式为_____,其分子的空间构型为 ______;
(4)R的一种配合物的化学式为![]() 。已知
。已知![]() 在水溶液中用过量硝酸银溶液处理,产生
在水溶液中用过量硝酸银溶液处理,产生![]() AgCl沉淀,此配合物最可能是 ______填序号。
AgCl沉淀,此配合物最可能是 ______填序号。
A.![]() B.
B.![]()
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯用途广泛,工业上可通过下列流程合成二甘醇及其衍生物。已知:R-OH + SOCl2 → R-Cl + SO2 ↑+ HCl↑ 请回答:

(1)写出B的官能团的电子式________________________。
(2)写出有关物质的结构简式:A_________________D_________________。
(3)指出反应类型:②_________________。
(4)写出下列化学方程式:反应①______________;反应②___________。
(5)①二甘醇又名(二)乙二醇醚,根据其结构判断下列说法正确的是____(填序号)。
a. 难溶于水 b. 沸点较高 c. 不能燃烧
②E的同分异构体很多,写出其中能够发生银镜反应的两种异构体的结构简式_________________。
(6)请写出由1-氯丙烷合成丙酮的合成路线图并注明反应条件(无机试剂任选)________。合成路线流程图示例如下:CH3CH2OH![]() CH2=CH2
CH2=CH2![]() Br-CH2CH2-Br
Br-CH2CH2-Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将 0.10 mol·L-1 盐酸滴入 20.00 mL 0.10 mol·L-1 氨水中,溶液中 pH 和 pOH 随加入盐酸体积变化曲线如图所示。已知:pOH=-lg c(OH-),下列正确的是

A. M 点所示溶液中可能存在c(Cl-)> c(NH4+)
B. N 点所示溶液中可能存在:c (NH4+)+ c(NH3﹒H2O)= c(Cl-)
C. Q 点盐酸与氨水恰好中和
D. M 点到Q点所示溶液中水的电离程度先变大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl﹣KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为PbSO4+2LiCl+Ca═ CaCl2+Li2SO4+Pb。下列有关说法正确的是

A. 正极反应式:Ca+2Cl-﹣2e-= CaCl2
B. 放电过程中,Li+向负极移动
C. 常温时,在正负极间接上电流表或检流计,指针发生偏转
D. 每转移0.1 mol电子,理论上生成10.35g Pb
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢卤酸的能量关系如图所示下列说法正确的是

A. 已知HF气体溶于水放热,则HF的△H1<0
B. 相同条件下,HCl的△H2比HBr的小
C. 相同条件下,HCl的△H3+△H4比HI的大
D. 一定条件下,气态原子生成1molH-X键放出akJ能量,则该条件下△H2=+akJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.有下列微粒:①11H、②21H、③31H、④16O2、⑤16O3。回答下列问题(填序号):
(1)以上5种微粒中共含有___种元素,__互为同素异形体;
(2)___互称为同位素。
Ⅱ.根据下列提供的一组物质回答问题:
①HCl ②CaCl2 ③MgO ④Cl2 ⑤NaOH ⑥NH4Cl
(1)仅含共价键的是___;离子化合物有___;(用序号表示)
(2)既有离子键又有共价键的是___;含有非极性键的是__;(用序号表示)
(3)HCl的电子式:____;NaOH的电子式:____;MgO的电子式:____。
用电子式表示CaCl2的形成过程:____________
用电子式表示Cl2的形成过程:______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com