
【题目】某同学欲配制480 mL物质的量浓度为0.1mol·L-1的CuSO4溶液。
(1)完成该实验用到的仪器主要有:托盘天平、胶头滴管、烧杯、玻璃棒、药匙和____________。
(2)写出整个实验简单的操作过程:计算→称量→溶解→转移→____________→定容→摇匀。
(3)如果用CuSO4固体来配制,应该称量固体的质量为_________________;如果用CuSO4·5H2O来配制,应该称量固体的质量为____________________。
(4)下列操作使配制的溶液浓度偏低的是__________________。
A.配制的过程中有少量的液体溅出烧杯。
B.使用前容量瓶用蒸馏水洗涤,且没有干燥。
C.定容时俯视液面。
D.定容摇匀后,液面下降,又加水至刻度线。
(5)取配制好的溶液50 mL用水稀释到100 mL所得溶液中Cu2+的物质的量浓度为_________。
【答案】500mL容量瓶 洗涤 8.0g 12.5g AD 0.05mol/L
【解析】
(1)依据配制溶液的一般步骤选择需要仪器,依据配制溶液体积选择容量瓶规格;
(2)依据配制溶液的一般步骤解答;
(3)依据m=cVM计算需要硫酸铜和五水硫酸铜的质量;
(4)分析操作对溶质的物质的量和溶液体积的影响,依据c=![]() 进行误差分析;
进行误差分析;
(5)根据稀释的公式c1V1=c2V2计算。
(1)实验室没有480mL的容量瓶,应该选用500mL容量瓶;故答案为:500mL容量瓶;
(2)配制500mL 0.1mol/L的硫酸铜溶液的操作步骤有:计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作;故答案为: 洗涤;
(3)配制500mL0.1mol/L的硫酸铜溶液,需要硫酸铜的物质的量为:n(CuSO4)=0.1mol/L×0.5L=0.05mol,需要硫酸铜的质量为:m(CuSO4)=160g/mol×0.05mol=8.0g;需要五水硫酸铜的质量为:m(CuSO45H2O)=250g/mol×0.05mol=12.5g;故答案为:8.0g;12.5g;
(4)A、配制的过程中有少量的液体溅出烧杯,导致溶质的物质的量偏少,浓度偏小;
B、使用前容量瓶用蒸馏水洗涤,且没有干燥,对溶质的物质的量及最终溶液体积都没有影响,不影响配制结果;
C、定容时俯视观察刻度线,液面在刻度线下方,溶液的体积偏小,所配溶液的浓度偏高;
D、定容摇匀后再加水即增大了溶液的体积,故溶液浓度偏低。
故答案为:AD
(5)利用稀释公式c1V1=c2V2,0.05L×0.1mol/L=0.1L×c2,c2=0.05mol/L,故答案为:0.05mol/L。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】中学化学中几种常见物质的转化关系如图所示,且已知将F的饱和溶液滴入沸水中,煮沸可得到以H为分散质的红褐色胶体。
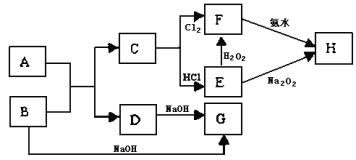
请回答下列问题:
(1)红褐色胶体中H粒子的直径大小范围____;
(2)写出H2O2的电子式:____;
(3)写出B→G的离子方程式____;
(4)若A、B恰好完全反应,将产物C与足量盐酸反应得到amol气体,另取等质量B与足量盐酸反应得到b mol气体,a:b=5:7,则A的化学式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某种有机物分子的球棍模型图,图中的“棍”代表单键或双键,不同大小的“球”代表不同的短周期元素的原子,对该有机物的叙述不正确的是
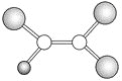
A. 该有机物可能的化学式为C2HCl3
B. 该有机物可以由乙烯和氯化氢通过加成反应得到
C. 该有机物分子中的所有原子在一个平面上
D. 该有机物分子中一定有碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是与生命活动密切相关的三种常见化合物,每种物质所含元素种类均不超过三种,甲是单质。它们之间有如下转化关系:
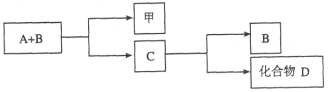
化合物D也是生活中常见的化合物,在一定条件下可发生如下反应:D+3甲![]() 3A+2B
3A+2B
请回答下列问题:
(1)在化合物A、B、C、D中所含元素完全相同的是__________和__________(填字母)。
(2)在常温下,A和B通过__________转化为C。该过程的能量转化关系如何?
____________________。
(3)写出由C生成D的反应的化学方程式____________________。
(4)化合物C是人类生命活动不可缺少的物质之一,它在血液中的正常含量是__________。
(5)目前化合物B在大气中含量呈上升趋势,对环境造成的影响是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式不正确的是
A.过量SO2通入次氯酸钠溶液中:SO2+ClO-+H2O=SO42-+Cl-+2H+
B.二氧化硅和氢氧化钠溶液反应:SiO2+2OH-=SiO32-+H2O
C.实验室制备Cl2:![]()
D.酸性介质中KMnO4氧化H2O2:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,4.48LCl2通入水中,转移电子数为0.2NA
B.273K、101kPa下,28g乙烯与丙烯混合物中含有C—H键的数目为4NA
C.1L 0.1mol/L Na2SO4溶液中含有的氧原子数为0.4NA
D.1molL-1CH3COOH与1molL-1CH3COONa溶液等体积混合,溶液中CH3COOH和CH3COO-的总数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钠常作漂白剂、杀菌剂、消毒剂。过氧化钠保存不当容易吸收空气中CO2而变质。
(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入__________溶液,充分振荡后有白色沉淀,证明Na2O2已经变质。
(2)该课外活动小组为了粗略测定过氧化钠的纯度,他们称取a g样品,并设计用下图装置来测定过氧化钠的质量分数。

①A中发生反应离子方程式为_____________________。
②将仪器连接好以后,必须进行的第一步操作是_____________________。
③B装置出来的气体是否需要干燥_________________。(填“是”或“否”)
④写出装置C中发生的所有反应的化学方程式_____________,______________。
⑤D中NaOH溶液的作用_______________________。
⑥实验结束时,读取实验中生成气体的体积时,不合理的是_______________。
a.直接读取气体体积,不需冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中水的体积
⑦读出量筒内水的体积后,折算成标准状况下氧气的体积为V mL,则样品中过氧化钠的质量分数为__________________。
⑧实验完成后E到F之间导管内残留水的体积会使测量结果__________。(填“偏大”、“偏小”或“不影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
(1)水分子中氧原子在基态时核外电子排布式为______________________________;
(2)写出与H2O分子互为等电子体的微粒_________________________(填2种)。
(3)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是______________
A.氧原子的杂化类型发生了改变 | B.微粒的形状发生了改变 |
C.微粒的化学性质发生了改变 | D.微粒中的键角发生了改变 |
(4)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是_________(请用相应的编号填写)
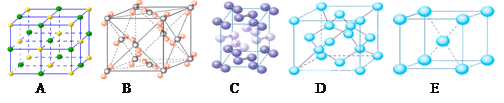
(5)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是51 kJ/mol,除氢键外,水分子间还存在范德华力(11 kJ/mol),则冰晶体中氢键的“键能” 是_________kJ/mol;
(6)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配离子。请写出生成此配离子的离子方程式:__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤烟气中含有大量SO2和NO。某科研小组研究臭氧氧化-碱吸收法同时脱除SO2和NO工艺,氧化过程反应原理及反应热、活化能数据如下:
反应Ⅰ:NO(g)+O3(g)![]() NO2(g)+O2(g) △H1=-200.9kJ/mol Ea1=3.2kJ/mol
NO2(g)+O2(g) △H1=-200.9kJ/mol Ea1=3.2kJ/mol
反应Ⅱ:SO2(g)+O3(g)![]() SO3(g)+O2(g) △H2=-241.6kJ/mol Ea2=58kJ/mol
SO3(g)+O2(g) △H2=-241.6kJ/mol Ea2=58kJ/mol
已知该体系中温度80℃以上臭氧发生分解反应:2O3(g)![]() 3O2(g)。请回答:
3O2(g)。请回答:
(1)已知反应Ⅰ在低温下自发进行,则该反应的熵变△S___0(填“大于”或“小于”)。
(2)其它条件不变,每次向反应器中充入含1.0molNO、1molSO2的模拟烟气和2.0molO3,改变温度,反应相同时间后体系中NO和SO2的转化率如图所示:
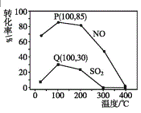
①由图可知相同温度下NO的转化率远高于SO2,结合题中数据分析其可能原因___。
②100℃、反应相同时间t时O3的分解率达10%,则体系中剩余O3的物质的量是___mol。
③下列法正确的是___。
A.P点一定为平衡状态点
B.温度高于200℃后,NO和SO2的转化率随温度升高显著下降、最后几乎为零
C.其它条件不变,若缩小反应器的容积可提高NO和SO2的转化率
D.臭氧氧化过程不能有效地脱除SO2,但后续步骤碱吸收可以有效脱硫
(3)工业上可以通过电解NO制备NH4NO3,原理如图所示。写出电解过程阳极的电极反应式___。
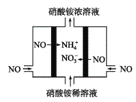
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com