
����Ŀ��A��B��C��D��E��FΪԭ���������������������Ԫ�ء���֪A��C��F��ԭ�ӵ�����㹲��11�����ӣ���������Ԫ�ص�����������ˮ����֮���������ܷ�Ӧ�����������κ�ˮ��DԪ��ԭ�ӵ������������ȴ�����������4����EԪ���⻯������2����ԭ�ӣ��Իش�
��1��д��Bԭ�ӽṹʾ��ͼ___
��2��Ԫ������������Ӧˮ�����м�����ǿ����___��д��һ�ֺ���FԪ�صľ���Ư���Ե�����___���û�ѧʽ��ʾ����
��3���õ���ʽ��ʾA��Fԭ���γɻ�����Ĺ���___��
��4��C��F����Ԫ������������ˮ����֮�䷴Ӧ�����ӷ���ʽ___��
��5�����ʵ��֤��E��F����Ԫ�طǽ����Ե�ǿ��___����ѧ����ʽ�ӱ�Ҫ����˵������
���𰸡�![]() NaOH HClO��Ca(ClO)2��NaClO��
NaOH HClO��Ca(ClO)2��NaClO�� ![]() Al(OH)3+3H+=Al3++3H2O H2S��Һ��ͨ��Cl2�����ɵ���ɫ��������Ӧ����HCl��S����Ӧ����ʽΪH2S+Cl2=2HCl+S��
Al(OH)3+3H+=Al3++3H2O H2S��Һ��ͨ��Cl2�����ɵ���ɫ��������Ӧ����HCl��S����Ӧ����ʽΪH2S+Cl2=2HCl+S��
��������
A��B��C��D��E��FΪԭ���������������������Ԫ�ء���֪A��C��F��ԭ�ӵ�����㹲��11�����ӣ���������Ԫ�ص�����������ˮ����֮���������ܷ�Ӧ�����������κ�ˮ����AΪ��Ԫ�أ�CΪ��Ԫ�أ�FΪ��Ԫ�أ�DԪ��ԭ�ӵ������������ȴ�����������4������Ϊ��Ԫ�أ�EԪ���⻯������2����ԭ�ӣ���Ϊ��Ԫ�أ��ݴ˷������
A��B��C��D��E��FΪԭ���������������������Ԫ�ء���֪A��C��F��ԭ�ӵ�����㹲��11�����ӣ���������Ԫ�ص�����������ˮ����֮���������ܷ�Ӧ�����������κ�ˮ����AΪ��Ԫ�أ�CΪ��Ԫ�أ���BΪþԪ�أ�FΪ��Ԫ�أ�DԪ��ԭ�ӵ������������ȴ�����������4������Ϊ��Ԫ�أ�EԪ���⻯������2����ԭ�ӣ���Ϊ��Ԫ�ء�
��1��BΪþԪ�أ�ԭ������Ϊ12��ԭ�ӽṹʾ��ͼΪ![]() ��
��
��2��ͬ���ڴ����ҽ�����������������������ˮ����ļ�����������Ԫ������������Ӧˮ�����м�����ǿ����NaOH��FΪ��Ԫ�أ�����FԪ�صľ���Ư���Ե�������HClO��Ca(ClO)2��NaClO�ȣ�
��3��A��Fԭ���γɻ�����NaCl���Ȼ���Ϊ���ӻ������������������ͨ�����Ӽ���϶��ɣ�NaCl���γɹ���Ϊ![]() ��
��
��4��C��F����Ԫ������������ˮ����Al(OH)3��HClO4֮�䷴Ӧ�����ӷ���ʽΪAl(OH)3+3H+=Al3++3H2O��
��5��EΪ��Ԫ�ء�FΪ��Ԫ�أ�֤����ǽ�����ǿ�������кܶ�������Ӧ�⻯����ȶ��ԣ�����������Ӧˮ��������ԣ��ǽ������ʵ������Եȣ���H2S��Һ��ͨ��Cl2�����ɵ���ɫ��������Ӧ����HCl��S����Ӧ����ʽΪH2S+Cl2=2HCl+S����


 ��ʦ�㲦��ϵ�д�
��ʦ�㲦��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪723Kʱ��2SO2��g��+O2��g��![]() 2SO3��g����H=��QkJ/mol������ͬ�����£���һ�ܱ�������ͨ��2mol SO2��1mol O2���ﵽƽ��ʱ�ų�������ΪQ1kJ������һ�����ͬ���ܱ�������ͨ��1mol SO2��0.5mol O2���ﵽƽ��ʱ�ų�������ΪQ2kJ����Q1��Q2��Q����Ĺ�ϵ�ǣ� ��
2SO3��g����H=��QkJ/mol������ͬ�����£���һ�ܱ�������ͨ��2mol SO2��1mol O2���ﵽƽ��ʱ�ų�������ΪQ1kJ������һ�����ͬ���ܱ�������ͨ��1mol SO2��0.5mol O2���ﵽƽ��ʱ�ų�������ΪQ2kJ����Q1��Q2��Q����Ĺ�ϵ�ǣ� ��
A��Q2=![]() B��Q2��
B��Q2��![]() C��Q2��Q1��Q D��Q=Q1��Q2
C��Q2��Q1��Q D��Q=Q1��Q2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���������õ�Ӫ��Һ��Ҫ��KCl��K2SO4��NH4Cl���ֹ���ԭ�ϵ����ʵ���֮��Ϊ1��4��8�������ø�Ӫ��Һ��ȡ214gNH4Cl������KCl��K2SO4�������ֱ�Ϊ�� ��
A.53.5g��214gB.37.25g��348g
C.74.5g��696gD.149g��696g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ҫ�ĵ���,�Dz������Ļ�����Ʒ֮һ����ϳ�ԭ��Ϊ:N2(g)+3H2(g)![]() 2NH3(g)��H=-92.4 kJ��mol-1,
2NH3(g)��H=-92.4 kJ��mol-1,
��1�����ܱ������У�Ͷ��1mol N2��3 mol H2�ڴ��������·�����Ӧ:
�ٵ���Ӧ�ﵽƽ��ʱ��N2��H2��Ũ�ȱ���__________
������ƽ����ϵ���¶�(�����������)����������ƽ����Է�������________��(��������С�����䡱)
�۵��ﵽƽ��ʱ�����������������ѹǿ���䣬ƽ�⽫_______ (�������������)�ƶ���
�����������ݡ����ȣ�����ʹ�������¶�Ѹ������ԭ����2����ƽ�⽫____________(������ƶ������������ƶ������ƶ���)���ﵽ��ƽ����������¶�________(����ڡ�����С�ڡ����ڡ�)ԭ����2����
��2���÷�Ӧ N2��g��+3H2��g��![]() 2NH3��g����H=��92.4kJ/mol ��һ�ܱ������з�������ͼ��ijһʱ��η�Ӧ�����뷴Ӧ���̵Ĺ�ϵ����ͼ��
2NH3��g����H=��92.4kJ/mol ��һ�ܱ������з�������ͼ��ijһʱ��η�Ӧ�����뷴Ӧ���̵Ĺ�ϵ����ͼ��

��t1��t3��t4ʱ�̣���ϵ�зֱ���ʲô���������˱仯��
t1______________��t3_____________��t4___________��
������ʱ����У����İٷֺ�����ߵ���______
A��0��t1 B��t2��t3 C��t3��t4 D��t4��t5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ����գ�
��1��ijԭ�Ӻ���6�����Ӻ�8�����ӣ��ú��ط��ű�ʾ��ԭ��___����Ԫ�ط��ű�ʾ����
��2��д��HClO�ĵ���ʽ___��CS2�Ľṹʽ___��
��3��S2����Al3+��Na+��F���������Ӱ뾶�ɴ�С˳��Ϊ___��H2O��H2S��I2���ַ����۷е��ɸߵ���˳��Ϊ___��
��4��Na2O2�к��еĻ�ѧ������Ϊ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.ij�¶�ʱ����һ��10L�ĺ��������У�X��Y��Z��Ϊ���壬�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ������ͼ��������գ�
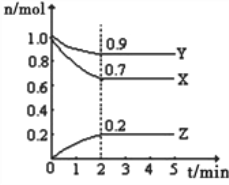
��1����Ӧ��ʼ��2min��������Z��ʾ��ƽ����Ӧ����Ϊ______________________��
��2��ƽ��ʱ�����ڻ�������ܶȱ���ʼʱ__________����������С������ȡ���ͬ������������ƽ����Է�����������ʼʱ___________��
��3����a mol X��b mol Y�Ļ�����巢��������Ӧ����Ӧ��ijʱ�̸����ʵ���ǡ�����㣺n��X��=n��Y��=2n��Z������ԭ���������a��b=___________��
���ں��º��ݵ��ܱ������У����������������ٷ����仯ʱ���ٻ�������ѹǿ���ڻ��������ܶȣ��ۻ������������ʵ������ܻ�������ƽ����Է����������ݻ���������ɫ������Ӧ���������ķ�Ӧ����֮�ȵ��ڻ�ѧ������֮�ȡ�
��1��һ����֤��2SO2(g)��O2(g)![]() 2SO3(g)�ﵽƽ��״̬����_______������ţ�
2SO3(g)�ﵽƽ��״̬����_______������ţ�
��2��һ����֤��I2(g)��H2(g)![]() 2HI(g)�ﵽƽ��״̬���� _________��������ţ�
2HI(g)�ﵽƽ��״̬���� _________��������ţ�
��3��һ����֤��A(s)��2B(g)![]() C(g)��D(g)�ﵽƽ��״̬����________����ע��B,C,D��Ϊ��ɫ���ʣ�
C(g)��D(g)�ﵽƽ��״̬����________����ע��B,C,D��Ϊ��ɫ���ʣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�ӦaA(g)+bB(g) ![]() pC(g)����֪���ﵽƽ��������¶ȣ�B��ת���ʱ��Сѹǿ��C������������С��
pC(g)����֪���ﵽƽ��������¶ȣ�B��ת���ʱ��Сѹǿ��C������������С��
��1���÷�Ӧ���淴Ӧ��________��Ӧ����������������������������a+b______p������<������>������=������
��2���¶ȡ�����������䣬ƽ������B��A��ת����_________��B��ת����_________��������������������С��������������
��3���������¶ȣ��ٴ�ƽ��ʱ��B��C��Ũ��֮�Ƚ�_____________��������������������С��������������
��4��������������ٴ�ƽ��ʱ��������������ʵ���___________��������������������С��������������
��5����B����ɫ���壬A��C��ɫ��ƽ���ѹ���������Ϊԭ����һ�룬�ٴ�ƽ��ʱ��������������ɫ____����ά������������ѹǿ���䣬����Ne���ٴ�ƽ��ʱ��������������ɫ__________��������������������dz��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ش��������⣺
��1������>������<��������
�ǽ����� | �۵� | �е㣨ͬѹ�� | ���� |
P___S | MgO ___CaS | CF4 ___SiCl4 | H-Cl___H-Br |
��2��һ����ȡNH2OH�ķ�ӦΪ2NO2-+4SO2+6H2O+6NH3=4S042-+6NH4++2NH2OH��
��N��H��O�ĵ縺�Դ�С�����˳��Ϊ____��
��NH2OH��Nԭ�ӵ��ӻ�����Ϊ____��
��NHOH��������H2O������Ϊ���Ƕ��Ǽ��Է����⣬����Ϊ____��
��3�������K[PtCl3��NH3��]��[PtCl3��NH3��]-�Ľṹ����ʾ��ͼ��ʾΪ_____�������ǿռ乹�ͣ���1molK[PtCl3��NH3��]�к�����������ĿΪ____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X��Y��Z��ԭ������֮��Ϊ22����Y2����Z3����������Ų���ͬ�����л�������ͬʱ���ڼ��Թ��ۼ��ͷǼ��Թ��ۼ�����(����)
A.X2Y2B.X2YC.Z2Y3D.X3ZY3
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com