
(12分)甲醇是重要的燃料,有广阔的应用前景:工业上一般以CO和为原料合成甲醇,该反应的热化学方程式为:

(1)下列措施中有利于增大该反应的反应速率且利于反应正向进行的是_____。
a.随时将CH3OH与反应混合物分离
b.降低反应温度
c.增大体系压强
d.使用高效催化剂
(2)已知:
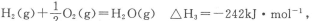
则表示1mol气态甲醇完全燃烧生成CO2和水蒸气时的热化学方程式为___________________.
(3)在容积为2L的恒容容器中,分别研究在三种不同温度下合成甲醇,下图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为2mol)与CO平衡转化率的关系。请回答:

①在图中三条曲线,对应的温度由高到低的顺序是__________________;
②利用a点对应的数据,计算出曲线Z在对应温度下 的平衡常数:K=______;
的平衡常数:K=______;
(4)恒温下,分别将1 molCO和2molH2置于恒容容器I和恒压容器Ⅱ中(两容器起始容积相同),充分反应。
①达到平衡所需时间是I _____Ⅱ(填“>”、“<”或“=”,下同)。达到平衡后,两容器中CH3OH的体积分数关系是I_____Ⅱ。
②平衡时,测得容器工中的压强减小了30%,则该容器中CO的转化率为______。
(1)c(2)CH3OH(g)+3/2O2=CO2(g)+2H2O(g)△H=-651KJ﹒mol-1(3)①Z>Y>X②1/4(4)①><②45%
【解析】
试题分析:(1)a、将甲醇分离,甲醇浓度减小,配合正向移动,反应速率减小,不选;b、降低温度,反应速率减小,平衡正向移动,不选;c、增大压强,反应速率增大,平衡正向移动,选;d、使用催化剂,反应速率加快,但平衡不移动,不选;所以选c。(2)根据盖斯定律分析,将方程式标记为①②③,运用-①+②+③,将方程式加减,得到热化学方程式为:CH3OH(g)+3/2O2=CO2(g)+2H2O(g)△H=-651KJ﹒mol-1(3)①根据方程式分析,因为温度升高,平衡逆向移动,一氧化碳的转化率增大,所以对应的温度为:Z>Y>X。②a点一氧化碳的转化率为50%,列式计算,
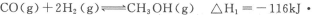
初始物质的里量浓度11.50
改变的物质的量浓度0.510.5
平衡时物质的量浓度0.50.50.5
平衡常数=(0.5)2/[(0.5×(0.5)3]=4。若方程式颠倒,则平衡常数为倒数,所以平衡常数为1/4。(4)①在恒容容器中随着反应的进行,体系的压强越来越小,所以Ⅰ中反应速率慢,所以需要的时间长。压强越小,平衡逆向移动,甲醇的体积分数越小。②列式计算:
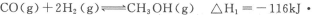
起始物质的量 1 2 0
改变的物质的量 x 2x x
平衡的物质的量 1-x 2-2x x
1-x+2-2x+x=(1+2)*1-30%x=0.45,所以一氧化碳的转化率=0.45/1=45%。
考点:化学平衡的计算。


科目:高中化学 来源:2014-2015四川省广安市高一期末考试化学试卷(解析版) 题型:选择题
有一无色透明溶液,取出少量滴入BaCl2溶液,只有白色沉淀生成;另取一定体积的无色溶液加入过量Na2O2,有无色无味气体产生,同时有白色沉淀生成,其沉淀量与加入Na2O2的量的关系如图所示,根据以上判断在①NH4+ ②H+ ③Al3+ ④Fe2+⑤Mg2+⑥NO3- ⑦CO32-⑧SO42-中一定存在的离子是

A.②③⑤⑧ B.③⑤⑦⑧
C.③④⑤⑧ D.②③⑤⑦⑧
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省聊城市茌平等三县高二上学期期末联考化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.焓变是一个与反应能否自发进行有关的因素,放热反应具有自发进行的倾向
B.在同一条件下物质有不同的熵值,其体系的混乱程度越大,熵值越大
C.自发反应是指不需要条件就能发生的反应
D.—个反应能否自发进行与焓变和熵变的共同影响有关
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省菏泽市高一上学期期末考试化学A试卷(解析版) 题型:选择题
对下列实验现象的解释正确的是
现 象 | 解 释 | |
A | Na2O2 投入到 FeCl2 溶液中得到大量红褐色沉淀 | Na2O2 具有还原性 |
B | 浓硝酸在光照条件下变黄 | 浓硝酸不稳定,生成的有色产物能溶于浓硝酸 |
C | 向某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 | 说明该溶液中含有SO42- |
D | 向盐酸中加入浓硫酸时产生白雾 | 说明浓硫酸具有脱水性 |
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省菏泽市高一上学期期末考试化学A试卷(解析版) 题型:选择题
下列对物质的分类正确的是
A.烧碱、纯碱、熟石灰都是碱
B.Na2O、Al2O3、Fe2O3都是碱性氧化物
C.H2SO4、NaOH、NaNO3都是电解质
D.铝土矿、水玻璃、小苏打都是混合物
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省德州市高二2月期末统考化学试卷(解析版) 题型:选择题
已知反应 ,达平衡时,要使c(A)增大同时使v(正)增大,应改变的条件为
,达平衡时,要使c(A)增大同时使v(正)增大,应改变的条件为
A.减小容器容积 B.增大容器容积
C.减小B的浓度 D.降温
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省德州市高二2月期末统考化学试卷(解析版) 题型:选择题
物质的量浓度相同的下列溶液中,NH4+浓度最大的是
A.NH4Cl B.NH4HSO4 C.CH3COONH4 D.NH3.H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省高一上学期期末化学试卷(解析版) 题型:选择题
在下列溶液中,各组离子一定能够大量共存的是
A.使酚酞变红的溶液:Na+ Cl- SO42- AlO2-
B.某无色溶液:CO32- NO3- Al3+ Ba2+
C.加入Al能放出H2的溶液中 NH4+、Cl-、Na+、SO42-
D.酸性溶液中: NO3-、SO32-、Na+、Fe3+
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省高二上学期期末考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.分子晶体的熔点比金属晶体的低
B.在晶体中只要有阳离子,一定有阴离子
C.在SiO2晶体中,Si原子与Si—O键数目比为1:2
D.离子化合物中可能含有非极性共价键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com