
����Ŀ��ij��Ӧ�з�Ӧ�����������У�AsH3��H2SO4��KBrO3��K2SO4��H3AsO4��H2O��һ��δ֪����X��
��1����֪KBrO3�ڷ�Ӧ�еõ����ӣ�����_____�����������ԭ������Ӧ����÷�Ӧ�Ļ�ԭ����________��
��2����֪0.2molKBrO3�ڷ�Ӧ�еõ�1mol��������X����X�Ļ�ѧʽΪ____��
��3������������Ӧ����֪________(�����)��
a�������ԣ�KBrO3>H3AsO4
b�������ԣ�H3AsO4>HBrO3
c����ԭ�ԣ�AsH3>X
d����ԭ�ԣ�X>AsH3
��4�����������ͻ�ԭ���Ļ�ѧʽ������ƽ���ϵ���������з����У����������ת�Ƶķ������Ŀ��_____________
![]() ��
��![]()
���𰸡���ԭ AsH3 Br2 ac 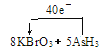
��������
���⿼����������ԭ��Ӧ�Ļ��������Լ��������ɡ�ͨ����ʧ�����غ㣬�����ж�����������ԭ������������ͻ�ԭ�����һ����������غ��ϵ���Ϳ����ж�����X����ɣ�����������ԭ��Ӧ��ǿ�����ɼ��ɶ����ʵ������Ժͻ�ԭ�Խ����жϡ�
(1)������ԭ��Ӧ�У��õ��ӵ����������������������ǻ�ԭ��Ӧ����������и��������ʣ��������Ԫ��һ����Br����һ����As������Br������ԭ��Ӧ������AsӦ�÷���������Ӧ����ô��ԭ����ΪAsH3��
(2)�����֪��X��KBrO3�Ļ�ԭ�������Ϊ0.2molKBrO3�ܵ�1mol��������X������X��Br�ļ�̬Ϊ0�ۣ�����Xֻ��ΪBr2��
(3)�ۺϷ���(1)��(2)����֪���÷�Ӧ��������ΪKBrO3����������ΪH3AsO4����ԭ��ΪAsH3����ԭ����ΪBr2�����Ը���������ԭ��Ӧ��ǿ�����ɿ�֪�������ԣ�KBrO3��H3AsO4����ԭ�ԣ�AsH3��Br2��
(4)����������KBrO3��AsH3�Ļ�ѧ����ϵ����Ϊ8:5�����Դ�Ϊ��



 ����������������ϵ�д�
����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и���������ָ����Һ��һ���ܴ����������(����)
A.ij��ɫ��������Һ�У�K����H����Fe2����Cl��
B.��0.1 mol��L��1OH������Һ�У�Na����K����![]() ��ClO��
��ClO��
C.��0.1 mol��L��1![]() ����Һ�У�K����Ca2����
����Һ�У�K����Ca2����![]() ��
��![]()
D.��0.1 mol��L��1OH������Һ�У�Fe3����![]() ��Cu2����
��Cu2����![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������a mol FeI2����Һ�У�ͨ��x mol Cl2�����и���Ϊͨ��Cl2�����У���Һ�ڷ�����Ӧ�����ӷ���ʽ�����в���ȷ����
A. x��a��2I+Cl2��I2+2Cl
B. x=1.2a��10Fe2++14I+12Cl2��10Fe3++7I2+24Cl
C. x=1.4a��4Fe2++10I+7Cl2��4Fe3++5I2+14Cl
D. x��1.5a��2Fe2++4I+3Cl2��2Fe3++2I2+6Cl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС����������(�� Al2O3��Fe2O3�� SiO2)Ϊԭ�Ͻ�������̽��(��������)��������������
![]()
A. ����٢ڹ����о�����˲���
B. a��b����Ԫ�صĻ��ϼ���ͬ
C. ��Ӧ�۵Ļ�ѧ����ʽΪ��2 NaAlO2��3H2O��CO2 = 2Al(OH)3����Na2CO3
D. dֻ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1���ҹ��Ǽ��⼼���Ƚ��Ĺ��ң��챦ʯ��Al2O3�����������ڲ�������IJ��ϡ��������ӷ���ʽ��֤������һ�����������____________��___________��
��2��ȡ������������ijþ���Ͻ�ֱ����������ϡ���������������Һ�У������ı�״����H2����ֱ�Ϊ33.6L��22.4L��úϽ���þ���������ʵ���֮��Ϊ___________��
��3����һ��������þ���Ͻ��ܽ���500mL�����У���Ӧ�����Һ����μ���2mol/LNaOH��Һ�������������������Һ����Ĺ�ϵ��ͼ��ʾ������������ʵ���Ũ�ȣ����跴Ӧǰ����Һ����ı仯���Բ��ƣ�_______________�������������������ֵ_____________g��
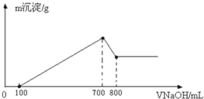
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼��������������������������塢�ϳɶ������̺������������ε�ԭ�ϣ�����ҽҩ���纸������ԭ�ϵȡ���ҵ�����Ȼ�隣������̿���Ʊ��ߴ���̼���̵Ĺ����������£�
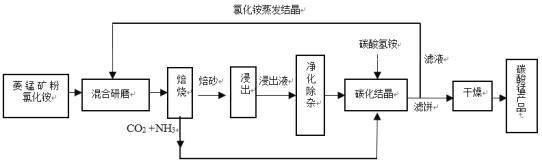
��֪�������̿�۵���Ҫ�ɷ���MnCO3����������Fe��Al��Ca��Mg��Ԫ�ء�
����ؽ���Mn+����Ũ��c(Mn+)=0.1 mol L -1���γ�M(OH)n������pH��Χ���£�
�������� | Fe2+ | Fe3+ | Al3+ | Mn2+ | Mg2+ |
��ʼ������pH | 6.3 | 1.5 | 3.8 | 8.8 | 9.6 |
������ȫ��pH | 8.3 | 2.8 | 5.2 | 10.8 | 11.6 |
�۳����£�Ksp(CaF2) =1.46��10-10��Ksp(MgF2) = 7.30��10-11
�ش��������⣺
(1)�����ĥ��ϸ�۵�Ŀ����_________________��
(2)��������ʱ��������Ҫ��Ӧ�Ļ�ѧ����ʽΪ_____________��
(3)����Һ�������������������£����ȼ���MnO2��Fe2+����ΪFe3+����Ӧ�����ӷ���ʽΪ________���ٵ�����ҺpH��ΧΪ________��Al3+��Fe3+��Ϊ������ȥ���ټ���NH4F����Ca2+��Mg2+����c(Ca2+)=1.0��10-5molL-1ʱ��c(Mg2+)=______molL-1��
(4)̼���ᾧ�����в�����(NH4)2CO3��Һ����NH4HCO3��Һ���ܵ�ԭ����_________��
(5)�ڲ��������п���ѭ�����õ�������__________��
(6)�ⶨ̼���̲�Ʒ�Ĵ��ȡ�
��ȡ0.2500g̼���̲�Ʒ����ƿ�У���25.00 mL���ᣬ���ȣ�̼����ȫ��ת��Ϊ[Mn(PO4)2]3-����ȴ�����¡���ˮϡ����50 mL���μ�2��3��ָʾ����Ȼ����Ũ��Ϊ0.2000 mol��L-1�����������[(NH4)2Fe(SO4)2]����Һ�ζ�(��ӦΪ��[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2![]() )���ظ�����3�Σ���¼�������±���
)���ظ�����3�Σ���¼�������±���
�ζ� ���� | 0.2000mol��L-1����������隣���Һ����(mL) | |
�ζ�ǰ | �ζ��� | |
1 | 0.10 | 10.20 |
2 | 0.22 | 11.32 |
3 | 1.05 | 10.95 |
���Ʒ�Ĵ���=____________�����ζ��յ�ʱ���Ӷ��������õ�̼���̴ֲ�Ʒ�Ĵ���__________��(����ƫ��������ƫ����������Ӱ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�������ͽ��۶���ȷ����
ʵ�� | ���� | ���� |
A�����������Na2SiO3������Һ��Сľ�������ɺ���ھƾ���������� | Сľ������ȼ�� | Na2SiO3��������� |
B���ⶨŨ�Ⱦ�Ϊ0.1 mol��L-1��CH3COONa��HCOONa��Һ��pH | CH3COONa��Һ��pH�ϴ� | ���H���������� HCOO-��CH3COO- |
C��ij��Һ�м�ŨNaOH��Һ���� | ������ʹʪ�����ɫʯ����ֽ���ɫ������ | ԭ��Һ���� |
D����SO2ͨ�����Ը��������Һ�� | ��Һ��ɫ | SO2����Ư���� |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������![]() (��ʽ̼��п)���ڸ߶˾�ϸ������Ʒ,����������
(��ʽ̼��п)���ڸ߶˾�ϸ������Ʒ,����������![]() ,������ˮ�ʹ���ij��Уʵ�����ù�ҵ������п(��Ҫ�ɷ�Ϊ
,������ˮ�ʹ���ij��Уʵ�����ù�ҵ������п(��Ҫ�ɷ�Ϊ![]() ,������
,������![]() )�Ʊ���������ʽ̼��п��Ʒ��������ͼ��ʾ:
)�Ʊ���������ʽ̼��п��Ʒ��������ͼ��ʾ:
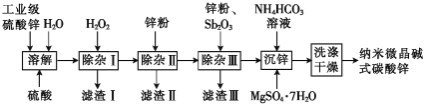
��֪:a.![]() ��
��![]() �ֱ���37.4��15.4��16.2��
�ֱ���37.4��15.4��16.2��
b.��������Һ�е�����Ũ��С��![]() ʱ����Ϊ������ȫ��
ʱ����Ϊ������ȫ��
c.������������Ҫ����Ԫ����![]() ��
��
(1)����������Ŀ���dz�ȥ��Һ�е���Ԫ��,��![]() ��������________________;����Һ��
��������________________;����Һ��![]() ,�˹����л�Ӧ������Һ��
,�˹����л�Ӧ������Һ��![]() ��____��Χ(���������Ӽ���Ӱ��)��
��____��Χ(���������Ӽ���Ӱ��)��
(2)��������������������Ϊ��ԭ���ӡ�
������������Ҫ����Ԫ����_________________________
�����������м����![]() ����Һ����Ҫ��
����Һ����Ҫ��![]() ��ʽ���ڡ���д��п��
��ʽ���ڡ���д��п��![]() ��Ӧ�����������仯������
��Ӧ�����������仯������![]() (
(![]() �и�Ԫ�ػ��ϼ���Ϊ0��)�����ӷ���ʽ:___________________________
�и�Ԫ�ػ��ϼ���Ϊ0��)�����ӷ���ʽ:___________________________
(3)����п����õ��Ĺ�������ȥ����ˮϴ��,�����Ҵ�ϴ�ӡ����Ҵ�ϴ�ӵ�Ŀ����_______________________
(4)����![]() ����ҪĿ���ǽ�����Ʒ��������,����Ԫ��
����ҪĿ���ǽ�����Ʒ��������,����Ԫ��![]() ����������������56%���ϡ���þ��п��������ֵ����,
����������������56%���ϡ���þ��п��������ֵ����,![]() �����ܻ�����_________(�ѧʽ),�Ӷ�����Ʒ���Ӱ�졣
�����ܻ�����_________(�ѧʽ),�Ӷ�����Ʒ���Ӱ�졣
(5)��Ʒ��п�ĺ�������![]() (�ɱ�ʾΪ
(�ɱ�ʾΪ![]() )�ζ��ⶨ,��Ӧ�����ӷ���ʽΪ
)�ζ��ⶨ,��Ӧ�����ӷ���ʽΪ![]() ��ȡ
��ȡ![]() ��������ʽ̼��п��Ʒ,���ܺ�õ�pHΪ5~6����Һ,�Զ��ӳ���ָʾ��,��
��������ʽ̼��п��Ʒ,���ܺ�õ�pHΪ5~6����Һ,�Զ��ӳ���ָʾ��,��![]() ����Һ�ζ�,����
����Һ�ζ�,����![]() ��Һ
��Һ![]() ,����Ʒ��п������������_______(�ô���ʽ��ʾ)��
,����Ʒ��п������������_______(�ô���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO��H2����Ϊ��Դ�ͻ���ԭ�ϣ�Ӧ��ʮ�ֹ㷺����ҵ�Ͽ�����CO��CO2��H2��Ӧ���Ʊ��״���
��Ӧ�٣�2H2(g)+CO(g)![]() CH3OH(g)��H����90.8kJ��mol-1
CH3OH(g)��H����90.8kJ��mol-1
��Ӧ�ڣ�H2(g)+CO2(g)![]() H2O(g)+CO(g)��H��+41.2kJ��mol-1
H2O(g)+CO(g)��H��+41.2kJ��mol-1
��1��д����CO2��H2��Ӧ�Ʊ��״����Ȼ�ѧ����ʽ______________��
��2����֪�������һ����̼��ˮ�������뷴Ӧ��ʱ���ᷢ�����·�Ӧ��CO(g)+H2O(g)![]() H2(g)+CO2(g)���÷�Ӧƽ�ⳣ�����¶ȵı仯�����ʾ��
H2(g)+CO2(g)���÷�Ӧƽ�ⳣ�����¶ȵı仯�����ʾ��
�¶�/�� | 400 | 500 | 800 |
ƽ�ⳣ��K | 9.94 | 9 | 1 |
�����¶ȣ���ƽ����ƶ�������______________�������������500��ʱ��CO��H2O����ʼŨ�Ⱦ�Ϊ0.020mol��L-1����������CO��ƽ��Ũ��Ϊ��______________mol��L-1��
��3��һ�������£�������CO2(g)��H2(g)�ϳ�CH4(g)��ͬʱ������H2O(g)��������ܱ������г���һ������CO2��H2����300��ʱ����������Ӧ��10min�ﵽƽ��ʱ�������ʵ���Ũ����ͼ��ʾ,���¶��µĵ�ƽ�ⳣ������_______________��
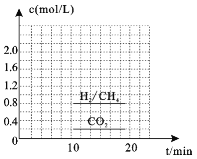
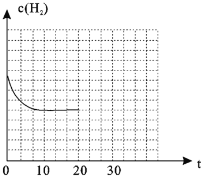
��4������20minʱ��Сѹǿ������30minʱ�ﵽƽ��״̬������ͼ2�л���H2�����ʵ���Ũ����ʱ��仯��ͼ��__________________��
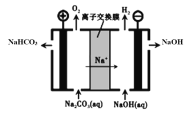
��5����ҵ�ϵ��Na2CO3��Һ��������NaHCO3��NaOH���ֹ�ҵ��Ҫԭ�ϣ�װ����ͼ��ʾ����д�������ĵ缫��Ӧʽ______________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com