
| A、已知25℃时,有关弱酸的电离平衡常数:HCN Ka=4.9×10-10; H2CO3 Ka1=4.3×10-7,Ka2=5.6×10-11.则将少量CO2通入NaCN溶液中反应的化学方程式为:2NaCN+H2O+CO2═2HCN+Na2CO3 |
| B、将pH=6的H2SO4稀释1000倍后,c(H+)=200c(SO42-) |
| C、已知CaCO3的Ksp=2.8×10-9,现将等体积的Na2CO3溶液与CaBr2溶液混合,若CaBr2溶液的浓度为 5.6×10-5 mol/L,则生成沉淀所需Na2CO3溶液的最小浓度为5×10-5mol/L |
D、 在不同条件下进行的异构化反应X?Y的进程图解如图所示.图中的“  ”是X,“ ”是X,“ ”是Y,则可以计算得到乙的平衡常数K=1,且比甲的平衡常数要小 ”是Y,则可以计算得到乙的平衡常数K=1,且比甲的平衡常数要小 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:

| A、图①可以表示F-、Na+、Mg2+、Al3+四种离子的离子半径大小关系 |
| B、图②可以表示ⅡA族元素的最外层电子数 |
| C、图③可以表示ⅥA族元素氢化物的沸点高低关系 |
| D、图④可以表示第三周期中的非金属元素对应单质的熔点高低关系 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ;(吸热反应)
;(吸热反应)| A、NBD的内能比Q的内能高 |
| B、NBD和Q互为同分异构体 |
| C、Q的一氯代物只有3种 |
| D、NBD的二氯代物可有9种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(A)=0.15mol?L-1?s-1 |
| B、v(B)=0.6mol?L-1?s-1 |
| C、v(C)=0.5mol?L-1?s-1 |
| D、v(D)=0.4mol?L-1?s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、光导纤维的主要化学成分是SiO2 |
| B、SiO2和CO2都是酸性氧化物,都能与强碱溶液反应 |
| C、SiO2和CO2都能溶于水且与水反应生成相应的酸 |
| D、硅属于非金属,是良好的半导体材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示.
某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示.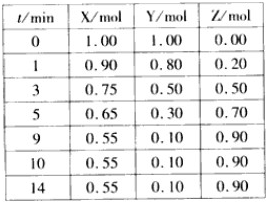
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com