
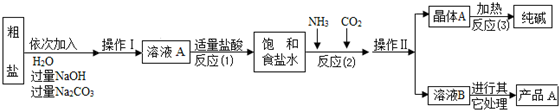
| ѡ���װ�� �����ţ� |
ʵ������ | ʵ����� |
| ��Ʒ��������A |

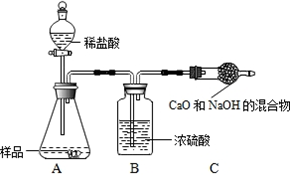
| 8.67g |
| 10g |


 ���ٴ�����ɽ����ϵ�д�
���ٴ�����ɽ����ϵ�д� ���ٴ���������ѧϰ����ѧ�ں����ν�ϵ�д�
���ٴ���������ѧϰ����ѧ�ں����ν�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ʵ������Ũ������MnO2��Ӧ��Cl2��MnO2+2H++2Cl-�TCl2��+Mn2++H2O |
| B������״����1.12 L����ͨ��10 mL1 mol/L���廯������Һ�У�2Fe2++4Br-+3Cl2�T2Fe3++6Cl-+2Br2 |
| C����NaOH��Һ�еμ�ͬŨ�ȵ�����Ca��HCO3��2��Һ��Ca2++HCO3-+OH-�TCaCO3��+H2O |
| D��Fe��OH��3��������Fe��OH��3+3H+�TFe3++3H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������Ӳ֬�ụΪͬϵ�C2H6��C9H20Ҳ��Ϊͬϵ�� |
| B������������������Ӫ�����ʣ��侧����Ҫ��������ʽ���ڣ�������Һ��pH�ɸı������ܽ�� |
| C��������ͱ���������ˮ����������3�ֶ��� |
| D��������Һ�м��뱥�ͣ�NH4��2SO4��Һ���г����������ټ�ˮ�������ܽ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ۺ���ά�� |
| B�����Ǻ���ѿ��? |
| C������������� |
| D���ʰ������������飨C2H5NO2��? |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
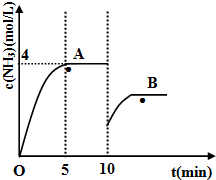 ���û�ѧ��Ӧԭ���о��������ȡ���ȵ��ʼ��仯����ķ�Ӧ����Ҫ���壮
���û�ѧ��Ӧԭ���о��������ȡ���ȵ��ʼ��仯����ķ�Ӧ����Ҫ���壮| ѹǿ/MPaת����/%�¶�/�� | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
| 7 |
| 10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
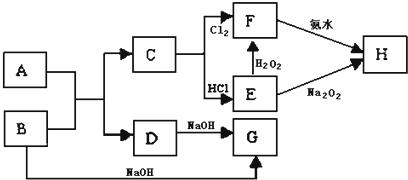
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��ϵ | c��SO2�� mol/L | c��O2�� mol/L | c��SO3�� mol/L | ��Ӧ���� |
| ��1�� | 0.0600 | 0.400 | 2.00 | |
| ��2�� | 0.0960 | 0.300 | 0.500 | |
| ��3�� | 0.300 | 0.0400 | 1.44 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com