
【题目】Ⅰ甲醚作为一种基本化工原料,由于其良好的易压缩、冷凝、汽化特性,使甲醚在制药、燃料、农药等化学工业中有许多独特的用途。
(1)已知:2CH3OH(g) ![]() CH3OCH3(g)+H2O(g) ΔH=-25 kJ·mol-1,某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
CH3OCH3(g)+H2O(g) ΔH=-25 kJ·mol-1,某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
![]()
①平衡时,c(CH3OCH3)等于________ mol·L-1,反应混合物的总能量减少________ kJ。
②若在平衡后的容器中再加入与起始时等量的CH3OH,请在下图中画出CH3OH的浓度的曲线示意图。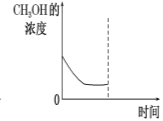
Ⅱ甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+ CO(g)![]() CH3OH(g)
CH3OH(g)
(2)下表所列数据是该反应在不同温度下的化学平衡常数(K)
![]()
①该反应的平衡常数表达式K= ,△H 0(填“>”、“<”或“=”).
②按下列物质的量发生反应,CO的转化率由大到小的顺序是 (填甲乙丙).

(3)已知在常温常压下:化学反应①②③④的平衡常数分别为K1,K2,K3,K4
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) K1
②2CO(g)+O2(g)=2CO2(g)K2
③H2O(g)=H2O(l)K3
④CH3OH(l)+O2(g)=CO(g)+2H2O(l)K4
则K4= (用含有K1,K2,K3的代数式表达)
【答案】
Ⅰ(1)①1.6 , 40 , ②如图所示
Ⅱ(2)①K= ![]() ②< ③甲>丙>乙 (3)
②< ③甲>丙>乙 (3)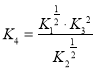
【解析】
试题分析:(1)①根据表中数据以及反应的化学方程式可知甲醇的起始浓度是0.8mol/L+1.24mol/L×2=3.28mol/L
2CH3OH(g) ![]() CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
起始浓度(mol/L) 3.28 0 0
转化浓度(mol/L) 2x x x
平衡浓度(mol/L)3.28-2x x x
则![]()
解得x=1.6
所以平衡时,c(CH3OCH3)等于1.6mol·L-1。消耗甲醇是3.2mol,所以反应混合物的总能量减少![]() 。
。
②若在平衡后的容器中再加入与起始时等量的CH3OH,则相当于是增大压强,反应前后体积不变,则平衡
(2)①在一定温度下,一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓度幂之积的比值是一个常数比值,根据方程式可知该反应的平衡常数表达式K=![]() 。根据表中数据可知升高温度平衡常数减小,这说明升高温度平衡向逆反应方向进行,因此上述反应的正反应是放热反应,则△H<0。
。根据表中数据可知升高温度平衡常数减小,这说明升高温度平衡向逆反应方向进行,因此上述反应的正反应是放热反应,则△H<0。
②甲相当于在丙的基础上增大氢气浓度,提高CO的转化率。乙相当于在丙的基础上增大CO浓度,提高氢气的转化率,但降低CO的转化率,则CO的转化率由大到小的顺序是甲>丙>乙。
(3)已知①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) K1
②2CO(g)+O2(g)=2CO2(g)K2
③H2O(g)=H2O(l)K3
④CH3OH(l)+O2(g)=CO(g)+2H2O(l)K4
则根据盖斯定律可知①÷2+③×2-②÷2即得到反应④,所以反应④的平衡常数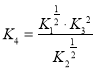 。
。


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
【题目】实验室使用的浓盐酸的溶质质量分数为36.5%,密度为1.19 g·cm-3,则物质的量浓度是( )
A.11.9 B.11.9 mol·L-1 C.0.012 mol·L-1 D.无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有通式均为(CH2O)n的六种有机物,性质如下:
①A是无色有刺激性的气体,可发生银镜反应
②B、C、D的式量均为A的2倍,E的式量的是A的3倍,F的式量是A的6倍
③B、E的水溶液可使紫色石蕊试液变红,还可与乙醇在一定条件下酯化
④E结构中含有—CH3,两分子E 可形成环状酯
⑤C不溶于水,D、F二种物质的水溶液均呈中性,C既能水解,又能发生银镜反应,D不能发生水解反应,却能发生银镜反应,还能与钠反应放出H2,F能发生银镜反应,淀粉水解可得F。
(1)请推断各物质的结构简式:
A ______________、 B__________________、 C ______________、D_______________、 E__________________、 F________________。
(2)请分别写出符合下列要求的E的同分异构体的结构简式:
①能发生银镜反应和酯化反应,又能发生水解反应 ;
②能发生银镜反应和酯化反应,不能发生水解反应 ;
(3)写出A发生银镜反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从结构的角度可以帮助我们更好的理解有机物的化学性质。
(1) 乙炔是一种重要的化工原料,将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀。Cu+基态核外电子排布式为____________。乙炔与氢氰酸反应可得丙烯腈H2C=CH-C≡N。丙烯腈分子中碳原子轨道杂化类型是____________。[Cu(NH3)2]Cl的氨水溶液在空气中放置迅速由无色变为深蓝色,写出该过程的离子方程式______________________。
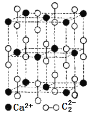
(2)实验室制乙炔使用的电石主要含有碳化钙,写出碳化钙的电子式______________, CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),但CaC2晶体中有哑铃形![]() 的存在,使晶胞沿一个方向拉长。CaC2晶体中1个Ca2+周围距离最近的
的存在,使晶胞沿一个方向拉长。CaC2晶体中1个Ca2+周围距离最近的![]() 数目为____________。已知CaC2晶体的密度为2.22g/cm3,该晶胞的体积为____________cm3
数目为____________。已知CaC2晶体的密度为2.22g/cm3,该晶胞的体积为____________cm3
(3) 甲醇催化氧化可得到甲醛,甲醛分子中的键角大约为____________,甲醇的沸点比甲醛的高,其主要原因是_____________________。
(4)已知苯酚具有弱酸性,其Ka=1.1 ×10-10;水杨酸第一级电离形成的离子为![]() 判断相同温度下电离平衡常数Ka2(水杨酸)_______Ka(苯酚)(填“>”或“<”),其原因是___。
判断相同温度下电离平衡常数Ka2(水杨酸)_______Ka(苯酚)(填“>”或“<”),其原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 NA为阿伏加德罗常数的值。有关草酸(HOOC-COOH)的下列说法错误的是( )
A.9.0g草酸中共用电子对数目为0.9NA
B.9.0 g草酸被NaClO氧化生成CO2,转移的电子数为0.2 NA
C.9.0 g草酸溶于水,其中C2O42-和HC2O4-的微粒数之和为0.1NA
D.9.0g草酸受热完全分解为CO2、CO、H2O,标况下测得生成的气体体积为4.48 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组依据反应AsO43-+2I-+2H+![]() AsO33-+I2+H2O设计如图原电池,探究pH对AsO43-氧化性的影响。测得电压与pH的关系如图。下列有关叙述错误的是
AsO33-+I2+H2O设计如图原电池,探究pH对AsO43-氧化性的影响。测得电压与pH的关系如图。下列有关叙述错误的是
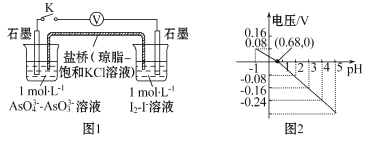
A.调节pH可以改变反应的方向
B.pH=0.68时,反应处于平衡状态
C.pH=5时, 负极电极反应式为2I--2e -= I2
D.pH>0.68时,氧化性I2>AsO43-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A.标准状况下,22.4L CHCl3含氯原子数为3NA
B.100mL 1 mol·L-1醋酸溶液中的氢原子数为0.4NA
C.常温常压下,11.2g乙烯中共用电子对数为2.4NA
D.6.4 g CaC2晶体中所含的离子总数为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2L容器中X、Y、Z三种物质的量随时间的变化曲线如图所示。由图中数据分析,

(1)达到平衡时,Y的浓度为_________________
(2)反应开始至2min,Z的平均反应速率为_____________
(3)该反应的化学方程式为______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com