
2- 4 |


科目:高中化学 来源: 题型:
| 测定序号 | 待测溶液的体积(mL) | 所耗盐酸标准液的体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 1 | 20.00 | 0.50 | 20.78 |
| 2 | 20.00 | 1.20 | 21.32 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
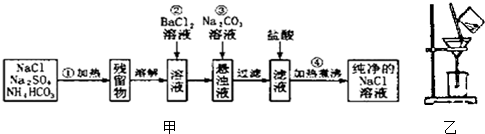
| 操作① |
| 加试剂A |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、凡是分子组成相差一个或几个CH2原子团的物质,彼此一定是同系物 |
| B、两种化合物组成元素相同,各元素质量分数也相同,则两者一定是同分异构体 |
| C、油脂、淀粉、纤维素、蛋白质都是高分子化合物、 |
| D、医院用紫外线灯消毒的依据的原理是紫外线能使病毒蛋白质发生变性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溴苯中的溴(NaOH溶液,分液) |
| B、乙酸乙酯中的乙醇(乙酸,分液) |
| C、苯中的苯酚(浓溴水,过滤) |
| D、乙醇中的乙酸(饱和Na2CO3溶液,分液) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com