
【题目】过氧化钙是一种温和的氧化剂,常温下为白色的固体,易溶于酸,难溶于水、乙醇等溶剂。某实验小组拟选用如图装置(部分固定装置略)制备过氧化钙。
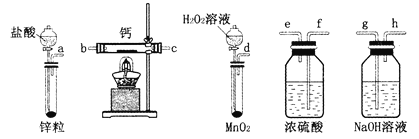
(1)请选择必要的装置,按气流方向连接顺序为____________(填仪器接口的字母编号,装置可重复使用)。
(2)根据完整的实验装置进行实验,实验步骤如下:
①检验装置的气密性后,装入药品;
②打开分液漏斗活塞,通入一段时间气体,加热药品;
③反应结束后,________(填操作);
④拆除装置,取出产物。
(3)一小组同学利用CaCl2在碱性条件下与H2O2反应制得。制备CaO2的实验方案和装置示意图:

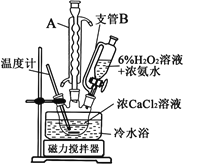
①三颈烧瓶中发生的主要反应的化学方程式为___________________________________;
②支管B的作用是_________________________;
③步骤③中洗涤CaO2·8H2O的液体X的最佳选择是____________;
A.无水乙醇B.浓盐酸C.水D.CaCl2溶液
④该反应常用冰水浴控制温度在℃左右,其可能的原因该反应是放热反应,温度低有利于提高CaO2·8H2O产率;________________________________________。
(4)测定产品中CaO2含量的实验步骤:
步骤一:准确称取ag产品于有塞锥形瓶中,加入适量蒸馏水和过量的bgKI晶体,再滴入少量2mol·L-1的硫酸,充分反应。
步骤二:向上述锥形瓶中加入几滴________(作指示剂)。
步骤三:逐滴加入浓度为cmol·L-1的Na2S2O3溶液至反应完全,滴定至终点,记录数据,再重复上述操作2次,得出三次平均消耗Na2S2O3溶液的体积为VmL。
CaO2的质量分数为________(用字母表示)。(已知:I2+2S2O32-===2I-+S4O62-)
【答案】dfebcf(或dfecbf) 熄灭酒精灯,待反应管冷却至室温,停止通入氧气,并关闭分液漏斗的活塞 CaCl2+H2O2+2NH3H2O+6H2O=CaO28H2O↓+2NH4Cl 平衡气压,便于恒压滴液漏斗中的液体能够顺利滴下 A 温度低可减少过氧化氢的分解,提高过氧化氢的利用率 淀粉溶液 ![]() %
%
【解析】
制备过氧化钙时,用双氧水制备氧气,钙属于极活泼的金属,极易与水反应生成氢氧化钙和氢气,而制备的氧气中会混有水蒸气,所以在与钙化合之前需要干燥,选用试剂是浓硫酸;同时为防止空气中水蒸气进入,最后还需要连接浓硫酸的洗气瓶。
(1)据分析可知制备过氧化钙时仪器正确的顺序;
(2)实验结束时为防止空气进入装置,还要继续通氧气直到装置冷却;
(3)①三颈烧瓶中氯化钙与双氧水发生反应,生成CaO28H2O沉淀和NH4Cl;
②支管B的作用是平衡气压,便于恒压滴液漏斗中的液体能够顺利滴下;
③根据过氧化钙(CaO2)难溶于水,可与水缓慢反应;不溶于醇类、乙醚等选择洗涤CaO28H2O的最佳试剂;
④该反应常用冰水浴控制温度在0℃左右,其可能的原因该反应是放热反应,温度低有利于提高CaO28H2O产率;温度低可减少过氧化氢的分解,提高过氧化氢的利用率;
(4)过氧化钙氧化碘化钾生成碘单质,碘遇淀粉变蓝,故指示剂选淀粉溶液;根据电子转移守恒关系CaO2~I2~2S2O32-计算。
(1)制备过氧化钙时,用双氧水制备氧气,钙属于极活泼的金属,极易与水反应生成氢氧化钙和氢气,而制备的氧气中会混有水蒸气,所以在与钙化合之前需要干燥,选用试剂是浓硫酸;同时为防止空气中水蒸气进入,最后还需要连接浓硫酸的洗气瓶,所以正确的顺序为:dfebcf或dfecbf;
(2)实验结束时为防止空气进入装置,还要继续通氧气直到装置冷却,所以实验结束时的操作为熄灭酒精灯,待反应管冷却至室温,停止通入氧气,并关闭分液漏斗的活塞;
(3)①三颈烧瓶中氯化钙与双氧水发生反应,主要反应的化学方程式为CaCl2+H2O2+2NH3H2O+6H2O=CaO28H2O↓+2NH4Cl;
②支管B的作用是平衡气压,便于恒压滴液漏斗中的液体能够顺利滴下;
③过氧化钙(CaO2)难溶于水,可与水缓慢反应,不溶于醇类、乙醚等步骤③中洗涤CaO28H2O的液体X的最佳选择是无水乙醇;
④该反应常用冰水浴控制温度在0℃左右,其可能的原因该反应是放热反应,温度低有利于提高CaO28H2O产率;温度低可减少过氧化氢的分解,提高过氧化氢的利用率;
(4)过氧化钙氧化碘化钾生成碘单质,碘遇淀粉变蓝,故指示剂选淀粉溶液,设CaO2的质量分数为ω,根据电子转移守恒关系可知:
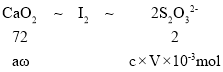
因此ω=![]() =
=![]() %
%


科目:高中化学 来源: 题型:
【题目】由环己烷可制得1,2—环己二醇,反应过程如下:

![]()
![]()
![]() A
A![]() B
B![]()

下列说法错误的是
A. ①的反应条件是光照B. ②的反应类型是消去反应
C. ③的反应类型是取代反应D. ④的反应条件是NaOH、H2O加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1×105Pa和298K时,将1mol气态AB分子分离成气态A原子和B原子所需要的能量称为键能(kJ/mol)。下面是一些共价键的键能:(已知氨分子中有三个等价的氮氢共价键)
共价键 | H-H键 | N三N键 | N-H键 |
键能(kJ/mo1) | 436 | 945 | 391 |
工业合成氨的化学方程式:N2+3H2![]() 2NH3
2NH3
(1)断开1molN2中的化学键需_______(填“吸收”或“放出”)_____kJ能量;
(2)形成2molNH3中的化学键需_______(填“吸收”或“放出”)__kJ能量;
(3)在298K时,取1molN2和3molH2放入一密闭容器中,在催化剂存在下进行反应。理论上放出或吸收的热量为Q1,则Q1为_____kJ。根据上表中的数据判断工业合成氨的反应是_______(填“吸热”或“放热”)反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】各种矿产资源的开发利用为人类发展提供了重要的物质保障,如图是一些矿产资源的利用流程,则下列说法不正确的是

A.粗铜电解精炼时,粗铜做阳极
B.黄铜矿冶炼铜时,副产物二氧化硫可用于生产硫酸,FeO可用作冶铁的原料。
C.生产铝、铜、高纯硅及玻璃过程中都涉及氧化还原反应
D.粗硅制高纯硅时,提纯四氯化硅可用多次分馏的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.有下列8种有机物按要求作答:
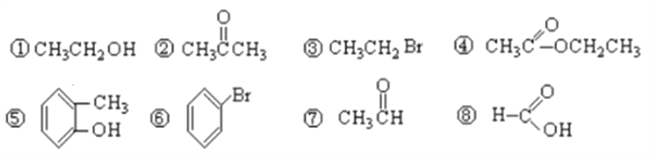
(1)按官能团分类,其中属于羧酸的有___________(填序号),属于醇的有_________(填序号);
(2)④中所含官能团的名称_______________,⑦中所含官能团结构简式_____________;
II.下列各组中的两种有机物,可能是:A.同一物质 B.同系物 C.同分异构体,请判断它们之间的关系(用字母完成填空):
(3)2-甲基丁烷和丁烷_______________;
(4)正戊烷和新戊烷_________________;
(5)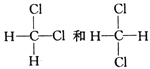 ______________。
______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是重要的化工原料,以乙烯为原料生产部分化工产品的流程如下(部分反应条件已略去):
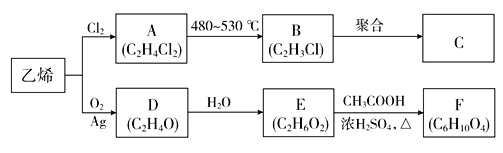
已知:E分子中含有两个羟基,且不连在同一个碳原子上。
请回答下列问题:
(1)由乙烯生成A的反应类型为________。
(2)C是一种常见的塑料,其化学名称为_________。
(3)D是环状化合物,其结构简式为__________________。
(4)写出下列反应的化学方程式:
①A→B:_____________________
②E→F:_____________________
(5)已知烯烃能发生如下反应:
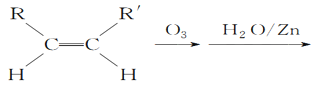 RCHO+R′CHO
RCHO+R′CHO
请写出下列反应产物的结构简式
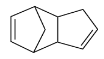
![]()
![]() ____________。
____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,回答下列问题:
IA | IIA | IIIA | IVA | VA | VIA | VIIA | ||
2 | ① | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
|
|
(1)写出①元素最高价氧化物的电子式和结构式________________ ,________________。
(2)这些元素的最高价氧化物的对应水化物中,________酸性最强(填化学式);________碱性最强(填化学式);能形成两性氢氧化物的元素是________(填元素符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物的性质与其所含官能团密切相关,按要求书写指定方程式。
(1)2—丁烯与氯化氢的反应:______;
(2)乙二酸与乙二醇反应生成环状酯:______;
(3)苯甲醛(![]() )与新制Cu(OH)2共热:______;
)与新制Cu(OH)2共热:______;
(4)苦杏仁酸(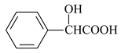 )发生缩聚反应生成的高分子化合物:______;
)发生缩聚反应生成的高分子化合物:______;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辣椒中含辣椒素,局部应用可助减轻疼痛。辣椒素酯类化合物的结构可以表示为: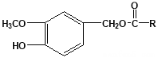 (R为烃基),其中一种辣椒素酯类化合物J的合成路线如下:
(R为烃基),其中一种辣椒素酯类化合物J的合成路线如下:
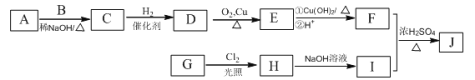
已知:
①A、B和E为同系物,其中B的相对分子质量为44,A和B核磁共振氢谱显示都有两组峰,峰面积比分别为9:1和3:1;
②化合物J的分子式为C15H22O4;
③
回答下列问题:
(1)G中含有的官能团有 、 。
(2)由C生成D的反应类型为 ,D的化学名称为 。
(3)①的化学方程式为 。
(4)J的结构简式为 。
(5)G的同分异构体中,苯环上的一氯代物只有一种的共有 种(不含立体异构),核磁共振氢谱显示2组峰的是 (写结构简式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com