
【题目】下表为元素周期表的一部分,请回答有关问题:
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
第2周期 | ① | ② | ||||||
第3周期 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)元素⑥的原子结构示意图___________;写出⑤的氧化物的一种用途__________。
(2)表中⑤和⑥气态氢化物的稳定性顺序为 ______ >______(填氢化物的化学式);
(3)表中能形成两性氢氧化物的元素是_________(填元素符号),该元素的单质与③的氢氧化物水溶液反应的离子反应方程式_______________。
【答案】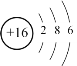 光导纤维 H2S SiH4 Al 2Al+2OH-+2H2O=2AlO2-+3H2↑
光导纤维 H2S SiH4 Al 2Al+2OH-+2H2O=2AlO2-+3H2↑
【解析】
根据8种元素在周期表中的位置,推出①为N,②为F,③为Na,④为Al,⑤为Si,⑥为S,⑦为Cl,⑧为Ar,然后利用元素周期律、元素及其化合物的性质等知识进行分析;
(1)⑥为S,其原子结构示意图为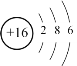 ,⑤为Si,其氧化物为SiO2,SiO2是光导纤维成分,即SiO2的用途可以制作光导纤维;
,⑤为Si,其氧化物为SiO2,SiO2是光导纤维成分,即SiO2的用途可以制作光导纤维;
(2)同周期从左向右非金属性增强,非金属性越强,其氢化物的稳定性越强,因此有H2S的稳定性强于SiH4;
(3)两性氢氧化物是Al(OH)3,即能形成两性氢氧化物的元素是Al;③的氢氧化物是NaOH,铝与NaOH反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑。


 星级口算天天练系列答案
星级口算天天练系列答案科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,它们之间有如下反应关系。

(1)若A是一种黑色单质,B是一种常见的难挥发性酸,C、D都是气体,试写出此反应的化学方程式_________________________________。
(2)若A是一种紫红色单质,B是一种常见的挥发性酸,反应时生成的C是无色气体,反应的离子方程式是________________________,B在反应中表现出的性质是_______、______。
(3)若实验室中利用A和B的反应制备气体C,C是一种无色、刺激性气味、密度比空气小的气体,试写出此反应的化学方程式________;实验室检验C的方法___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在四支试管中发生反应:CaCO3+2HCl=CaCl2+CO2↑+H2O,生成气体的速率最大的是( )
试管 | 温度/℃ | 等质量的CaCO3的形状 | 盐酸浓度/mol.L-1 |
A | 20 | 块状 | 0.5 |
B | 20 | 块状 | 1.0 |
C | 40 | 块状 | 1.0 |
D | 40 | 粉末 | 1.0 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,不正确的是( )
A. 有机化合物中每个碳原子最多形成4个共价键
B. 乙烯能使酸性高锰酸钾溶液和溴水褪色,但二者反应原理不相同
C. 在浓硫酸存在下,苯与浓硝酸共热生成硝基苯的反应属于取代反应
D. 乙烯和苯均能发生氧化反应,说明乙烯和苯分子中均有碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知难溶于水的盐在水中存在溶解平衡:
![]()
在一定温度下,水溶液中Ag+的物质的量浓度和Cl-的物质的量浓度的乘积为一常数,可用 KSP表示:KSP = c(Ag+)·c(Cl-)=1.8·10-10 。
若把足量AgCl分别放入① 100 mL蒸馏水,② 100 mL 0.1 mol / L NaCl溶液,③ 100 mL 0.1 mol / L AlCl3溶液,④ 100 mL 0.1 mol / L MgCl2溶液中,搅拌后,在相同温度下Ag+浓度由大到小的顺序(用序号回答)是 ______>______>______>______。在0.1 mol / L AlCl3溶液中,Ag+的物质的量浓度最多为_________mol / L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于碳、硅的说法正确的是( )
A.碳、硅的最外层均有4个电子,易得电子表现较强氧化性
B.硅是构成岩石的基本元素,地壳中含量处于第二位
C.硅在自然界中既有游离态又有化合态
D.碳的氧化物和硅的氧化物在常温常压下均为气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。

主要实验步骤如下:①按图组装仪器,并检验装置的气密性;
②将a g试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液;
③称量盛有碱石灰的U型管的质量,得到bg;
④从分液漏斗滴入6mol·L-1的硫酸,直到不再产生气体时为止;
⑤从导管A处缓缓鼓入一定量的空气;
⑥再次称量盛有碱石灰的U型管的质量,得到c g;
⑦重复步骤⑤和⑥的操作,直到U型管的质量基本不变,为d g。
请回答下列问题:
(1)用托盘天平称量药品时,如果天平的指针向左偏转,说明______。
(2)图中装置中干燥管B的作用是_____。
(3)如果将分液漏斗中的硫酸换成浓度相同的足量盐酸,测试的结果____(填偏高、偏低或不变)。
(4)步骤⑤的目的是________。
(5)试样中纯碱的质量分数的计算式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种酯,分子式是C14H12O2,A可以由醇B跟羧酸C发生酯化反应得到,A不能使溴的CCl4溶液褪色,氧化B可以得到C。
(1)写出A、B、C的结构简式:A、______,B、________,C、____________。
(2)写出B的两种同分异构体的结构简式,它们都可以跟NaOH反应________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com