
【题目】下列叙述正确的是
A.发生化学反应时失去电子越多的金属原子,还原能力越强
B.某元素从化合态变成游离态,该元素一定被还原
C.由同种分子构成的物质一定是纯净物
D.电离时能生成H+的化合物一定是酸
 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:
【题目】某溶液中含有NH![]() 、SO
、SO![]() 、SiO
、SiO![]() 、Br-、CO
、Br-、CO![]() 、Na+,向该溶液中通入过量的Cl2,下列判断正确的是( )
、Na+,向该溶液中通入过量的Cl2,下列判断正确的是( )
①反应前后,溶液中离子浓度基本保持不变的有NH![]() 、Na+;②有胶状物质生成;③有气体产生;④溶液颜色发生变化; ⑤共发生了2个氧化还原反应。
、Na+;②有胶状物质生成;③有气体产生;④溶液颜色发生变化; ⑤共发生了2个氧化还原反应。
A.①②③④ B.②③④
C.①③⑤ D.②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验误差分析正确的是
A. 用润湿的pH试纸测稀碱溶液的pH,测定值偏小
B. 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
C. 滴定前滴定管内无气泡,终点读数时有气泡,读取滴定溶液体积偏小
D. 测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度差偏小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分,有关说法中正确的是
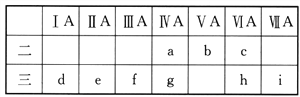
① a、b、e、f四种元素的原子半径:e>f>b>a
② h、i两种元素阴离子的还原性:h>i
③ a、g两种元素的氢化物的稳定性:a>g
④d、e、f三种元素的最高价氧化物对应的水化物碱性依次增强
⑤九种元素中d元素的单质还原性最强
A. ①③④ B. ②③⑤ C. ②④⑤ D. ①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各原子或离子的电子排列式错误的是
A. Na+1s22s22p6 B. F-1s22s22p6
C. N3+ 1s22s22p6 D. O2-1s22s22p6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关萃取操作的说法中,不正确的是( )
A.实验使用的主要仪器是分液漏斗
B.溶质溶于萃取剂中所得的溶液不一定有颜色
C.溶质在萃取剂中的溶解度比在原溶剂中的溶解度大
D.CCl4、苯、汽油、酒精均可萃取碘水中的碘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请参考题中图表,已知E1=134 kJ·mol-1、E2=368 kJ·mol-1,根据要求回答问题:
(1)图Ⅰ是1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是__________(填“增大”、“减小”或“不变”,下同),ΔH的变化是__________。请写出NO2和CO反应的热化学方程式___________________。

(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应的热化学方程式如下:
①CH3OH(g)+H2O(g)==CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1
②CH3OH(g)+![]() O2(g)==CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)==CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
且H2O(g)==H2O(l) ΔH=-44 kJ·mol-1,则甲醇蒸汽燃烧为液态水的热化学方程式为_______________。
(3)如表所示是部分化学键的键能参数:
化学键 | P—P | P—O | O===O | P===O |
键能/kJ·mol-1 | a | b | c | x |

已知白磷的燃烧热为d kJ·mol-1,白磷及其完全燃烧的产物的结构如图Ⅱ所示,则表中x=__________ kJ·mol-1(用含a、b、c、d的代表数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质相互混合后,能发生离子反应的是( )
A.碳和氧化铜混合高温加热
B.硫酸钾溶液和氯化镁溶液
C.硫酸钠溶液和硝酸铁溶液
D.氢氧化钠溶液和硝酸铁溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com