
【题目】分别用浓度均为![]() 的
的![]() 和NaOH溶液,滴定
和NaOH溶液,滴定![]() 溶液,随滴定溶液体积的增大,溶液的导电能力变化曲线如图所示,下列说法中正确的是
溶液,随滴定溶液体积的增大,溶液的导电能力变化曲线如图所示,下列说法中正确的是![]()
![]()
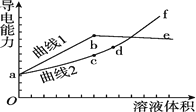
A.曲线2代表滴加![]() 溶液的变化曲线
溶液的变化曲线
B.b和d点对应的溶液均显碱性
C.b点溶液中![]()
D.![]() 段导电能力升高的原因是发生了反应
段导电能力升高的原因是发生了反应![]()
科目:高中化学 来源: 题型:
【题目】在不同温度下,向 2 L密闭容器中加入1 mol NO(g)和1 mol活性炭(C),发生反应:2NO(g)+C(s) ![]() N2(g)+CO2(g) ΔH=-213.5 kJ·mol-1,达到平衡时的数据如下。
N2(g)+CO2(g) ΔH=-213.5 kJ·mol-1,达到平衡时的数据如下。
温度/℃ | n(C)/mol | n(CO2)/mol |
t1 | 0.70 | |
t2 | 0.25 |
下列说法不正确的是( )
A.上述信息可推知:t1<t2
B.t1℃ 时,该反应的平衡常数K=![]()
C.t2℃ 时,若反应达平衡后再缩小容器的容积,c(N2)∶c(NO)不变
D.t1℃ 时,若开始时反应物的用量均减小一半,平衡后NO的转化率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨基锂(LiNH2)是一种白色有光泽的结晶或粉末,熔点是390 ℃,沸点是430 ℃,溶于冷水,遇热水则强烈水解。在380~400 ℃时锂与氨气直接反应可制得LiNH2,下面是实验室制备LiNH2时可能用到的装置图,回答下列问题。
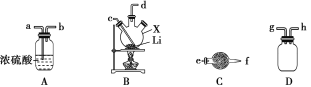
(1)仅从试剂性质角度分析,下列各组试剂不宜用于实验室制备NH3的是__________(填字母)。
A. 浓氨水、CaO B. NH4Cl固体、Ca(OH)2固体
C. 浓氨水 D. NH4NO3固体、NaOH固体
(2)用(1)中合适的试剂制取的NH3按气流方向自左向右,则图中装置的连接顺序为__________(填接口处字母),装置A的作用是__________。
(3)装置C中仪器的名称是___________,盛装的试剂是___________。实验开始后,向X中通入NH3与加热仪器X的先后顺序为___________。
(4)实验室还可用浓氨水与固体NaOH混合制备氨气,但多次实验表明,此方法收集到的NH3量总是比理论值低许多,其最可能的原因是_________。
(5)氨基锂能与热水反应生成LiOH与一种气体,请推测该气体的成分并用实验验证你的结论:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工艺的一个重要工序是铜洗,其目的是用铜液![]() 醋酸二氨合铜
醋酸二氨合铜![]() Ⅰ
Ⅰ![]() ,氨水
,氨水![]() 吸收在生产过程中产生的CO和
吸收在生产过程中产生的CO和![]() 等气体,铜液吸收CO的反应是放热反应,其反应方程式为:
等气体,铜液吸收CO的反应是放热反应,其反应方程式为:![]() ; 完成下列填空:
; 完成下列填空:
![]() 如果要提高上述反应的反应速率,可以采取的措施是 ______
如果要提高上述反应的反应速率,可以采取的措施是 ______ ![]() 选填编号
选填编号![]()
![]() 减压
减压 ![]() 增加
增加![]() 的浓度
的浓度 ![]() 升温
升温 ![]() 及时移走产物
及时移走产物
![]() 铜液中的氨可吸收二氧化碳,写出该反应的化学方程式: ______
铜液中的氨可吸收二氧化碳,写出该反应的化学方程式: ______
![]() 简述铜液吸收CO及铜液再生的操作步骤
简述铜液吸收CO及铜液再生的操作步骤![]() 注明吸收和再生的条件
注明吸收和再生的条件![]() .______
.______
![]() 铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为 ______ 通过比较 ______ 可判断氮、磷两种元素的非金属性强弱.
铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为 ______ 通过比较 ______ 可判断氮、磷两种元素的非金属性强弱.
![]() 已知
已知![]() 与
与![]() 分子结构相似,
分子结构相似,![]() 的电子式是 ______
的电子式是 ______ ![]() 熔点高于
熔点高于![]() ,其原因是 ______
,其原因是 ______
![]() 提取的
提取的![]() 中含少量
中含少量![]() 、
、![]() 将产品溶解,加入
将产品溶解,加入![]() ,加热至沸,再加入
,加热至沸,再加入![]() 溶液,过滤,蒸发结晶,得到工业氯化铵.加热至沸的目的是 ______
溶液,过滤,蒸发结晶,得到工业氯化铵.加热至沸的目的是 ______ ![]() 滤渣的主要成分是 ______ 、 ______ .
滤渣的主要成分是 ______ 、 ______ .
![]() 称取
称取![]() 小苏打样品
小苏打样品![]() 含少量
含少量![]() ,配置成250mL溶液,取
,配置成250mL溶液,取![]() 用
用![]() 盐酸滴定,消耗盐酸
盐酸滴定,消耗盐酸![]() 实验中所需的定量仪器出滴定管外,还有 ______
实验中所需的定量仪器出滴定管外,还有 ______ ![]() 选甲基橙而不选酚酞作为指示剂的原因是 ______
选甲基橙而不选酚酞作为指示剂的原因是 ______ ![]() 样品中
样品中![]() 质量分数为 ______
质量分数为 ______ ![]() 保留3位小数
保留3位小数![]()
![]() 将一定量小苏打样品
将一定量小苏打样品![]() 含少量
含少量![]() 溶于足量盐酸,蒸干后称量固体质量,也可测量定小苏打的含量.若蒸发过程中有少量液体溅出,则测定结果 ______
溶于足量盐酸,蒸干后称量固体质量,也可测量定小苏打的含量.若蒸发过程中有少量液体溅出,则测定结果 ______ ![]() 选填“偏高”、“偏低”或“不受影响”
选填“偏高”、“偏低”或“不受影响”![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于反应热的叙述正确的是( )
A.当ΔH<0时,表示该反应为吸热反应
B.由C(s)+![]() O2(g)=CO(g)的反应热为110.5kJ·mol-1,可知碳的燃烧热为110.5kJ·mol-1
O2(g)=CO(g)的反应热为110.5kJ·mol-1,可知碳的燃烧热为110.5kJ·mol-1
C.反应热的大小与反应物所具有的能量和生成物所具有的能量无关
D.1molNaOH分别和1molCH3COOH、1molHNO3反应放出的热量:CH3COOH<HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前,科学界拟合成一种“双重结构”的球形分子,即把足球烯C60的分子容纳在Si60分子中,外面的硅原子与里面的碳原子以共价键结合,下列叙述错误的是( )
A.该晶体为原子晶体B.该物质的熔沸点较低
C.该物质是新化合物D.该物质的相对分子量质量为2400
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2 L恒容密闭容器中投入一定量的A、B,发生反应:3A(g)+bB(g)![]() cC(g)+2D(s),12 s时生成C的物质的量为0.8 mol(反应进程如图所示)。下列说法中正确的是
cC(g)+2D(s),12 s时生成C的物质的量为0.8 mol(反应进程如图所示)。下列说法中正确的是

A.图中两曲线相交时,A的消耗速率等于A的生成速率
B.0-2 s,D的平均反应速率为0.1 mol·L-1·s-1
C.化学计量系数之比b:c=1:4
D.12 s时,A的转化率为75%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机玻璃的单体甲基丙烯酸甲酯(MMA) 的合成原理如下:
 (MMA)
(MMA)
下列说法正确的是
A. 若反应①的原子利用率为100%,则物质X为CO2
B. 可用分液漏斗分离MMA和甲醇
C. ![]() 、
、![]() 均可发生加成反应、氧化反应、取代反应
均可发生加成反应、氧化反应、取代反应
D. MMA与H2反应生成Y,能与NaHCO3溶液反应的Y的同分异构体有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期主族元素原子半径与原子序数的关系图。下列说法正确的是( )
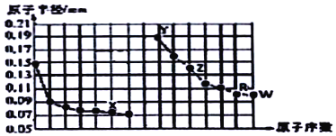
A.X所在主族中,X的简单氢化物分子间存在氢键,所以其氢化物稳定性最强
B.R简单氢化物的酸性弱于W简单氢化物,故元素非金属性R小于W
C.在同周期中,W的含氧酸酸性最强
D.Y的氢化物可以与水反应,产生一种单质气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com