
【题目】分子式为C10H12O2的有机物,满足以下条件:①苯环上只有两个取代基;②与FeCl3溶液发生显色反应;③能发生银镜反应.则满足这些条件的有机物共有( )
A.6种
B.9种
C.12种
D.15种
【答案】D
【解析】解:分子式为C10H12O2 , 能与FeCl3溶液发生显色反应、能发生银镜反应,说明其分子中含有酚羟基和醛基(醛基可以存在于甲酸某酯中),C10H12O2的不饱和度为 ![]() =5,苯环和羧基的不饱和度为5,则其它结构都是链状单键,除苯环碳外,其中一个取代基为﹣OH,直接连在苯环碳上,另一个取代基中还含有:10﹣6=4个C,此取代基的结构可以为﹣CH2CH2CH2OOCH,或者﹣CH(CH3)CH2OOCH,或者为﹣CH2CH(CH3)OOCH,或者为﹣C(CH3)2OOCH,或者﹣CH(CH2CH3)OOCH,各有邻、间、对3种,故共有15种,故满足这些条件的有机物共有15种,
=5,苯环和羧基的不饱和度为5,则其它结构都是链状单键,除苯环碳外,其中一个取代基为﹣OH,直接连在苯环碳上,另一个取代基中还含有:10﹣6=4个C,此取代基的结构可以为﹣CH2CH2CH2OOCH,或者﹣CH(CH3)CH2OOCH,或者为﹣CH2CH(CH3)OOCH,或者为﹣C(CH3)2OOCH,或者﹣CH(CH2CH3)OOCH,各有邻、间、对3种,故共有15种,故满足这些条件的有机物共有15种,
故选D.


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】某溶液既能溶解Al(OH)3 , 又能溶解H2SiO3 , 在该溶液中可以大量共存的离子组是( )
A.K+、Na+、HCO ![]() 、NO
、NO ![]()
B.Na+、SO ![]() 、Cl﹣、ClO﹣
、Cl﹣、ClO﹣
C.H+、Mg2+、SO ![]() 、NO
、NO ![]()
D.Ag+、K+、NO ![]() 、Na+
、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含大量Fe2+、Al3+、Fe3+、Na+、Cl﹣、SO ![]() 离子,其中加入足量的Na2O2固体后,再加入足量的盐酸溶解沉淀,最后溶液中的离子数目与反应前相比保持不变的是( )
离子,其中加入足量的Na2O2固体后,再加入足量的盐酸溶解沉淀,最后溶液中的离子数目与反应前相比保持不变的是( )
A.Na+、Fe2+
B.Al3+、SO ![]()
C.Fe3+、SO ![]()
D.Al3+、Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下,发生下列几种反应:①16H++10Z一+2XO ![]() =2X2++5Z2+8H2O ②2A2++B2=2A3++2B一 ③2B一+Z2=B2+2Z根据上述反应,判断下列结论中错误的是( )
=2X2++5Z2+8H2O ②2A2++B2=2A3++2B一 ③2B一+Z2=B2+2Z根据上述反应,判断下列结论中错误的是( )
A.氧化性强弱的顺序为:XO ![]() >Z2>B2>A3+
>Z2>B2>A3+
B.Z2在①、③反应中为还原剂
C.溶液中可发生:Z2+2A2+=2A3++2Z一
D.X2十是XO ![]() 的氧化产物
的氧化产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某品牌糖衣片补血剂,除去糖衣后显淡蓝绿色,主要成分是硫酸亚铁,不含其它铁的化合物.某研究性学习小组为测定该补血剂中硫酸亚铁的含量进行了以下探究: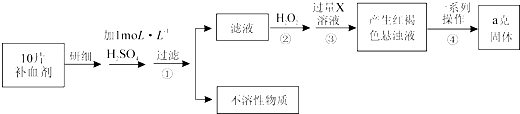
请回答下列问题:
(1)Ⅰ.①实验时用10molL﹣1的浓硫酸,配制100mL 1molL﹣1 H2SO4溶液,所需浓硫酸的体积为mL;②下列操作中,容量瓶所具备的功能有(填序号);
A.配制一定体积准确浓度的标准溶液 B.长期贮存溶液
C.常用来代替量筒量取一定体积的液体 D.用来溶解固体溶质
③在下列配制过程示意图中,有错误的是(填写序号);
④下列说法正确的
A.洗涤烧杯2~3次,并将洗涤液移入容量瓶以减少误差
B.某同学将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低
C.定容时仰视观察,所配溶液浓度会偏低
(2)Ⅱ.①步骤②加入过量H2O2后,溶液中主要存在的金属阳离子是;②从红褐色的悬浊液到最后的称量,其过程中所需的基本操作为:a. , b.洗涤,c.灼烧,d.冷却
③若称得固体的质量为ag,则每片补血剂中含硫酸亚铁的质量为g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】周期表前四周期的元素a、b、c、d、e,原子序数依次增大.A的核外电子总数与其电子层数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同主族,e的最外层只有1个电子,但次外层有18个电子.回答下列问题:
(1)b、c、d中第一电离能最大的是(填元素符号),e的价层电子轨道示意图为 .
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为;分子中既含有极性共价键,又含有非极性共价键的化合物是(填化学式,写两种).
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是;酸根呈三角锥结构的酸是 . (填化学式)
(4)c和e形成的一种离子化合物的晶体结构如图1,则e离子的电荷为 .
(5)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构,阳离子呈轴向狭长的八面体结构(如图2所示).该化合物中阴离子为 , 阳离子中存在的化学键类型有;该化合物加热时首先失去的组分是 , 判断理由是 . 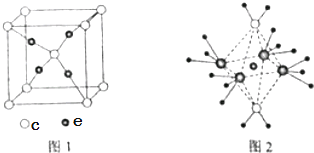
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2直接排放会对环境造成危害.SO2的尾气处理通常有以下几种方法: 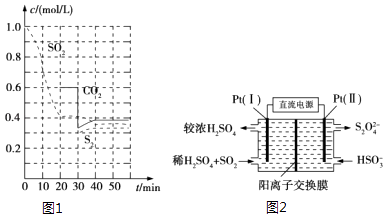
(1)活性炭还原法 反应原理:恒温恒容时2C(s)+2SO2(g)S2(g)+2CO2(g).
反应进行到不同时间测得各物质的浓度如图1:
①0~20min反应速率表示为v(SO2)=;
②30min时,改变某一条件平衡发生移动,则改变的条件最有可能是;
③能说明上述反应达到平衡状态的是 .
a.SO2 的消耗速率与CO2 的生成速率相同 b.混合气体的密度不变
c.S2的浓度不变 d.SO2 与S2的物质的量之比为2:1
(2)亚硫酸钠吸收法 ①Na2SO3溶液吸收SO2的离子方程式为;
②常温下,当吸收至NaHSO3时,吸收液中相关离子浓度关系一定正确的是(填序号).
a.c(Na+)+c(H+)>c(SO32﹣)+c(HSO3﹣)+c(OH﹣)
b.c(Na+)=c(SO32﹣)+c(HSO3﹣)+c(H2SO3)
c.c(Na+)>c(HSO3﹣)>c(H+)>c(SO32﹣)
d.水电离出c(H+)=1×10﹣8 mol/L
(3)电化学处理法 ①如图2所示,Pt(Ⅰ)电极的电极反应式为;
②当电路中转移0.02mol e﹣时(较浓H2SO4尚未排出),交换膜左侧溶液中约增加mol离子.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1905年德国化学家哈伯发明了合成氨的方法,他因此获得了1918年度诺贝尔化学奖.氨的合成不仅解决了地球上因粮食不足而导致的饥饿与死亡问题,在国防、能源、轻工业方面也有广泛用途.
Ⅰ.以氨为原料,合成尿素的反应原理为:
2NH3(g)+CO2(g)═CO(NH2)2(l)+H2O(g)△H=a kJ/mol.
为研究平衡时CO2的转化率与反应物投料比( ![]() )及温度的关系,研究小组在10L恒容密闭容器中进行模拟反应,并绘出如图(Ⅰ、Ⅱ曲线分别表示在不同投料比时,CO2的转化率与温度之间的关系).
)及温度的关系,研究小组在10L恒容密闭容器中进行模拟反应,并绘出如图(Ⅰ、Ⅱ曲线分别表示在不同投料比时,CO2的转化率与温度之间的关系).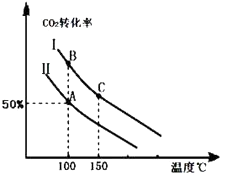
(1)a0 (填“>”或“<”),判断依据是 .
(2)①投料比:Ⅱ(填“>”或“<”).
②若n(CO2)起始=10mol,曲线Ⅱ的投料比为0.4,在100℃条件下发生反应,达平衡至A点,则A点与起始压强比为 .
③A点平衡常数与B点平衡常数间的关系:KAKB(填“>”或“<”或“=”).B点正反应速率与C点正反应速率间的关系为:v(B)v(C)(填“>”或“<”或“=”).
(3)若按曲线Ⅰ的投料比投料,在上述实验中压缩容器体积至5L,在图中画出反应达平衡时的二氧化碳的转化率与温度之间的关系曲线.
(4)为提高CO2转化率可以采取的措施是 .
a.使用催化剂 b.及时从体系中分离出部分CO(NH2)2c.将体系中的水蒸气液化分离
氨气可用于工业上生产硝酸,其尾气中的NO2可用氨水吸收生成硝酸铵,25℃时,将10molNH4NO3溶于水,溶液显酸性,向该溶液中滴加1L某浓度的氨水,溶液呈中性,则滴加氨水的过程中水的电离平衡将(填“正向”、“逆向”或“不”) 移动,此中性溶液中NH3H2O的物质的量为mol.(25℃时,NH3H2O的电离平衡常数Kb=2×10﹣5)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的数值,下列叙述正确的是( )
A.0.1molL﹣1的NaCl溶液中Cl﹣的数目为0.1NA
B.16g O3中所含的氧原子数为NA
C.22.4L H2中含有的氢原子数一定为2NA
D.1mol Cl2与过量的金属钠充分反应后,转移的电子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com