
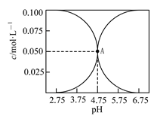
【题目】常温下,有c(CH3COOH)+c(CH3COO-)=0.1 mol·L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH的关系如下图所示。下列溶液中离子浓度关系正确的是
A.c(Na+)=0.1 mol·L-1的溶液中: c(H+)+c(CH3COOH)=c(OH-)
B.点A溶液中:c(Na+)>c(CH3COOH)
C.pH=3.5的溶液中:c(Na+)>c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-)
D.c(CH3COO-)=0.025 mol·L-1的溶液中:3c(Na+)<c(CH3COOH)
【答案】AD
【解析】
结合物质性质观察图可知,随着pH值的增大,浓度降低的是CH3COOH,浓度升高的是CH3COO-,在pH=4.75时,c(CH3COOH) =c(CH3COO-),可在此认识基础上对各选项作出判断。
A. 根据电荷守恒有:c(H+)+c(Na+)=c(OH-)+c(CH3COO-),根据物料守恒有:c(CH3COO-)+c(CH3COOH)=c(Na+),将两等式相加得: c(H+)+c(CH3COOH)=c(OH-),A选项正确;
B. 根据电荷守恒有:c(H+)+c(Na+)=c(OH-)+c(CH3COO-),点A溶液pH=4.75,显酸性,c(H+)>c(OH-),所以,c(Na+)<c(CH3COOH),B选项错误;
C. pH=3.5时,溶液显酸性,c(H+)>c(OH-),所以,c(Na+)<c(CH3COOH),C选项错误;
D. 根据电荷守恒有:c(H+)+c(Na+)=c(OH-)+c(CH3COO-),c(CH3COO-)=0.025 mol·L-1的溶液显酸性,c(H+)>c(OH-),所以, c(Na+)=c(OH-)-c(H+)+c(CH3COO-)<c(CH3COO-)=![]() c(CH3COOH),即,3c(Na+)<c(CH3COOH),D选项正确;
c(CH3COOH),即,3c(Na+)<c(CH3COOH),D选项正确;
答案选AD。


科目:高中化学 来源: 题型:
【题目】化合物H的分子中含有醛基和酯基。H可以用C和F在一定条件下合成(如图):
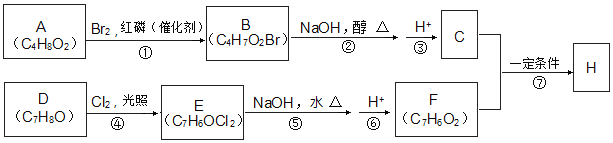
已知以下信息:
①A的核磁共振氢谱中有三组峰;且能与饱和碳酸氢钠溶液反应放出CO2。
②RCH2COOH 。
。
③化合物D苯环上的一氯代物只有两种。
④通常同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
(1)A的名称为___。
(2)D的官能团名称为___。
(3)反应②的化学方程式为__,⑦的反应类型为___。
(4)F的结构简式为__。
(5)H在一定条件下反应生成高聚物的化学方程式为___。
(6)F的同系物G比F相对分子质量大14,G的同分异构体中能同时满足如下条件:
①苯环上只有两个取代基;②不能使FeCl3溶液显色,共有__种(不考虑立体异构)。其中能与碳酸氢钠溶液反应且核磁共振氢谱为4组峰,且峰面积比为3:2:2:1,写出G的这种同分异构体的结构简式__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是原子序数依次增大的前四周期元素。已知A元素基态原子的核外电子分占四个原子轨道;B元素基态原子的成对电子数是未成对电子数的6倍;C元素是同周期元素中电负性最大的元素;D元素基态原子的L层与M层的电子数相等,且与s能级的电子总数相等;E元素可与C元素形成2种常见化合物,其中一种为棕黄色,另一种为浅绿色。
请回答下列问题:
(1)E元素基态原子的价层电子排布式为________,属于________区的元素。
(2)A、B两元素的氧化物的晶体类型分别为________、________;写出B元素的最高价氧化物与HF溶液反应的化学方程式:_____________________________。
(3)元素A的一种氢化物是重要的化工原料,常把它的产量作为衡量石油化工发展水平的标志,该分子中σ键和π键的数目分别为________和________。
(4)原子总数和价电子总数都相同的分子、离子或基团属于等电子体,由A~E中的元素形成的微粒中,与SO42-互为等电子体的分子是________(填分子式,任写一种),SO42-中的键角为________。
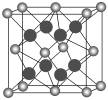
(5)D元素与最活泼的非金属元素形成的化合物的晶胞结构如图所示,其中“![]() ”代表的微粒是________(用元素符号或离子符号表示),该离子化合物晶体的密度为a g/cm3,则晶胞的体积是________(写出表达式即可)。
”代表的微粒是________(用元素符号或离子符号表示),该离子化合物晶体的密度为a g/cm3,则晶胞的体积是________(写出表达式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对分别盛有不同无色溶液的①②③④四支试管进行如下操作。现象和结论对应正确的是( )
选项 | 操作 | 现象 | 结论 |
A | 向①中滴加 | 试纸变蓝 | 原溶液中有 |
B | 向②中滴入 | 有白色沉淀生成 | 原溶液中有 |
C | 向③中先滴加 | 生成白色沉淀 | 原溶液中有 |
D | 向④中滴加氯水和 | 下层溶液呈橙色 | 原溶液中有 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取Cu、Cu2O和CuO固体混合物,将其分成两等份,一份用足量的氢气还原,反应后固体质量减少6.40g,另一份加入1000mL稀硝酸,固体恰好完全溶解,收集到标准状况下NO气体4.48L,所用硝酸的物质的量浓度为
A. 3.2mol/L B. 1.6mol/L C. 0.9mol/L D. 无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加碘食盐中含碘酸钾(KIO3),化学兴趣小组对加碘食盐展开研究性学习。
(1)加碘食盐中KIO3的制备可以采用以下两种方法:
方法一:碘单质与KClO3溶液反应生成KIO3和Cl2;
方法二:碘单质与H2O2在催化剂作用下反应生成HIO3,再与K2CO3作用生成KIO3;两种方法制等质量的KIO3,理论上消耗KClO3和H2O2的物质的量之比为 _______ 。
(2)兴趣小组测定食用精制盐中碘元素含量的实验步骤为:
步骤1:准确称取25.00 g食盐,加适量蒸馏水使其完全溶解,配成100.00 mL溶液;
步骤2:取所配溶液25.00 mL于锥形瓶中,用稀硫酸酸化该溶液,加入足量KI溶液,使之充分反应;
步骤3:滴入2~3滴淀粉溶液作指示剂,用1.0×10-3 mol·L-1的Na2S2O3标准溶液滴定至终点,恰好完全反应时消耗12.00 mL标准溶液。
已知步骤3中所发生反应的离子方程式为I2+2S2O32-=2I-+S4O62-。
①步骤3中滴定终点的现象是 _______ 。
②下列情况会使测定结果偏大的是 _______ 。
A 装Na2S2O3标准溶液的滴定管水洗后未用Na2S2O3标准溶液润洗
B 装Na2S2O3标准溶液的滴定管滴定前有气泡,滴定终了无气泡
C 滴定时未充分振荡,溶液局部变色就终止
D 若其他读数正确,滴定结束读数时俯视
③计算该精制盐的碘元素含量(mg·kg-1),写出计算过程_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某些元素在周期表中的位置如图所示:
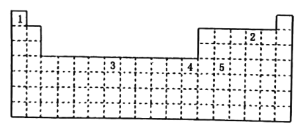
下列说法正确的是( )
A.表中五种元素位于5个不同的区
B.元素4的基态原子的价电子排布式为3d104s2与它具有相同最外层电子数的元素只可能处于ds区
C.元素1、2、3的基态原子中,未成对电子数之比为1:3:5
D.元素5的原子结构示意图为: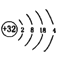
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种重要的化工原料,在化工领域有广泛应用。
(1)甲醇燃料电池由于结构简单、能量转化率高、对环境天污染,可作为常规能源的替代品而越来越受到关注。其工作原理如如图所示:
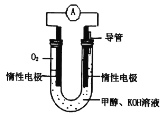
①该电池正极的电极反应为___,放电过程中负极区域溶液的pH值___(填“变大”或“变小”或“不变”)。
②该电池总反应的化学方程式为___。
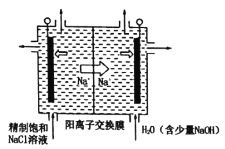
(2)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高校、光谱、安全的杀菌消毒剂。目前已开发出用电解法制取ClO2的新工艺。
①如图中用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。则阳极产生ClO2的电极反应式为____。
②电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为___mol。
(3)英国《自然》杂志近期报道了一种新型铝离子电池,以金属铝和石墨为电极,用A1Cl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示。
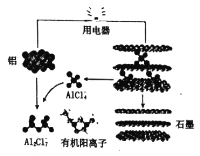
①电池放电时负极的电极反应式为___。
②充电时有机阳离子向___电极移动(填“铝”或“石墨”)。
③电池充电时,电路中每转移0.15mol电子,理论上生成___g铝。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳捕获技术用于去除气流中的二氧化碳或者分离出二氧化碳作为气体产物,其中CO2催化合成甲酸是原子利用率高的反应,且生成的甲酸是重要化工原料。下列说法不正确的是( )
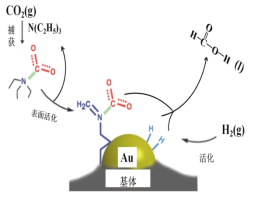
A. 二氧化碳的电子式: ![]()
B. 在捕获过程,二氧化碳分子中的共价键完全断裂
C. N(C2H5)3能够协助二氧化碳到达催化剂表面
D. CO2催化加氢合成甲酸的总反应式:H2+CO2=HCOOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com