
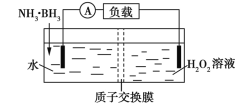
【题目】氨硼烷(NH3·BH3)电池可在常温下工作,装置如图所示。未加入氨硼烷之前,两极室质量相等,电池反应为NH3·BH3+3H2O2═NH4BO2+4H2O。已知两极室中电解质足量,下列说法正确的是
A. 正极的电极反应式为2H++2![]() ═H2↑
═H2↑
B. 电池工作时,H+通过质子交换膜向负极移动
C. 电池工作时,正、负极分别放出H2和NH3
D. 工作一段时间后,若左右两极室质量差为1.9 g,则电路中转移0.6 mol电子
【答案】D
【解析】
本题考察新型原电池工作原理,根据电池反应可知,正、负极的电极反应分别为
3H2O2+6H++6e-=6H2O、NH3·BH3+2H2O-6e-=NH4BO2+6H+。
A. 正极的电极反应式为:3H2O2+6H++6e-=6H2O,没有气体生成,A项错误;
B.原电池工作时,氢离子作为阳离子向正极移动,B项错误;
C.两电极反应分别为:3H2O2+6H++6e-=6H2O、NH3·BH3+2H2O-6e-=NH4BO2+6H+。
两极均没有气体生成,C项错误;
D.从电极反应式来看,如有6mol电子转移,则左极室质量增加31g-6g=25g,右极室质量增加6g,两极室质量之差为19g,所以当左右两室质量差为1.9g时,电路中转移0.6mol电子,D项正确;
所以答案选择D项。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次递增,其中Y与Z同主族。X与Y、Z与W均可形成如图所示的分子结构,且Z与W形成的分子中所有原子最外层均满足8电子稳定结构。下列说法中正确的是

A.原子半径:W > Z > Y > X
B.气态氢化物热稳定性:Y > Z > W
C.元素Z和W均存在两种以上的含氧酸
D.元素Z和W在自然界中均只能以化合态存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下将pH=8的NaOH溶液稀释1000倍,稀释后溶液中c(Na+)与c(OH-)之比接近
A. 1:1 B. 1:102 C. 102:1 D. 1:103
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中科院董绍俊课题组将二氧化锰和生物质置于一个由滤纸制成的折纸通道内形成电池(如下图所示),该电池可将可乐(pH=2.5)中的葡萄糖作为燃料获得能量。下列说法正确的是

A. a极为正极
B. 随着反应不断进行,负极区的pH不断增大
C. 消耗0.01mol葡萄糖,电路中转移0.02mol电子
D. b极的电极反应式为:MnO2+2H2O+2e-=Mn2++4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下面的方案检验试液中的![]() ,其中方案设计严密的是( )
,其中方案设计严密的是( )
A. 试液![]() 无沉淀
无沉淀![]() 白色沉淀
白色沉淀
B. 试液![]() 无沉淀
无沉淀![]() 白色沉淀
白色沉淀
C. 试液![]() 白色沉淀
白色沉淀![]() 白色沉淀
白色沉淀
D.试液![]() 无沉淀
无沉淀![]() 白色沉淀
白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家一直致力于“人工固氮”的研究,现已有多种方法。
(方法一)1918年,德国化学家哈伯因发明工业合成氨(N2(g)+3H2(g)![]() 2NH3(g) H<0)的方法而荣获诺贝尔化学奖。
2NH3(g) H<0)的方法而荣获诺贝尔化学奖。
(1)若将1molN2和3molH2放入1L的密闭容器中,5min后N2的浓度为0.8mol/L,这段时间内用N2的浓度变化表示的反应速率为_____mol/(L·min)。
(2)在一定温度下的定容密闭容器中发生上述反应,下列叙述能说明反应已经达到平衡状态的是____。
a. v(N2)正=3v(H2)逆
b. 容器中气体的密度不随时间而变化
c. 容器中气体的分子总数不随时间而变化
d. 容器中气体的平均相对分子质量不随时间而变化
(3)合成氨反应的生产条件选择中,能用勒夏特列原理解释的是________。
①使用催化剂 ②高温 ③高压 ④及时将氨气液化从体系中分离出来
A. ①③ B. ②③ C. ③④ D. ②④
(方法二)1998年,两位希腊化学家提出了电解合成氨的新思路:
(4)采用高质子导电性的SCY陶瓷(能传递H+)为介质,实现了高温(570℃)常压下高转化率的电解法合成氨,转化率可达到78%,装置如下图:
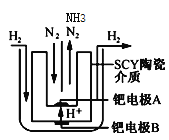
钯电极A是电解池的___极(填“阳”或“阴”),阳极反应式为________。
(方法三)最新的“人工固氮”研究报道:在常温、常压、光照条件下,N2在催化剂表面与水发生反应,直接生成氨气和氧气:
已知:N2(g)+3H2(g) ![]() 2NH3(g) △H=-92 kJ/mol
2NH3(g) △H=-92 kJ/mol
2H2(g)+O2(g)=2H2O(1) △H=-571.6 kJ/mol
(5)写出上述固氮反应的热化学方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应叙述相符合的是( )
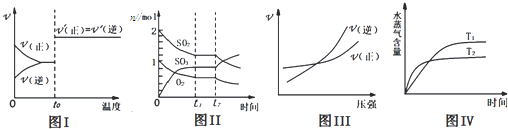
A.图I:反应H2+I22HI达平衡后,升高温度时反应速率随时间的变化
B.图Ⅱ:反应2SO2+O22SO3达平衡后,缩小容器体积时各成分的物质的量变化
C.图III:反应N2+3H22NH3在温度一定的情况下,反应速率与压强的关系
D.图IV:反应CO2(g)+H2(g)CO(g)+H2O(g)△H>0,水蒸气含量随时间的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为消除目前燃料燃烧时产生的环境污染,同时缓解能源危机,有关专家提出了利用太阳能制取氢能的构想。下列说法正确的是
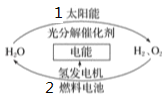
A. 过程1是放热反应
B. 过程2可将化学能转化为电能
C. 氢能源可从自然界直接获取,是一次能源
D. 氢气不易贮存和运输,无开发利用价值
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】α-溴代羰基化合物合成大位阻醚的有效方法可用于药物化学和化学生物学领域。用此法合成化合物J的路线如下:

已知:
回答下列问题:
(1)F中含有的含氧官能团的名称是______,用系统命名法命名A的名称是______。
(2)B→ C所需试剂和反应条件为___________。
(3)由C生成D的化学反应方程式是__________。
(4)写出G的结构简式_________,写出检验某溶液中存在G的一种化学方法________。
(5)F+H→J的反应类型是_______。F与C在CuBr和磷配体催化作用下也可合成大位阻醚,写出其中一种有机产物的结构简式:_______。
(6)化合物X是E的同分异构体,分子中不含羧基,既能发生水解反应,又能与金属钠反应。符合上述条件的X的同分异构体有_______种(不考虑立体异构),其中能发生银镜反应,核磁共振氢谱有3组峰,峰面积之比为1:1:6的结构简式为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com