
【题目】相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:N2(g) + 3H2(g) ![]() 2NH3(g)△H=-92.4 kJ/mol。实验测得起始、平衡时的有关数据如下表:
2NH3(g)△H=-92.4 kJ/mol。实验测得起始、平衡时的有关数据如下表:
容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
N2 | H2 | NH3 | ||
① | 1 | 3 | 0 | 放出热量a kJ |
② | 2 | 3 | 0 | 放出热量b kJ |
③ | 2 | 6 | 0 | 放出热量c kJ |
下列叙述正确的是
A. 放出热量关系:a < b <92.4
B. 三个容器内反应的平衡常数:③>①>②
C. 达平衡时氨气的体积分数:①>③
D. N2的转化率:②>①>③
科目:高中化学 来源: 题型:
【题目】你认为下列说法正确的是( )
A. 液态氟化氢中存在氢键,所以其分子比氯化氢更稳定
B. 氢键存在于分子之间,也存在于分子之内
C. 对于分子,其范德华力只随着相对分子质量的增大而增大
D. NH3极易溶于水而CH4难溶于水的原因只是NH3是极性分子,CH4是非极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ti、Fe、Cu、Ni为过渡金属元素,在工业生产中有重要的应用.
(1)①常温下Fe(CO)5呈液态,熔点为-20.5℃,沸点为103℃.据此可以判断其晶体为_________晶体,Fe(CO)5中铁的化合价为0,则该物质中含有的化学键类型有______(填字母).
A 离子键 B 极性共价键 C 非极性共价键 D 配位键
②NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中心离子的配位数为________,配体H2O中O原子的杂化方式为________.
③NiO、FeO的晶体结构类型均与氧化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO_______FeO(填“<”或“>”).
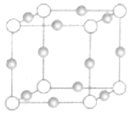
(2)Cu、N两元素形成某种化合物的晶胞结构如图(灰色球表示Cu原子),已知紧邻的白球与灰球之间的距离为acm,该晶胞的密度为________gcm-3.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Kevlar(凯夫拉),原名聚对苯二甲酰对苯二胺,具有超高的机械性能,是制作防弹衣的原材料。Kevlar 的结构片段如右图所示,则下列说法不正确的是( )
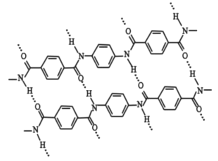
A.Kevlar 属于聚酰胺类合成高分子材料
B.图中虚线表示高分子链之间形成了类似肽链间的多重氢键,增强了材料的机械性能
C.Kevlar 可以发生完全水解,得到一种单体分子,该分子中既含有-COOH,又含有-NH2
D.Kevlar 高分子链的结构简式为 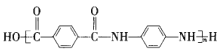
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向 0.01 mol·L-1 的醋酸溶液中滴入 pH=7 的醋酸铵溶液,溶液 pH 随滴入醋酸铵溶液体积变化的曲线示意图如图所示。下列分析正确的是
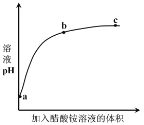
A.a点,pH = 2
B.b点,c(CH3COO-) > c(NH4+)
C.c点,pH可能大于7
D.ac段,pH的增大仅是因为醋酸电离平衡逆向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在实验报告中记录下列数据,其中正确的是
A. 用 100 mL 量筒量取 12.5 mL 盐酸
B. 称量 NaOH 固体时,将 NaOH 直接放在托盘上的纸上
C. 需用 220 mL, 1 mol·L-1 CuSO4 溶液,配制时需称 62.5g 的 CuSO4·5H2O 晶体
D. 配制稀硫酸时,先向烧杯中注入浓硫酸,再加水稀释
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将3.8 g CO和H2混合气体,在足量的氧气中燃烧,产物全部通过足量的Na2O2,则Na2O2增重
A. 2 g B. 3.8 g C. 5 g D. 无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行的实验,能达到相应实验目的的是()
A. 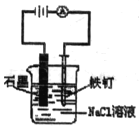 防止铁钉生锈
防止铁钉生锈
B. 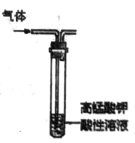 除去乙烷中混有的乙烯
除去乙烷中混有的乙烯
C. 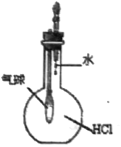 验证HCl气体在水中的溶解性
验证HCl气体在水中的溶解性
D. 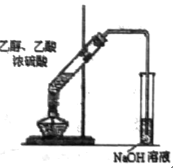 实验室制取乙酸乙酯
实验室制取乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄可用于酿酒。
(1)检验葡萄汁含葡萄糖的方法是:向其中加碱调至碱性,再加入新制备的Cu(OH)2,加热,其现象是_______________________________________。
(2)葡萄在酿酒过程中,葡萄糖转化为酒精的过程如下,补充完成下列化学方程式。
C6H12O6(葡萄糖)![]() 2________+2C2H5OH
2________+2C2H5OH
(3)葡萄酒密封储存过程中生成了有香味的酯,酯也可以通过化学实验来制备。实验室用下图所示装置制备乙酸乙酯:

①试管a中生成乙酸乙酯的化学方程式是________________________________。
②试管b中盛放的试剂是饱和_________________溶液。
⑧实验开始时,试管b中的导管不伸入液面下的原因是___________________。
④若分离出试管b中生成的乙酸乙酯,需要用到的仪器是____(填序号)。
a. 漏斗 b. 分液漏斗 c. 长颈漏斗
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com