
【题目】化学工业与人类的生产生活息息相关,回答下列问题:
已知反应: Fe(s)+CO2(g) ![]() FeO(s)+CO(g) △H =a kJmol-1,测得在不同温度下,平衡常数 K 值如下:
FeO(s)+CO(g) △H =a kJmol-1,测得在不同温度下,平衡常数 K 值如下:
温度/℃ | 500 | 700 | 900 |
K | 1.00 | 1.47 | 2.40 |
(1)写出 K 的表达式__________________。
(2)反应中的 a____________0(填“>”、“<”或“=”)。
(3)若 500℃时进行反应,CO2 起始浓度为 3molL-1,CO 的平衡浓度为______molL-1。
(4)700 ℃时反应达到平衡,要使该平衡向右移动且能增大 CO2(g)的转化率,其他条件不变时,可以采取的措施有________(填序号)。
A.升高温度到 900 ℃ B.通入 CO2
C.增加 Fe 的量 D.使用合适的催化剂
(5)700℃反应达到平衡,此时增大反应中 CO 的浓度,该平衡移动后达到新的平衡,其它条件不变时,CO 和 CO2 的体积比值__________(填“增大”、“减小”或 “不变”)。
【答案】 K=![]() > 1.5 A 不变
> 1.5 A 不变
【解析】(1)反应Fe(s)+CO2(g) ![]() FeO(s)+CO(g)的平衡常数 K =
FeO(s)+CO(g)的平衡常数 K =![]() ;(2)根据表中数据可知,升高温度,平衡常数增大,说明平衡向正反应方向移动,正反应为吸热反应,△H>0,故a>0;(3)若 500℃时进行反应,CO2 起始浓度为 3molL-1,CO 的平衡浓度为xmolL-1,则:
;(2)根据表中数据可知,升高温度,平衡常数增大,说明平衡向正反应方向移动,正反应为吸热反应,△H>0,故a>0;(3)若 500℃时进行反应,CO2 起始浓度为 3molL-1,CO 的平衡浓度为xmolL-1,则:
Fe(s)+CO2(g) ![]() FeO(s)+CO(g)
FeO(s)+CO(g)
起始浓度(mol/L) 3 0
改变浓度(mol/L) x x
平衡浓度(mol/L) 3-x x
K =![]() =
=![]() =1,解得x=1.5mol/L;(4)A、升高温度到900 ℃,该平衡向右移动且能增大CO2(g)的转化率,选项A正确;B、通入CO2平衡向右移动,但降低了CO2(g)的转化率,选项B不正确;C、铁是固体,增加 Fe 的量,浓度不变,平衡不移动,选项C不正确;D、催化剂不能改变平衡状态,选项D不正确,答案选A;(5)化学平衡常数只与温度有关,与浓度无关,700℃反应达到平衡,此时增大反应中 CO 的浓度,该平衡移动后达到新的平衡,其它条件不变时,CO 和 CO2 的体积比值等于平衡常数,温度不变,平衡常数不变,故CO 和 CO2 的体积比值不变。
=1,解得x=1.5mol/L;(4)A、升高温度到900 ℃,该平衡向右移动且能增大CO2(g)的转化率,选项A正确;B、通入CO2平衡向右移动,但降低了CO2(g)的转化率,选项B不正确;C、铁是固体,增加 Fe 的量,浓度不变,平衡不移动,选项C不正确;D、催化剂不能改变平衡状态,选项D不正确,答案选A;(5)化学平衡常数只与温度有关,与浓度无关,700℃反应达到平衡,此时增大反应中 CO 的浓度,该平衡移动后达到新的平衡,其它条件不变时,CO 和 CO2 的体积比值等于平衡常数,温度不变,平衡常数不变,故CO 和 CO2 的体积比值不变。


 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】用提供的试剂(溴水、浓硝酸 、碘水、新制氢氧化铜浊液)分别鉴别下列有机物,将所用试剂及产生的现象的序号填在横线上。
序号 | 待鉴别的物质 | 试剂 | 现象 |
① | 乙烯 | _____ | ____________ |
② | 葡萄糖 | _____ | ___________ |
③ | 淀粉 | _____ | ___________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学小组学生利用如图所列装置进行“铁与水反应”的实验,并进行了其他有关实验.(图中夹持及尾气处理装置均已略去) 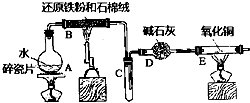
(1)装置B中发生反应的化学方程是
(2)装置E中的现象是
(3)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤.
①欲检验溶液中含有Fe3+ , 选用的试剂为 , 现象是 .
②该实验小组同学用上述试剂没有检测到Fe3+ , 用离子方程式解释滤液中不存在Fe3+可能的原因: .
③在此溶液中加入少量酸性高锰酸钾溶液,高锰酸钾褪色,溶液中反应的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空
(1)在Fe3O4+4CO ![]() 3Fe+4CO2的中,是还原剂,元素被还原,当有标状下的CO气体560ml完全反应时,生成Fe是克.
3Fe+4CO2的中,是还原剂,元素被还原,当有标状下的CO气体560ml完全反应时,生成Fe是克.
(2)下列物质能导电的是(用序号填空,下同)属于电解质的是 , 属于非电解质的是 .
①水银 ②烧碱 ③大理石 ④氯化钠晶体 ⑤盐酸
⑥氨气 ⑦蔗糖 ⑧氯气 ⑨液态氯化氢 ⑩硫酸溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是

A. 根据图①可判断该可逆反应正反应为吸热反应
B. 若②表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(s)的影响,则乙对应的压强大
3C(g)+D(s)的影响,则乙对应的压强大
C. 图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
D. 根据图④,若除去CuSO4溶被中的Fe3+,可向溶液中加入适量CuO,调节pH至4左右
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分是Al2O3 , 还有少量的Fe2O3、SiO2提取冶炼铝的原料氧化铝.工艺流程如图:(每步所加试剂均稍过量) 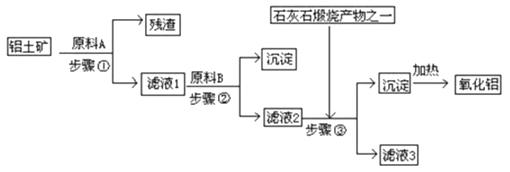
(1)步骤①中所得残渣的成分是(用化学式表示)、流程中分离固体和溶液的方 法是 , 所用到的玻璃仪器有烧杯、玻璃棒和 .
(2)步骤③中若加入过量的石灰石煅烧产物,则滤液3的成分是 , 该反应的 离子方程是: .
(3)如果省去步骤①,即溶解铝土矿是从加入原料B开始,后续操作不变,则会对氧化 铝的提取有什么影响 .
(4)实验室里常向AlCl3溶液中加入氨水来制取Al(OH)3 , 写出该反应的离子方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com