
【题目】实验室可用KMnO4和浓盐酸反应制取氯气:KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O(未配平)
(1)配平化学方程式,并用单线桥标出电子转移的方向和数目。________。
(2)将上述配平的化学方程式改写为离子方程式________。
(3)浓盐酸在反应中显示出来的性质是________。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(4)若产生0.5mol Cl2,则被氧化的HCl ____mol,转移的电子的数目约为____。
【答案】![]() 2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O ② 1 6.02×1023
2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O ② 1 6.02×1023
【解析】
(1)KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O中,Mn元素的化合价由+7降低为+2价,Cl元素的化合价由-1价升高到0,化合价升高数=化合价降低数=转移电子数=10,根据电子守恒可知,MnCl2的化学计量数为2,Cl2的化学计量数为5,再根据质量守恒定律可知,配平的化学反应为2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O,单线桥表示反应中电子转移的方向和数目为![]() ;
;
(2)在反应2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O中,改为离子反应时Cl2和H2O应保留化学式,其余物质均写成离子形式,则离子反应为2MnO4-+16H++10Cl-═Mn2++5Cl2↑+8H2O;
(3)由反应可知,盐酸参与反应生成KCl和MnCl2时表现其酸性,生成Cl2时表现其还原性答案为:②;
(4)Cl元素的化合价由-1价升高到0,产生0.5molCl2,则被氧化的HCl为0.5mol×2=1mol,转移的电子的物质的量为0.5mol×2×(1-0)=1mol,转移的电子的数目为约为6.02×1023。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案科目:高中化学 来源: 题型:
【题目】莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是

A.分子式为C7H6O5
B.分子中含有2种官能团
C.可发生加成和取代反应
D.在水溶液羧基和羟基均能电离出H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化工原料的结构简式如图所示,下列关于该有机物的说法正确的是( )
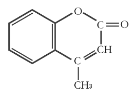
A.1 mol该物质最多能和5mol H2发生加成反应
B.能使酸性KMnO4溶液褪色,能发生加成反应和取代反应
C.该分子中所有原子都可能共平面
D.该物质的分子式为C10H10O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是()
A.![]() 中,氧化剂和还原剂的物质的量之比为1:4
中,氧化剂和还原剂的物质的量之比为1:4
B.![]() 中,氧化产物和还原产物的质量之比为1:1
中,氧化产物和还原产物的质量之比为1:1
C.![]() 中,发生氧化反应和发生还原反应的氮元素的质量之比为5:3
中,发生氧化反应和发生还原反应的氮元素的质量之比为5:3
D.![]() 中,被氧化和被还原的硫元素的物质的量之比为1:1
中,被氧化和被还原的硫元素的物质的量之比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在溶液中可发生以下反应:①![]() ②
②![]() ③
③![]() 由此判断下列说法正确的是()
由此判断下列说法正确的是()
A.铁元素在反应①中被还原,在③中被氧化
B.反应②中当有1molCl2被氧化时,有2molBr—被还原
C.氧化性强弱顺序为:![]()
D.还原性强弱顺序为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】α-鸢尾酮香料的分子结构如图,下列说法不正确的是

A. α-鸢尾酮可与某种酚互为同分异构体
B. 1 mol α-鸢尾酮最多可与3molH2加成
C. α-鸢尾酮能发生银镜反应
D. α-鸢尾酮经加氢→消去→加氢三步反应可转变为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废水中可能含有下列离子中的若干种:Fe3+、Al3+、Fe2+、Cu2+、Cl-、CO32-、NO3-、SO42-、SiO32-。现进行如下实验:
Ⅰ.取少量溶液,加入KSCN溶液,无明显变化。
Ⅱ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色。
Ⅲ.向Ⅱ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
Ⅳ.向Ⅱ中所得的溶液中加入过量浓氨水,仅有红褐色沉淀生成。过滤,在所得滤液中加入盐酸至酸性时,再加入氢氧化钠溶液,有蓝色沉淀生成。
请回答下列问题:
(1)该废水中一定含有的离子是_________________________。
(2)实验Ⅱ中加入少量盐酸生成无色气体的离子方程式是______________________。
(3)过滤除去Ⅳ中的蓝色沉淀,调整滤液的pH为10.7左右时,加入铝粉,反应产生氨气和氮气的体积比为1:4,其离子方程式为Al+NO3-+OH-→ AlO2-+NH3+N2+H2O(未配平)。还原产物是_________,若除去0.2 mol NO3-,要消耗铝________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液100mL,其中可能含Fe3+、Al3+、Na+、Mg2+、Cu2+、NH4+、K+、CO32-、SO42-等离子中的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如图所示。
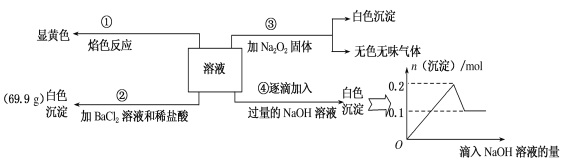
请回答下列问题:
(1)焰色反应是___(填“物理”或“化学”)变化;实验③中产生的无色无味气体是___(填化学式)。
(2)原溶液中一定存在的离子有___,一定不存在的离子有____。
(3)若溶液中K+物质的量为0.04mol,则c(Na+)=___mol/L。
(4)将一定量Fe2O3和Al2O3混合物溶于100mL稀硫酸中,向反应后的溶液中缓慢加入NaOH溶液,加入NaOH溶液的体积与生成沉淀的质量关系如图所示,试回答:
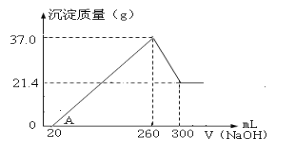
①混合物中含Fe2O3的质量为___g;
②所用硫酸溶液物质的量浓度为___mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物X、Y、A、B、C、D、E、F、G之间的转化关系如图所示。
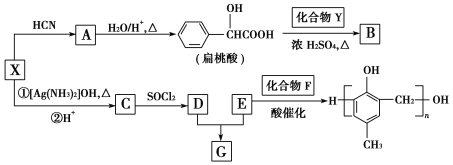
已知:①![]()
②![]() (R、R'代表烃基)
(R、R'代表烃基)
③X在催化剂作用下可与H2反应生成化合物Y;
④化合物F的核磁共振氢谱图中只有一个吸收峰。
请回答下列问题:
(1)X的含氧官能团的名称是________________________,X与HCN反应生成A的反应类型是_______________________。
(2)酯类化合物B的分子式是C15H14O3,其结构简式是__________________________。
(3)X发生银镜反应的化学方程式是:________________________。
(4)G在NaOH溶液中发生水解反应的化学方程式是_______________________。
(5)![]() 的同分异构体中:①能发生水解反应;②能发生银镜反应;③能与氯化铁溶液发生显色反应。满足上述条件的同分异构体共有________种(不考虑立体异构)。
的同分异构体中:①能发生水解反应;②能发生银镜反应;③能与氯化铁溶液发生显色反应。满足上述条件的同分异构体共有________种(不考虑立体异构)。
(6)写出以C2H5OH为原料合成乳酸(![]() )的路线(其他试剂任选)。________________________________________________________________________。
)的路线(其他试剂任选)。________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com