
【题目】在下列给定条件的溶液中,一定能大量共存的离子组是( )
A.使pH试纸显深蓝色的溶液:Ca2+、NH4+、HCO3-、Cl-
B.室温下,![]() =0.1mol/L的溶液:Na+、K+、SiO32-、NO3-
=0.1mol/L的溶液:Na+、K+、SiO32-、NO3-
C.含FeCl3的溶液:K+、Na+、SO42-、CO32-
D.能与金属铝反应放出氢气的溶液:Mg2+、Na+、SO42-、Cl-
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOCl)是有机合成中的重要试剂,工业上可用NO和Cl2合成。回答下列问题:
(1)已知:①2NO2(g)+NaCl(s)NaNO3(s)+NOCl(g) △H1
②4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g) △H2
③2NO(g)+Cl2(g) 2NOCl(g) △H3
则△H3=_____________(用含△H1、△H2的代数式表示)。
(2)一定温度下,向2L密闭容器中充入amol NOCl(g),发生反应2NOCl(g)2NO(g)+Cl2(g)。
①已知上述反应中正反应速率的表达式为v正=k·cn(NOCl)。300℃时,测得正反应速率与NOCl的浓度的关系如表所示:
c(NOCl)/(mol/L) | v正/(molL-1s-1) |
0.20 | 1.6×10-9 |
0.40 | 6.4×10-9 |
0.60 | 1.44×10-8 |
n=______;k=_____L·mol-1·s-1;当c(NOCl)=0.50 mol·L-1时,v正=_____mol·L-1·s-1。
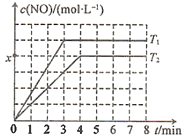
②测得NO的物质的量浓度与温度的关系如图所示(x<0.5a),T1________T2(填“>”“<”或“=”);T2温度下,该反应的平衡常数K=________mol·L-1(用含a、x的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高炉炼铁过程中发生的主要反应为:![]() Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)![]()
![]() Fe(s)+CO2(g)。已知该反应在不同温度下的平衡常数如下:
Fe(s)+CO2(g)。已知该反应在不同温度下的平衡常数如下:
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
请回答下列问题:
(1)该反应的平衡常数表达式K=________,该反应是_________反应(填“放热”或“吸热”)。
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe2O3、CO各4.0 mol,反应经过20min后达到平衡。求该时间范围内反应的平均反应速率v(CO)=__________、CO的平衡转化率=__________。
(3)欲提高(2)中CO的平衡转化率,可采取的措施是________
A.降低反应温度 B.增加Fe2O3的量 C.加入合适的催化剂 D.移出部分CO2 E.减小容器的容积
(4)在1L的密闭容器中,1150℃条件,下列达平衡状态的是__________。
A | B | C | D | |
n(Fe2O3) | 0.350 | 0.027 | 0.080 | 0.080 |
n(CO) | 0.010 | 0.010 | 0.010 | 0.050 |
n(Fe) | 0.100 | 0.064 | 0.080 | 0.080 |
n(CO2) | 0.035 | 0.088 | 0.037 | 0.050 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质能满足如图所示转化关系的是(图中箭头表示进一步转化)

a | b | c | d | |
① | Si | SiO2 | H2SiO3 | Na2SiO3 |
② | Al | AlCl3 | NaAlO2 | Al(OH)3 |
③ | Cu | CuO | Cu(OH)2 | CuSO4 |
④ | Fe2O3 | FeCl3 | FeCl2 | Fe |
A. ①② B. ②③ C. ③④ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在某200mL的稀硫酸和稀硝酸的混合溶液中逐量地加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。(设硝酸只被还原为NO气体,Fe的相对原子质量为56)。下列有关分析错误的是
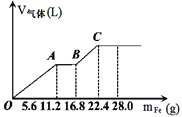
A.原混合酸中NO3-的物质的量为0.2mol
B.原混合酸中H2SO4物质的量浓度为2mol/L
C.OA段与BC段反应中电子转移的物质的量之比为2:1
D.取20mL原混合酸加水稀释至1L后溶液的pH=1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】没食子酸丙酯简称PG,是一种白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂。其结构简式如图所示。
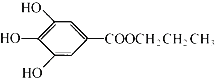
已知:PG经水解可转化为没食子酸,没食子酸能与NaHCO3溶液反应生成CO2
回答下列问题:
(1)从分子结构或性质上看,PG具有抗氧化作用的主要原因是:______(文字简述)
(2)1mol没食子酸最多可以与含________mol碳酸钠的溶液发生反应。
(3)写出PG在NaOH溶液中水解的化学方程式:_______________________。
(4)没食子酸有多种同分异构体,写出其中符合下列要求的同分异构体的结构简式:____。
a.含有苯环,且苯环上的一溴代物只有一种;
b.既能发生银镜反应,又能发生水解反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.含0.1molFeI2的溶液中通入0.125molCl2:2Fe2++8I-+5Cl2=2Fe3++4I2+10Cl-
B.浓硝酸中加入过量铁粉并加热:Fe+3NO3-+6H+![]() Fe3++3NO2↑+3H2O
Fe3++3NO2↑+3H2O
C.Cu溶于稀HNO3:Cu+2H++NO3-=Cu2++NO2↑+H2O
D.氢氧化铁中加入过量氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g))![]() 2SO3(g)反应过程的能量变化如图所示,已知1molSO2(g)被氧化为1molSO3(g)的ΔH=-akJ/mol(a﹥0)。回答下列问题:
2SO3(g)反应过程的能量变化如图所示,已知1molSO2(g)被氧化为1molSO3(g)的ΔH=-akJ/mol(a﹥0)。回答下列问题:
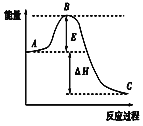
(1)图中A表示:__,E的大小对该反应的反应热ΔH__(填“是”或“否”)有影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点__(填“升高”或“降低”),理由是__。
(2)图中ΔH=__kJ/mol。
(3)在一定温度下,将2molSO2和1molO2放在一密闭容器中,在催化剂作用下充分反应。测得反应放出的热量__(填“等于”、“大于”或“小于”)2akJ。
(4)V2O5的催化循环机理可能为:V2O5氧化SO2时,自己被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:
①__;②4VO2+O2=2V2O5
(5)已知固态单质硫的燃烧热为bkJ/mol,计算由S(s)生成3molSO3(g)的ΔH=___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铋(Bi)及其化合物广泛应用于电子、医药等领域。一种以含铋矿石辉铋矿(主要成分为Bi2S3,含少量杂质PbO2等)为原料,采用湿法冶金制备铋单质的工艺流程如下:
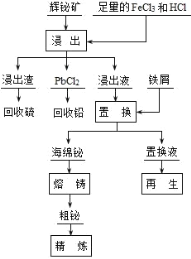
已知:PbCl2是一种难溶于冷水,易溶于热水的白色固体。 回答下列问题:
(1)铋(Bi)位于ⅤA族,铋的氢化物的热稳定性______氨气(填“大于”或“小于”)。
(2)“浸出”时,为了提高浸出速率,可采用的措施有______(任写一条)
(3)加热浸出时,PbO2 生成 PbCl2 和一种气体,此反应的化学方程式为______, 从产物中分离回收 PbCl2 的步骤是______、洗涤、干燥。从保护环境和原料循环利 用的角度,请指出上述工艺流程中可以采取的措施为______。
(4)电解精炼粗铋时必须补充含 Bi3+浓度高的电解液。可用粗铋、铅条作为两个电极,铅条外用素烧 的陶瓷坩埚作隔膜(Bi3+不能透过,H+能透过),电解液开始时为盐酸和食盐的混合液。则粗铋为电解池的 ______极,电解总反应为______。
(5)25℃时,向浓度均为 0.02mol·L-1 的 Cu2+、Bi3+的混合溶液中滴加 Na2S 溶液(设溶液体积增加 1倍),使 Cu2+恰好沉淀完全即溶液中 c(Cu2+)=1×10-5 mol·L-1,此时是否有 Bi2S3 沉淀生成______(列式计算说明)。(已知:25℃时,Ksp(CuS)=6.0×10-36、Ksp(Bi2S3)=1.8×10-99)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com