
【题目】X、Y、Z、W、M、R、Q是短周期主族元素,部分元素的原子半径和化合价信息如下表所示:
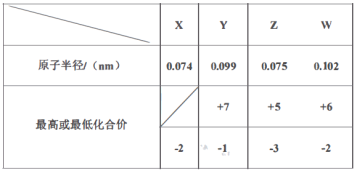
M的焰色反应为黄色:X、Y、R位于周期表中不同周期;Q的单质为半导体材料。
(1)Q元素在周期表中的位置是___;构成化合物M2X2的化学键类型是___。
(2)写出X、Y、R按原子个数之比为1:1:1形成的化合物的电子式___。
(3)Y与W相比,非金属性较强的是___(用元素符号表示),下列事实能证明这一结论的是___(选填字母序号)。
a.常温下W的单质呈固态,Y的单质呈气态
b.Y与W形成的化合物中W呈正价
c.Y和M反应时,lmolY原子所得电子数少于lmolW原子所得电子数
(4)R、W两种元素组成的离子在水溶液中与H+和OH-都不能大量共存,还能与氯水反应,写出其与新制氯水反应的离子方程式___。
(5)Z2R4为二元弱碱,在水中的电离与氨相似,写出其在水中的第一步电离方程式___,Z2R4与磷酸形成的磷酸二氢盐的化学式为___。
【答案】第一周期第ⅠA族 离子键、共价键 ![]() Cl b 4Cl2+4H2O+HS-=9H++SO42-+8Cl- N2H4+H2O
Cl b 4Cl2+4H2O+HS-=9H++SO42-+8Cl- N2H4+H2O![]() N2H5++OH- N2H6(H2PO4)2
N2H5++OH- N2H6(H2PO4)2
【解析】
从表格中可知,X的化合价为-2,X为O,Y的最高化合价为+7、最低化合价为-1,Y为Cl,W的最高化合价为+6、最低化合价为-2,W为S,Z的最高化合价为+5、最低化合价为-3,Z为N或P,且半径小于Y和W,所以Z为N,M的焰色反应为黄色,M为Na,X、Y、R位于周期表中不同周期,R为H,Q的单质为半导体材料,Q为Si。
(1)Q为H,在周期表中的位置是第一周期第ⅠA族;M为Na、X为O,构成化合物M2X2的化学式为Na2O2,化学键类型为离子键、共价键;
(2)X为O、Y为Cl、R为H,X、Y、R按原子个数之比为1:1:1形成的化合物为HClO,其电子式 ![]() ;
;
(3)Y为Cl、W为S,Y与W相比,非金属性较强的Cl;
a. 状态不能作为判断非金属性强弱的依据,a错误;
b. Cl与S形成的化合物中S呈正价,说明Cl吸引电子的能力强,Cl元素的非金属性更强,b正确;
c. 得电子数目与非金属性强弱无必然的联系,c错误;
(4)R为H、W为S,R、W两种元素组成的离子为HS-,在水溶液中与H+和OH-都反应,所以不能大量共存,能与氯水反应,其与新制氯水反应的离子方程式为:4Cl2+4H2O+HS-=9H++SO42-+8Cl-;
(5)Z为N、R为H,Z2R4为N2H4,二元弱碱,在水中的电离与氨相似,其在水中的第一步电离方程式为:N2H4+H2O![]() N2H5++OH-,N2H4与磷酸形成的磷酸二氢盐的化学式为N2H6(H2PO4)2
N2H5++OH-,N2H4与磷酸形成的磷酸二氢盐的化学式为N2H6(H2PO4)2


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列反应中,反应前后固体物质的质量不变的是( )
A.氢气通过灼热的CuO粉末B.二氧化碳通过Na2O2粉末
C.铝与Fe2O3发生铝热反应D.将锌粒投入Cu(NO3)2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把10.2g Na2CO3·10H2O和NaHCO3组成的固体混合物溶于水配成100 mL溶液,其中c(Na+)=0.8 mol·L-1。若把等质量的固体混合物加热至恒重,残留固体的质量是( )
A.3.18 gB.2.12 gC.4.24 gD.5.28 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种短周期主族元素,前三种元素在周期表中的位置如图所示:
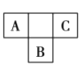
A、B、C三种元素中有两种元素的最高价氧化物对应的水化物是强酸,D元素的原子半径在短周期元素中最大,E是最高正价为![]() 的非金属元素。
的非金属元素。
(1)C在周期表中的位置是______
(2)A、B、C三种元素中两种元素所形成的两种强酸的分子式分别为______;上述五种元素形成的简单离子中,电子层结构相同的离子的半径由大到小的顺序为____________
(3)举例说明C的非金属性比B的非金属性强:____________
(4)D的单质与E所形成的最常见化合物能发生剧烈反应,写出相应的离子方程式:____________;A、E之间形成的最简单化合物(过量)与C的单质混合后可得到一种单质和一种盐,对应的化学方程式为____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】R、W、X、Y、M是原子序数依次增大的五种短周期主族元素。R最常见同位素的原子核中不含中子。W与X可形成两种稳定的化合物:WX和WX2。工业革命以来,人类使用的化石燃料在燃烧过程中将大量WX2排入大气,在一定程度导致地球表面平均温度升高。Y与 X 是同一主族的元素,且在元素周期表中与X相邻。
(1)W的原子结构示意图是_______________。
(2)WX2的电子式是________________。
(3)R2X、R2Y中,稳定性较高的是___________(填化学式),请从原子结构的角度解释其原因:_____________________。
(4)Se与Y是同一主族的元素,且在元素周期表中与Y相邻。
①根据元素周期律,下列推断正确的是___________填字母序号)。
a.Se的最高正化合价为+7价
b.H2Se的还原性比H2Y强
c.H2SeO3的酸性比H2YO4强
d.SeO2在一定条件下可与NaOH溶液反应
②室温下向SeO2固体表面吹入NH3,可得到两种单质和H2O,该反应的化学方程式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有a~g7种短周期主族元素,它们在元素周期表中的相对位置如图所示,请回答下列问题:
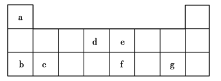
(1)下列选项中,元素的原子间最容易形成离子键的是______(填序号,下同),元素的原子间最容易形成共价键的是______。
A.![]() 和
和![]() B.
B.![]() 和
和![]() C.
C.![]() 和
和![]() D.
D.![]() 和
和![]()
(2)下列由a~g7种元素原子形成的各种分子中,所有原子最外层都满足8电子稳定结构的是______(填序号)。
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
(3)由题述元素中的3种非金属元素形成的AB型离子化合物的电子式为______。
(4)![]() 与
与![]() 可形成一种化合物
可形成一种化合物![]() ,其含有的化学键类型为______,其与过量稀盐酸反应的化学方程式为______。
,其含有的化学键类型为______,其与过量稀盐酸反应的化学方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有机物A与NaOH的醇溶液混合加热得产物C和溶液D。C与乙烯混合在催化剂作用下可反应生成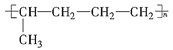 的高聚物。而在溶液D中先加入硝酸酸化,后加AgNO3溶液有白色沉淀生成,则A的结构简式可能为( )
的高聚物。而在溶液D中先加入硝酸酸化,后加AgNO3溶液有白色沉淀生成,则A的结构简式可能为( )
A.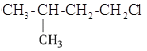 B.
B.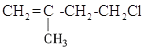
C.CH3CH2CH2ClD.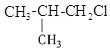
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用微生物燃料电池原理,可以处理宇航员排出的粪便,同时得到电能。美国宇航局设计的方案是:用微生物中的芽孢杆菌来处理粪便产生氨气,氨气与氧气分别通入燃料电池两极,最终生成常见的无毒物质。示意图如下所示。下列说法错误的是( )
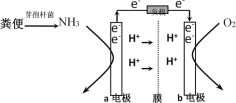
A.a电极是负极,b电极是正极
B.负极区发生的反应是2NH3 - 6e-=N2+6H+
C.正极区,每消耗标准状况下2.24 L O2,a向b电极转移0.4 mol电子
D.电池工作时电子通过由a经负载流向b电极,再穿过离子交换膜回到a电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应2NO2N2O4(g) H<0。将一定量的NO2充入注射器中并密封,改变活塞位置的过程中,气体透光率随时间的变化如图所示(气体颜色越深,透光率越小)。下列说法不正确的是
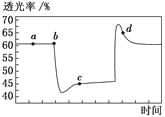
A.b 点的操作是压缩注射器
B.c 点与a点相比,c(NO2)增大、c(N2O4)减小
C.d 点:υ(正)<υ(逆)
D.若在c点将温度降低,其透光率将增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com