
【题目】下列物质中,只含有离子键的是
A.HClB.CaCl2C.NH4ClD.NaOH
科目:高中化学 来源: 题型:
【题目】2018年大部分地区爆发了流感流感常伴随发热高烧等症状。布洛芬是一种常用的儿童退热药,它的BHC合成法如下
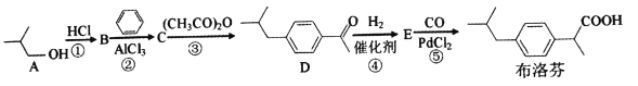
(1)A的名称是__________,B的核磁共振氢谱有__________种吸收峰。
(2)①反应需用浓盐酸而不用稀盐酸,其原因是______________________________。
(3)E的分子式是__________,官能团的名称是__________。
(4)③反应的化学方程式是____________________,反应类型是__________。
(5)满足下列条件的布洛芬的同分异构体有__________种
a遇FeCl3溶液显紫色 b.分子中有5种不同化学环境的氢 c.能发生银镜反应
(6)请写出由苯和( CH3COOCH2CO)2O为原料合成![]() 的线路图(其他试剂任选)___________
的线路图(其他试剂任选)___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生反应:C(s)+CO2(g) ![]() 2CO(g),下列说法不正确的是( )
2CO(g),下列说法不正确的是( )
A. 增大CO2浓度可以加快反应速率
B. 升高温度可以加快反应速率
C. 容器体积不变时,向其中充入N2,反应速率不变
D. 增加碳的质量可以加快反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是一种医药中间体,由芳香化合物A制备G的一种合成路线如下:

回答下列问题:已知:①酯能被LiAlH4还原为醇
②
(1)A的化学名称_________________。
(2)C的结构简式_______________,由B生成C的反应类型_____________。
(3)由F生成G的反应方程式_____________________。
(4)芳香化合物X是C的同分异构体,1mol X与足量碳酸氢钠溶液反应生成88g CO2,其核磁共振氢谱显示有3种不同化学环境的氢,峰面积之比为3:1:1的有________种,写出1种符合要求的X的结构简式__________________。
(5)参照上述合成路线,写出用甲醇和苯甲醇为原料制备化合物 的合成路线__________。
的合成路线__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石英砂岩,是硅石中的一种,其主要化学成分可简单表示为MgAl4Si10O26(OH)2(假设杂质均能溶于硫酸),工业上拟用该物质为原料制备高纯度硅,其艺流程如图所示:
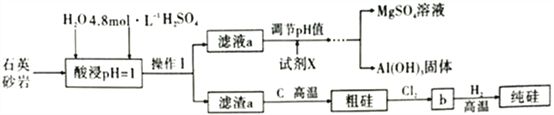
(1)请将石英砂岩的组成用氧化物的形式表示:________________,酸浸时,为了提高浸取率可采取的措施有______________________________________。(答出两点)
(2)实验室用18.4mol·L-1的浓硫酸配制250mL4.8mol·L-1的硫酸,需量取浓硫酸_______mL(结果保留一位小数);配制时所用玻璃仪器除量筒、烧杯和玻璃棒外,还需__________________________。
(3)制备高纯硅的过程中需要用到Cl2,请写出实验室制备Cl2的离子反应方程式:______________。
(4)请写出b和H2反应的化学方程式,并用单线桥法表示该反应过程中电子的转移:_______________。
(5)通过实验测得滤液a中c(Al3+)=1.0mol·L-1,c(Mg2+)=0.28mol·L-1,某同学打算通过调节溶液的pH值使Al3+和Mg2+完全分离(当离子浓度降到1.0×10-6mol·L-1时即视为完全分离),则试剂X用_______(填“0.1mol·L-1NaOH或“0.1mol·L-1氨水”)较好;沉淀时应控制溶液的pH值的取值范围为_______(已知:KspAl(OH)3=8.0×10-33,Ksp[Mg(OH)2]=2.8×10-11,lg2=0.3,lg5=0.7)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组分别用如图所示装置对原电池和电解原理进行实验探究。

请回答:
Ⅰ.用如图1所示装置进行第一组实验:
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是_______(填字母序号)。
A. 铝 B. 石墨 C. 银 D. 铂
(2)M极发生反应的电极反应式为________;
(3)实验过程中,SO42﹣________(填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有___________________,写出产生此现象的反应方程式:__________________;
Ⅱ.用如图2所示装置进行第二组实验:
(4)实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO42﹣)在溶液中呈紫红色。电解过程中,X极区溶液的pH________(填“增大”、“减小”或“不变”);
(5)电解过程中,Y极发生的电极反应为Fe﹣6e﹣+8OH﹣═FeO42﹣+4H2O 和 4OH﹣﹣4e﹣═2H2O+O2↑,若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少________g。
(6)在碱性锌电池中,用高铁酸钾作为正极材料,电池总反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2 该电池正极的电极反应式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300 ℃时,将2 mol SO2、1 mol O2混合于2 L的恒容密闭容器中,发生反应2SO2(g) + O2(g) ![]() 2SO3(g) ΔH,2 min末达到平衡,测得SO2的转化率为60%。请根据化学反应的有关原理回答下列问题:
2SO3(g) ΔH,2 min末达到平衡,测得SO2的转化率为60%。请根据化学反应的有关原理回答下列问题:
(1)能证明反应已经达到平衡状态的是________。
① c(SO2)∶c(O2)∶c(SO3) = 2∶1∶2
②单位时间内生成n mol SO3的同时消耗n mol SO2
③反应速率v(SO3) = 2v(O2)
④温度和体积一定时,容器内压强不再变化
⑤温度和压强一定时,混合气体的密度不再变化
(2)下图表示该反应的速率(v)随时间(t)变化的关系:
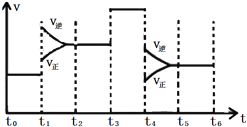
据图分析;t3时改变的外界条件可能是________;t6时保持体积不变向体系中充入少量He,平衡________(填“向左”“向右”或“不”)移动。SO2含量最高的区间是______(填“t0~t1”、“t2~t3”、“t3~t4”或“t5~t6”)。
(3)300 ℃时,该反应的平衡常数为________,若升高温度该反应的平衡常数减小,则ΔH___0(填“大于”、“小于”或“不确定”)。
(4)如果在相同条件下,上述反应从逆反应方向开始进行,开始时加入SO2 0.6 mol、SO3 1.4 mol,若使平衡时各物质的量浓度与原来平衡相同,则还应加入O2________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中加入氯化钡溶液生成白色沉淀,再加入稀硝酸沉淀不溶解也无气体逸出,则这种溶液中( )
A.一定含有SO42﹣
B.一定含有Ag+
C.可能不含CO32﹣
D.可能含有SO42﹣或Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,由N2O和CO2组成的混合气体的密度是C2H4、N2和H2组成的混合气体密度的 2倍,则C2H4、N2和H2组成的混合气体中H2的质量分数为
A. 3/13 B. 10/13 C. 大于3/13,小于10/13 D. 3/143
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com