
【题目】某同学设计的微型实验装置验证SO2的性质,通过分析实验,下列结论表达正确的是

A. a棉球褪色,验证SO2具有氧化性
B. b棉球褪色,验证SO2具有酸性氧化物的通性
C. c棉球蓝色褪去,验证SO2漂白性
D. 可以使用浓硫酸吸收尾气
【答案】B
【解析】
亚硫酸钠与浓硫酸反应生成二氧化硫,二氧化硫能使品红溶液褪色,二氧化硫是酸性氧化物,与碱反应生成亚硫酸钠和水,碘单质具有氧化性,能够氧化二氧化硫生成硫酸,据此分析解答。
A.a棉球中品红褪色,可以验证SO2具有漂白性,故A错误;
B.b棉球褪色,SO2与碱液反应,碱性减弱,溶液褪色,验证SO2具有酸性氧化物的性质,故B正确;
C.碘与SO2和水反应生成氢碘酸和硫酸,碘单质反应完全,c棉球蓝色褪去,可以验证SO2的还原性,故C错误;
D.SO2尽管有还原性,但不能被浓硫酸氧化,因此不能用浓硫酸吸收尾气,SO2具有酸性氧化物的性质,可以用碱液吸收尾气,故D错误;
答案选B。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】25℃时,用0.100mol·L-1的NaOH溶液滴定20.00mL0.100mol·L-1的HA溶液,溶液的pH与所加NaOH溶液体积(V)的关系如图所示。下列说法不正确的是
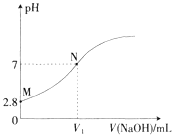
A. V1<20
B. Ka(HA)的数量级为10-5
C. M点溶液加少量水稀释,![]() 增大
增大
D. N点后,随着NaOH溶液的加入,溶液中水的电离程度逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既属于氧化还原反应,又是吸热反应的是:
A.铝片与稀盐酸反应B.Ba(OH)2·8H2O与NH4Cl反应
C.灼热的碳与CO反应D.甲烷在氧气中燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)利用原电池装置可以验证Fe3+与Cu2+氧化性相对强弱,如下图所示。

该方案的实验原理是自发进行的氧化还原反应可以设计为原电池。写出该氧化还原反应的离子方程式:__________。该装置中的负极材料是______(填化学式),正极反应式是_______。
(2)某研究性学习小组为证明2Fe3++2I-2Fe2++I2为可逆反应,设计如下两种方案。
方案一:
取5mL0.1mol/LKI溶液,滴加2mL0.1mol/L的FeCl3溶液,再继续加入2mLCCl4,充分振荡、静置、分层,再取上层清液,滴加KSCN溶液。
①方案一中能证明该反应为可逆反应的现象是______。
②有同学认为方案一设计不够严密,即使该反应为不可逆反应也可能出现上述现象,其原因是(用离子方程式表示)_____。
方案二:
设计如下图原电池装置,接通灵敏电流计,指针向右偏转(注:灵敏电流计指针总是偏向电源正极),随着时间进行电流计读数逐渐变小,最后读数变为零。当指针读数变零后,在右管中加入1mol/L FeCl2溶液。

③方案二中,“读数变为零”是因为____________.
④“在右管中加入1mol/L FeCl2溶液”后,观察到灵敏电流计的指针______偏转(填“向左”、“向右”或“不”),可证明该反应为可逆反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酰乙酸乙酯是有机合成中非常重要的原料,实验室制备乙酰乙酸乙酯的反应原理、装置示意图和有关数据如下所示:


实验步骤:
(I)合成:向三颈烧瓶中加入9.8 mL无水乙酸乙酯,迅速加入0.1 g切细的金属钠。水浴加热反应液,缓慢回流约2h至金属钠全部反应完。停止加热,冷却后向反应混合物中加入50%乙酸至反应液呈弱酸性。
(II)分离与提纯:
①向反应混合物中加入等体积的饱和食盐水,分离得到有机层。
②水层用5 mL无水乙酸乙酯萃取,分液。
③将①②所得有机层合并,洗涤、干燥、蒸馏得到乙酰乙酸乙酯粗产品。
④蒸馏粗产品得到乙酰乙酸乙酯3.9g。
(l)迅速加入金属钠的原因是_________(用化学方程式说明)。
(2)球形冷凝管中冷却水从_____(填“上”或“下”)口进入,上方干燥管中盛有无水CaCl2,其作用是_______。
(3)实验室制备乙酰乙酸乙酯时,通常在无水乙酸乙酯中加入微量的无水乙醇,其作用是_______。
(4)分离与提纯操作①中使用的分离仪器是_______。加入饱和食盐水的作用是_______。
(5)分离与提纯操作③用饱和NaHCO3溶液洗涤的目的是______________。
(6)本实验的产率为______%(结果保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,都是强电解质的是( )
A.HNO3、HCl、BaSO4B.NH4Cl、CH3COOH、Na2S
C.NaOH、Ca(OH)2、NH3·H2OD.HClO、CH3COONa、Ba(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中正确的是
A. FeBr2溶液中加入等物质的量的Cl2:2Fe2+ + 2Br- + 2Cl2 = 2Fe3++Br2+4Cl-
B. 用氢氟酸在玻璃上“刻字”:SiO2 + 4H+ + 4F- = SiF4↑+ 2H2O
C. 将铜丝投入稀硝酸中:Cu + 4H+ + 2NO3-= Cu2+ + 2NO2↑+ 2H2O
D. NaOH与NH4Cl溶液混合加热:NH4+ + OH- ![]() NH3·H2O
NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E都为短周期元素,A是相对原子质量最小的元素;B的+1价阳离子和C的-1价阴离子都与氖原子具有相同的电子层结构;D在C的下一周期,可与B形成BD型离子化合物;E和C为同一周期元素,其最高价氧化物对应的水化物为一种强酸.请根据以上信息回答下列问题.
(1)C元素在元素周期表中的位置是________________
(2)画出B元素的离子结构示意图______________
(3)与E的氢化物分子所含电子总数相等的分子是_____(举一例,填化学式,下同)、离子是_________
(4)D的单质与B的最高价氧化物对应的水化物的溶液发生反应的离子方程式为_________
(5)写出A元素与B元素形成化合物的化学式________
(6)下列可以判断C和D非金属性强弱的是_______
a.单质的熔点C比D低 b.单质与氢气反应C比D剧烈
c.气态氢化物稳定性C比D稳定 d.单质的密度C比D小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2mol金属钠和1mol氯气反应的能量关系如图所示,下列说法不正确的是

A. 相同条件下,K(s)的(ΔH2′+ΔH3′)<Na(s)的(ΔH2+ΔH3)
B. ΔH4的值数值上和Cl-Cl共价键的键能相等
C. ΔH5<0,在相同条件下,2Br(g)的ΔH5′>ΔH5
D. ΔH7<0,且该过程形成了分子间作用力
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com