
【题目】室温下,一气态烃与过量氧气混合完全燃烧,恢复到室温,使燃烧产物通过浓硫酸,体积比反应前减少50mL,再通过NaOH溶液,体积又减少了40mL,原烃的分子式是( )
A.CH4B.C2H4C.C2H6D.C3H8
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】三氯化铁是合成草酸铁的重要原料。
利用工业FeCl3制取纯净的草酸铁晶体[Fe2(C2O4)3·5H2O]的实验流程如下图所示:

(1)抑制FeCl3水解,溶液X为___________。
(2)流程中FeCl3能被异丙醚萃取,其原因是__________________________;检验萃取、分液后所得水层中是否含有Fe3+的方法是_______________________________________。
(3)得Fe2(C2O4)3·5H2O需用冰水洗涤,其目的是________________________。
(4)为测定所得草酸铁晶体的纯度,实验室称取a g样品,加硫酸酸化,用KMnO4标准溶液滴定生成的H2C2O4,KMnO4标准溶液应置于下图所示仪器_____(填“甲”或“乙”)中。
![]()
下列情况会造成实验测得Fe2(C2O4)3·5H2O含量偏低的是_____________。
a.盛放KMnO4的滴定管水洗后未用标准液润洗
b.滴定管滴定前尖嘴部分有气泡,滴定后消失
c.滴定前仰视读数,滴定后俯视读数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己烯雌酚是一种激素类药物,其结构简式如图所示。下列有关叙述中不正确的是( )
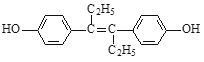
A. 己烯雌酚的分子式为C18H20O2
B. 己烯雌酚分子中一定有16个碳原子共平面
C. 己烯雌酚为芳香族化合物
D. 己烯雌酚可发生加成、取代、氧化、加聚、酯化、硝化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图示为一种天然产物,具有一定的除草功效,下列有关该化合物的说法错误的是( )

A.分子中含有三种含氧官能团
B.1mol该化合物最多能与6molNaOH反应
C.既可以发生取代反应,又能够发生加成反应
D.能与FeCl3发生显色反应,不能和NaHCO3反应放出CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作能达到相应实验目的的是
选项 | 实验目的 | 实验操作 |
A | 探究I-与Fe2+的还原性强弱 | 向FeCl3稀溶液中依次加入KI溶液、淀粉 |
B | 探究HPO42-在水溶液中的电离程度与水解程度的相对大小 | 测定0.1 mol·L-1NaH2PO4溶液的pH |
C | 配制0.1 mol·L-1邻苯二甲酸氢钾( | 称取5.1 g邻苯二甲酸氢钾于烧杯中,加入少量蒸馏水溶解,转移至500 mL容量瓶中定容 |
D | 比较CaCO3和CaSO4的Ksp大小 | 向澄清石灰水中滴入0.1 mol·L-1Na2CO3溶液至不再有沉淀产生,再滴加0.1 mol·L-1Na2SO4溶液 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是一种常用的还原剂、媒染剂。某化学小组同学在实验室里用如下两种方法来制备无水
是一种常用的还原剂、媒染剂。某化学小组同学在实验室里用如下两种方法来制备无水![]() 。有关物质的性质如下:
。有关物质的性质如下:
|
|
|
| |
溶解性 | 不溶于水,易溶于苯、乙醇 | 不溶于 | ||
熔点 |
| 53 | 易升华 | |
沸点 | 132 | 173 |
|
|
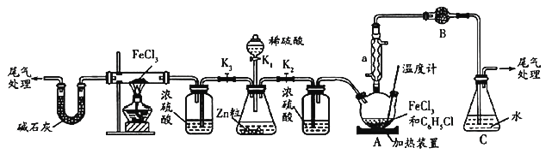
请回答下列问题:
(1)利用反应![]() 制取无水
制取无水![]() 并测定
并测定![]() 的转化率。按上图装置,在三颈烧瓶中放入
的转化率。按上图装置,在三颈烧瓶中放入![]() 无水氯化铁和过量的氯苯。打开
无水氯化铁和过量的氯苯。打开![]() 、
、![]() ,关闭
,关闭![]() ,通一段时间
,通一段时间![]() 后关闭
后关闭![]() ,控制三颈烧瓶内反应温度在
,控制三颈烧瓶内反应温度在![]() ,反应一段时间。反应完成后打开
,反应一段时间。反应完成后打开![]() 再通氢气一段时间。
再通氢气一段时间。
①仪器a的名称是_________,装置B中盛装的试剂是____________。
②反应后再通入![]() 的目的是________。
的目的是________。
③冷却实验装置,将三颈烧瓶内物质倒出,经过滤、用苯洗涤、干燥后,得到粗产品,回收滤液中![]() 的操作方法是________。
的操作方法是________。
(2)打开![]() 、
、![]() ,关闭
,关闭![]() ,通氢气与氯化铁反应制取无水
,通氢气与氯化铁反应制取无水![]() 。
。
①写出反应的化学方程式_____________。
②实验制得![]() 后并防止氧化的操作是_______。
后并防止氧化的操作是_______。
③请指出该制备方法的缺点________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学兴趣小组的同学们想要探究锰的性质,进行了下列实验和探究。
Ⅰ![]() 的制取:在查阅资料后,兴趣小组的同学们设计了以软锰矿石
的制取:在查阅资料后,兴趣小组的同学们设计了以软锰矿石![]() 为原料制取
为原料制取![]() 的步骤,并实验室模拟制备。
的步骤,并实验室模拟制备。
![]()
![]() 已知溶液Ⅰ中Mn为
已知溶液Ⅰ中Mn为![]() 价
价![]()
(1)在“碱熔氧化”时,既可将![]() 与KOH混合物熔融后通入氧气,也可加入
与KOH混合物熔融后通入氧气,也可加入![]() 作为氧化剂。请分析哪种方法更合适并简述理由:________。
作为氧化剂。请分析哪种方法更合适并简述理由:________。
(2)步骤①是________。酸化过程中只需通入过量![]() 即可,请写出对应的离子方程式:_________。
即可,请写出对应的离子方程式:_________。
(3)实际上用这种方法制取![]() 效率很低。若工业上要用此法制取
效率很低。若工业上要用此法制取![]() ,应_______以提高原料的利用率。在实际生产过程中,还可用Ni为阳极、Fe为阴极电解溶液Ⅰ以获得高浓度的
,应_______以提高原料的利用率。在实际生产过程中,还可用Ni为阳极、Fe为阴极电解溶液Ⅰ以获得高浓度的![]() 溶液,试写出阴极的电极反应方程式:_______。
溶液,试写出阴极的电极反应方程式:_______。
Ⅱ![]() 的成分探究:化学实验室存有一瓶开封已久的
的成分探究:化学实验室存有一瓶开封已久的![]() 试剂,化学兴趣小组欲研究该
试剂,化学兴趣小组欲研究该![]() 的纯度。
的纯度。
(1)打开试剂瓶时,有一股气流冲出。甲同学取少量粉末于试管中,加适量蒸馏水振荡,发现固体部分溶解,试管底部沉积有少量黑色不溶物,且溶解过程中管壁发热明显。甲同学查阅资料得知:![]() 变质时有
变质时有![]() 和两种含锰物质生成,且含锰物质中,较高氧化态物质与较低氧化态物质的物质的量之比为
和两种含锰物质生成,且含锰物质中,较高氧化态物质与较低氧化态物质的物质的量之比为![]() 。试写出
。试写出![]() 受热分解的化学方程式:________。
受热分解的化学方程式:________。
为进一步确定![]() 的纯度,乙同学和丙同学先后进行了以下实验;
的纯度,乙同学和丙同学先后进行了以下实验;
①取![]() 样品溶于试管中,过滤,得到黑色固体和滤液1;
样品溶于试管中,过滤,得到黑色固体和滤液1;
②洗涤黑色固体,留取洗涤液,重复三次;
③用分析天平称量黑色固体,其质量为![]() 。
。
(2)据此,乙同学计算得出![]() 的纯度为________
的纯度为________![]() 。
。
在乙同学的实验的基础上,丙同学继续完成了以下实验:
④将②中的洗涤液加入滤液1中,在滤液1中逐滴滴加![]() 溶液,直到灰绿色固体不再增加为止;
溶液,直到灰绿色固体不再增加为止;
⑤过滤,得滤液2,洗涤灰绿色固体并留取洗涤液,重复三次;
⑥将⑤中的洗涤液加入滤液2中,加水标定至![]() ,酸化后用标准液A进行滴定操作,每次取样
,酸化后用标准液A进行滴定操作,每次取样![]() ,总共重复进行了四次滴定实验。
,总共重复进行了四次滴定实验。![]() 提示:
提示:![]()
(3)若步骤④未将②中洗涤液加入滤液1中,会导致最终滴定结果________![]() 填“偏大”“偏小”或“不变”
填“偏大”“偏小”或“不变”![]() 。
。
(4)标准液A可选用下列的________![]() 填字母序号
填字母序号![]() 。
。
a.![]() 溶液 b.
溶液 b.![]() 溶液
溶液
c.![]() 酸性NaI溶液 d.
酸性NaI溶液 d.![]() 酸性
酸性![]() 溶液
溶液
(5)完成所有滴定实验后,最终丙同学计算出![]() 的纯度比乙同学计算所得的数据偏小,请结合上述实验操作分析两位同学实验结果差异较大的原因是______________
的纯度比乙同学计算所得的数据偏小,请结合上述实验操作分析两位同学实验结果差异较大的原因是______________![]() 写2条
写2条![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用甲烷与氯气发生取代反应,同时获得副产品盐酸的设想在工业上已成为现实。某化学兴趣小组拟在实验室中模拟上述过程,其设计的模拟装置如下:
根据要求填空:
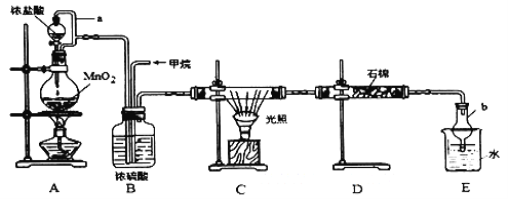
根据要求填空:
(1)A装置发生反应的离子方程式是_________________________________。C装置中CH4与Cl2生成一氯代物的化学反应方程式是___________________________ 。
(2)导管a的作用是____________。仪器b的名称是____________。
(3)D装置中的石棉上均匀附着潮湿的KI,其作用是______________ 。
(4)E装置的作用是____________。(填序号)。
A.收集气体 B.吸收氯气 C.防止倒吸 D.吸收氯化氢
(5)该装置的缺陷是没有进行尾气处理,其尾气的主要成分是_______.
A.CH4 B.CH3Cl C.CH2Cl2 D.CHCl3 E.CCl4
(6)设V(Cl2)/V(CH4)=x,若理论上欲获得最多的氯化氢,则x值应______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源。
(1)在25℃、101kPa下,16g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式为______。
(2)化学反应中放出的热能(焓变,△H)与反应物和生成物的键能(E)有关。已知:H2(g)+Cl2(g)=2HCl(g) △H=﹣185kJ/mol,E(H﹣Cl)=432kJ/mol,E(Cl﹣Cl)=243kJ/mol则E(H﹣H)=_____。
(3)纳米级Cu2O由于具有优良的催化性能而受到关注.已知:2Cu(s)+ ![]() O2(g)═Cu2O(s)△H=﹣169kJmol﹣1,C(s)+
O2(g)═Cu2O(s)△H=﹣169kJmol﹣1,C(s)+ ![]() O2(g)═CO(g)△H=﹣110.5kJmol﹣1,2Cu(s)+O2(g)═2CuO(s)△H=﹣314kJmol﹣1,则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式_____。
O2(g)═CO(g)△H=﹣110.5kJmol﹣1,2Cu(s)+O2(g)═2CuO(s)△H=﹣314kJmol﹣1,则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式_____。
(4)如图是N2(g)和H2(g)反应生成2molNH3(g)过程中能量变化示意图:
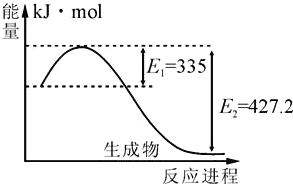
①请计算每生成1molNH3放出热量为:______。
②若起始时向容器内充入1molN2和3molH2达平衡后N2的转化率为20%,则反应放出的热量为Q1kJ,则Q1的数值为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com