
����Ŀ���Ҷ����������ᣬ������ˮ��Ϊ�˲ⶨ���ᾧ��H2C2O4��xH2O�е�xֵ��ijʵ��С�����ʵ�飬�������£�
�ٳ�ȡ1.260g���ᾧ�壬���100mL��Һ��
��ȡ25.00mL��H2C2O4��Һ������ƿ�ڣ��ټ�������ϡ���ᡣ
����Ũ��Ϊ0.1000mol/L��KMnO4����Һ���еζ������ζ��ﵽ�յ㡣
���ظ�ʵ�顣��¼�����������£�
ʵ����� | V(KMnO4��Һ) | |
�ζ�ǰ�̶�/mL | �ζ���̶�/mL | |
1 | 0.10 | 10.00 |
2 | 1.10 | 11.10 |
3 | 1.50 | 13.50 |
4 | 0.70 | 10.80 |
�ش��������⣺
(1)�Ҷ����KMnO4����Һ��Ӧ�����ӷ���ʽΪ____________
(2)�������Ҫʹ���ձ�����Ͳ������������ͷ�ιܣ���ȱ�ٵIJ�������Ϊ_______(������)������۵ζ������У�ʢװKMnO4��Һ������Ϊ__________________(������)��
(3)��ʵ��ζ��ﵽ�յ�ı�־��__________________________;
(4)�������ݣ�����H2C2O4��Һ�����ʵ���Ũ��Ϊ______mol/L��x=____________��
(5)���ζ��յ�ʱ���ӵζ��̶ܿȣ���xֵ��_____________(����ƫ��������ƫС������������) ��
���𰸡�2MnO4��+5H2C2O4+6H+=2Mn2++10CO2+8H2O 100mL����ƿ ��ʽ�ζ��� ���������һ��KMnO4��Һʱ����Һ����ɫ��Ϊ�Ϻ�ɫ���Ұ�����ڲ���ɫ������ζ��յ� 0.1000 2 ƫ��
��������
��1�����ᱻ���������Һ����Ϊ������̼��ˮ��
��2����������һ�����ʵ���Ũ�ȵ���Һ�IJ������ʹ�����������������Һ����ǿ�����ԣ��ܸ�ʴ��
��3�����������Һ����ɫ����ʼ����ĸ��������Һ�����ỹԭΪMn2+��������ز�����ɫʱ��������ȫ��Ӧ��
��4������c(H2C2O4)=![]() �������Ũ�ȣ�����
�������Ũ�ȣ�����![]() ����ƽ��Ħ���������ٸ���M����x����ֵ��
����ƽ��Ħ���������ٸ���M����x����ֵ��
��5�����ζ��յ����ʱ����Һ�棬���ĸ��������Һ�����ƫС��
��1�����ᱻ���������Һ����Ϊ������̼��ˮ����Ӧ�����ӷ���ʽ��2MnO4��+5 H2C2O4+ 6H+=2Mn2++10CO2��+8H2O��
�������2MnO4��+5 H2C2O4+ 6H+=2Mn2++10CO2��+8H2O��
��2����������һ�����ʵ���Ũ�ȵ���Һ�IJ��裺���㡢�������ܽ⡢��Һ��ϴ�ӡ����ݡ�ҡ�ȡ�װƿ���棬���100mL��Һ����Ҫʹ���ձ�����Ͳ����������100mL����ƿ����ͷ�ιܵȣ����������Һ����ǿ�����ԣ��ܸ�ʴ�����������Һʢװ����ʽ�ζ����У�
�����Ϊ��100mL����ƿ �� ��ʽ�ζ��ܣ�
��3�������һ��K2MnO4��Һ����H2C2O4����Һ�У���Һ����ɫ��Ϊ��ɫ����������Ӳ��ָ�ԭ������ɫ���ﵽ�ζ��յ㣬�ζ�������
�����Ϊ�����������һ��KMnO4��Һʱ����Һ����ɫ��Ϊ�Ϻ�ɫ���Ұ�����ڲ���ɫ������ζ��յ㣻
��4����3��ʵ�����ƫ��������Χ����1����2����4��ʵ��ƽ�����ĸ��������Һ�������10mL������c(H2C2O4)=![]() ��c(H2C2O4)=
��c(H2C2O4)=![]() mol/L��n(H2C2O4)=0.1mol/L��0.1L=0.01mol������
mol/L��n(H2C2O4)=0.1mol/L��0.1L=0.01mol������![]() ��
��![]() ��90+18x=126��x=2��
��90+18x=126��x=2��
�������0.1000 �� 2��
��5�����ζ��յ����ʱ����Һ�棬���ĸ��������Һ�����ƫС����ò���Ũ��ƫС����������ʵ���ƫС��Mƫ������xƫ��
�����Ϊ��ƫ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������п����ΪʳƷпǿ������ԭ�ϡ���ҵ�ϳ�����п����������п����п�����Ҫ�ɷ���ZnCO3������������Fe2O3��FeCO3��MgO��CaO�ȣ�������������ͼ���£�

(1)����п����ĥ�ɷ۵�Ŀ����___________________________��
(2)д��Fe3+ˮ������ӷ���ʽ_____________________________________________��
(3)�����±����ݣ���������Һ2����pHʱ�������Ͽ�ѡ�õ��������Ϊ__________��
������ѧʽ | Mg(OH)2 | Zn(OH)2 | MgCO3 | CaCO3 |
��ʼ������pH | 10.4 | 6.4 |
|
|
������ȫ��pH | 12.4 | 8.0 |
|
|
��ʼ�ܽ��pH |
| 10.5 |
|
|
Ksp | 5.6��10-12 |
| 6.8��10-6 | 2.8��10-9 |
(4)��ҵ�ϴ�����Һ3����ȡMgO�����У����ʵķ�Ӧ����________ѡ����š�
A������ʯ�� B��ʯ���� C��������Һ D����ˮ
(5)����Һ4��֮��IJ�������Ϊ______________��______________�����ˡ�ϴ�ӡ����
(6)����ͼ�����ݣ���п�����ZnCO3����������������__________�ô���ʽ��ʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ����ʶ������ԭ��Ӧ���Ȼ�刺ɳ�ȥͭ�����������ͭ��![]()
��1��������ԭ��Ӧ��ʵ����__________����д��ţ���
A��������ʧ�� B�����ϼ۵����� C���������������� D�����ӵĵ�ʧ��ƫ��
��2���õ����ű��������Ӧ�е���ת�Ƶķ������Ŀ________��
��3��������Ӧ�У��Ȼ����N�Ļ��ϼ�_______������������������������_____������������ʧ�������ӣ���____������������������ԭ������������_____����������������ԭ�����ԣ�����____����������������ԭ������Ӧ��
��4���������ͻ�ԭ�����ʵ���֮����___��
��5��������![]() 11.2 L����״����ʱ��ת��___�����ӣ�����ԭ��CuO__mol��
11.2 L����״����ʱ��ת��___�����ӣ�����ԭ��CuO__mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼװ�ÿ�������������ϴ�ӡ�����ռ���������β�����������塣��װ�ÿ����ڣ�������

A.�������������
B.����غͶ���������������
C.̼��ƺ��������ɶ�����̼
D.�Ȼ��ƺ�Ũ���������Ȼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ȼ������Ҫ�ɷ�ΪCH4���ɽ�CH4��Ƴ�ȼ�ϵ�أ��������Դ���⣬װ����ͼ��ʾ���ڱ�״���£�����ͨ����飬���ļ���VL������˵����������

A. ��0<V��33.6 Lʱ��������ӦʽΪCH4��10OH��-8e��== CO32����7H2O
B. ������ӦʽΪO2 +4H+ +4e��==2H2O
C. ��V=67.2 Lʱ������ܷ�Ӧ����ʽ��дΪCH4��2O2��NaOH== NaHCO3��2H2O
D. �������Һ�е�Na+�������ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������о�̼Ԫ�صĻ���������Ҫ���壬�ش��������⣺
(1)�ں��¡������ܱ������м���H2C2O4��������Ӧ��H2C2O4(s)![]() CO2(g)+CO(g)+H2O(g)������������˵����Ӧ�Ѿ��ﵽƽ��״̬����________��
CO2(g)+CO(g)+H2O(g)������������˵����Ӧ�Ѿ��ﵽƽ��״̬����________��
A��ѹǿ���ٱ仯
B��CO2(g)������������ֲ���
C�����������ܶȲ��ٱ仯
D����������ƽ��Ħ���������ֲ���
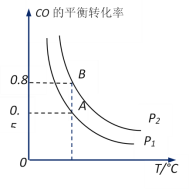
(2)��ҵ�Ͽ���ͨ����ӦCO(g)+2H2(g)![]() CH3OH(g)�Ʊ��״�����һ�ݻ��ɱ������г���2molCO��4molH2,CO��ƽ��ת �������¶�(T)��ѹǿ(P)�ı仯��ϵ��ͼ��ʾ���÷�Ӧ��H_______0(����>������<����������)���Ƚ�A��ʱ��CO��ʾ������Ӧ������B��ʱ��CH3OH��ʾ���淴Ӧ���ʵĴ�Сv��(CO)____v��(CH3OH)(����>������<����������)������ѹǿP1�´ﵽ��ѧƽ��״̬Aʱ�����������Ϊ10L�������Ӧ��ʼʱ�Գ���2molCO��4molH2,����ѹǿP2�´ﵽƽ��״̬Bʱ���������V(B)=________L��
CH3OH(g)�Ʊ��״�����һ�ݻ��ɱ������г���2molCO��4molH2,CO��ƽ��ת �������¶�(T)��ѹǿ(P)�ı仯��ϵ��ͼ��ʾ���÷�Ӧ��H_______0(����>������<����������)���Ƚ�A��ʱ��CO��ʾ������Ӧ������B��ʱ��CH3OH��ʾ���淴Ӧ���ʵĴ�Сv��(CO)____v��(CH3OH)(����>������<����������)������ѹǿP1�´ﵽ��ѧƽ��״̬Aʱ�����������Ϊ10L�������Ӧ��ʼʱ�Գ���2molCO��4molH2,����ѹǿP2�´ﵽƽ��״̬Bʱ���������V(B)=________L��
(3)��ƽ���ƶ��ĽǶȷ���AlCl3��Һ�����ܽ�CaCO3�����ԭ����_________________
(4)�����£����ijCaCO3�ı�����ҺpH=10.0������CO32���ĵڶ���ˮ�⣬����Ksp(CaCO3)=__________(������λ��Ч����)(��֪��Ka1(H2CO3)=4.4��10-7Ka2(H2CO3)=4.7��10-11)
(5)��һ�ֿɳ����Na-Al/FeS����ع���ʱNa+�����ʵ������ֲ��䣬�����ú�Na+�ĵ��������Ϊ����ʣ���֪�õ�ص�������ӦʽΪ2Na++FeS+2e-=Na2S+Fe, ��ŵ�ʱ������ӦʽΪ____________________���õ�س��ʱ����ת��2mol����ʱ�����������ı仯��Ϊ______g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ӧ��2SO2(g)��O2(g)![]() 2SO3(g) ��H<0��ij�¶��£���2 mol SO2��1 mol O2����10 L�ܱ������У���Ӧ�ﵽƽ���SO2��ƽ��ת����(��)����ϵ��ѹǿ(p)�Ĺ�ϵ��ͼ����ʾ��������˵����ȷ����( )
2SO3(g) ��H<0��ij�¶��£���2 mol SO2��1 mol O2����10 L�ܱ������У���Ӧ�ﵽƽ���SO2��ƽ��ת����(��)����ϵ��ѹǿ(p)�Ĺ�ϵ��ͼ����ʾ��������˵����ȷ����( )

A. ��ͼ��֪��A��SO2��ƽ��Ũ��Ϊ0.4 mol��L��1
B. ��ͼ��֪��B��SO2��O2��SO3��ƽ��Ũ��֮��Ϊ2��1��2
C. ��ƽ�����С�����ݻ�����Ӧ���ʱ仯ͼ�������ͼ�ұ�ʾ
D. ѹǿΪ0.50 MPaʱ����ͬ�¶���SO2ת�������¶ȹ�ϵ���ͼ����T2>T1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijУ��ѧ��ȤС���ѧ����ʵ�����ö������̺�Ũ���ᷴӦ����ȡ������װ����ͼ��

��1��д��ʵ������ȡ�����Ļ�ѧ��Ӧ����ʽ___��
��2��Ϊ�˳�ȥ�����е������Ȼ������壬�������ռ�����֮ǰ������������___�����Լ���ţ���Ϊ���ղ��������������ձ��м���___�����Լ���ţ����仯ѧ����ʽ��___��
A.ˮ B.Ũ���� C.����ʳ��ˮ D.�ռ���Һ
��3����ȤС���Ա��ͬѧ��Ϊ���˷�Ӧװ�û�����������ȡ___�����ţ���
A.���� B.���� C.������̼ D.�Ȼ���
���ǣ���Ա��ͬѧ��Ϊ��Ҫ������װ������ȡ��ͬѧ��������壬����Ľ����е�___�����ţ���������___��
A.����ķ���װ�� B.������ռ�װ�� C.β������װ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ����, ��Ա��еĢ١�����Ԫ��,��д���пհ�:
���� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0�� |
2 | �� | �� | �� | |||||
3 | �� | �� | �� | �� | �� | |||
4 | �� |
(1)����ЩԪ���У���ѧ�������������:_____(��Ԫ�ط���)��ԭ�ӽṹʾ��ͼΪ_____ ��
(2)������������ˮ�����У�������ǿ�Ļ�����Ļ�ѧʽ��_______��������ǿ�Ļ����������ʽ��:_____________��
(3)�õ���ʽ��ʾԪ�آ���Ļ�������γɹ��̣�________���û���������_____(�� �����ۡ������ӡ�)�����
(4)��ʾ����H�Ļ�����Ļ�ѧʽ_________________���û���������____________������ԡ����Ǽ��ԡ������γɵġ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com