
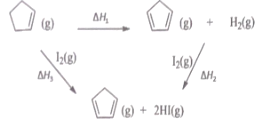
【题目】环戊二烯之(![]() ) 是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产,根据能量循环图和表格中的键能,下列说法正确的是
) 是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产,根据能量循环图和表格中的键能,下列说法正确的是
共价键 | 键能/ |
H-H | 436 |
H-I | 299 |
I-I | 151 |
A.△H1+△H2+△H3=0
B.△H1<△H3
C.![]() (g)转化为
(g)转化为![]() (g)的过程中,有C-H的断裂和形成
(g)的过程中,有C-H的断裂和形成
D.在相同条件下,生成 2molHCl(g) 的△H2′<△H2
【答案】D
【解析】
A.根据盖斯定律,△H3=△H1+△H2,则△H1+△H2-△H3=0,故A错误;
B.根据△H=反应物的键能之和-生成物键能之和,则△H3-△H1=△H2= E(I-I)+ E(H-H)- 2E(H-I)= 151kJ/mol+436 kJ/mol -2×299 kJ/mol =-11 kJ/mol<0,则△H3<△H1,故B错误;
C.![]() (g)转化为
(g)转化为![]() (g)的过程中,有C-H的断裂和C-C的形成,故C错误;
(g)的过程中,有C-H的断裂和C-C的形成,故C错误;
D.根据△H=反应物的键能之和-生成物键能之和,△H2= E(H-H)+E(I-I)-2E(H-I)= 151kJ/mol+436 kJ/mol -2×299 kJ/mol =-11 kJ/mol<0,Cl的半径小于I,Cl得电子能力比I强,形成的化学键的键能比I的大,放出的热量更多,△H2′<0,放出的热量越多,焓变越小,在相同条件下,生成 2molHCl(g) 的△H2′<△H2,故D正确;
答案选D。


科目:高中化学 来源: 题型:
【题目】氮氧化物是大气主要污染物,主要来自于工业废气及汽车尾气的排放,工业废气中NO是主要成分之一。
(1)乙烯作为还原剂的脱硝(NO),其反应机理示意图如图所示.写出解吸过程的化学方程式____________________。

(2)FeSO4-Na2SO3复合吸收剂吸收烟气中的NO,该方法利用Fe2+易与NO发生络合反应的特性,原理如下NO+FeSO4![]() Fe(NO)SO4
Fe(NO)SO4
①如图是一段时间内不同吸收剂对NO脱除率对比,加入Na2SO3溶液后,吸收效率增强,除了Na2SO3也能吸收部分NO外,还能防氧化从而增大Fe2+的含量,写出此原理的离子方程式_______________________________________。

②模拟实验表明,温度过高或过低都会降低NO的脱除率,其原因是_______________________________________。
(3)采用无隔膜法电解食盐水脱氮可将氮氧化物转化成NO3-,原理如图

①无隔膜条件下电解食盐水后溶液呈弱碱性,原因是____________________________.
②写出NO发生反应的离子方程式____________________________。
③根据下图所示,脱NO过程中控制溶液pH在______________范围内更合理。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业排放的烟气中的SO2是大气的一次污染物之一,同时也是雾篮天气的重要前体物。工业上常用氨水吸二氧化硫气体。常温时,向10mL0.1molL-l的氨水中通入SO2,SO2体积(标准状况)与溶液pH的关系如图所示(忽略溶液体积变化)。
已知:25℃时,NH3H2O的Kb=l.7×l0-5,H2SO3的Ka1=l.3×10-2,Ka2=6.2×l0-8。
回答下列问题:
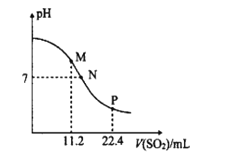
(1)M点溶液中阴离子浓度由大到小的顺序为__,![]() __(填>、=或<)2。
__(填>、=或<)2。
(2)N点溶液中的溶质为__(填化学式),c(NH4+):c(HSO3-)=__。
(3)水的电离程度M点__P点(填“大于”、“小于”或“等于”)。
(4)反应NH3H2O+H2SO3![]() NH4++HSO3-+H2O的平衡常数K=__。
NH4++HSO3-+H2O的平衡常数K=__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素L、X、Y、Z、W的原子序数依次递增,其中只有一种金属元素, L和Y、X和Z分别同主族,由X、Y、Z三种元素形成的化合物M结构如图所示,在工业上用作漂白剂等。下列叙述正确的是 ( )

A.简单离子半径:Z>W>Y>X>L
B.化合物M可用作氧化剂
C.Z、W的氧化物对应的水化物均为强酸
D.X、Z、W可分别与Y形成含有非极性共价键的二元离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组为了分析补血剂 FeSO4·7H2O 中铁元素的质量分数,用 KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:5Fe2++MnO4- +8H+= 5Fe3++Mn2++4H2O。
(1)实验前,首先要精确配制一定物质的量浓度的 KMnO4 溶液 250 mL,配制时需要用的仪器除天平、药匙、玻璃棒、烧杯、胶头滴管外,还需____________。
(2)滴定前是否要滴加指示剂?_____(填“是”或“否”),理由是_____。
(3)某同学设计的下列滴定方式中,最合理的是_____(填序号)
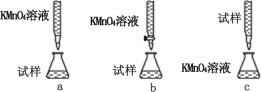
(4)该实验小组称取 12.0 g 补血剂在容量瓶中配成 100 mL 溶液,量取 25.00 mL 试样溶液, 用 0.100 mol·L-1 KMnO4标准溶液滴定。 达到滴定终点时, 消耗标准溶液20.00 mL,则所测补血剂中铁元素的质量分数是_____(精确至 0.01%)。
(5)若该小组配制溶液和滴定操作时引起的误差忽略,最终所测补血剂中铁元素含量 仍偏小,其可能原因是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列说法正确的是
A.pH 相等的盐酸和醋酸,加水稀释相同倍数后,c(Cl-)=c(CH3COO- )
B.0.l molL-1 氨水的p H= a,加入适量的氯化铵固体可使溶液pH= a+ l
C.物质的量浓度相等的 (NH4)2SO4 溶液与(NH4) 2CO3溶液中, 前者大于后者
前者大于后者
D.等物质的量浓度等体积的醋酸溶液和氢氟酸溶液,与足量氢氧化钠反应,放出的热量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以经预处理的废旧磷酸亚铁锂电极(主要成分为LiFePO4、 Al、C)为原料,生产Li2CO3 的部分工艺流程如下:
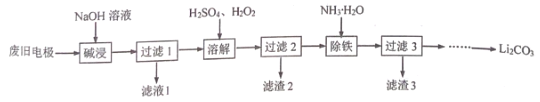
已知:LiFePO4难溶于水和碱性溶液,可溶于酸性溶液。Li2CO3溶于稀酸,微溶于水。下列说法不正确的是
A.滤渣2的主要成分为C
B.溶解时发生反应的离子反应方程式:2LiFePO4+2H++H2O2=2Li++2Fe3++ 2![]() + 2H2O
+ 2H2O
C.向过滤3的滤液中加入饱和Na2CO3溶液即可生成Li2CO3沉淀
D.已知将Li2CO3、FePO4x H2O、H2C2O4 混合反应可重新获得LiFePO4,理论上完全反应消耗的n(Li2CO3):n(FePO4x H2O):n(H2C2O4)=1:2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】褪黑素是一种内源性生物钟调节剂,在人体内由食物中的色氨酸转化得到

下列说法不正确的是
A.色氨酸分子中存在氨基酸和羧基,可形成内盐,具有较高的熔点
B.在色氨酸水溶液中,可通过调节溶液的pH使其形成晶体析出
C.在一定条件下,色氨酸可发生缩聚反应
D.褪黑素与色氨酸结构相似,也具有两性化合物的特性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用下列装置可测量一定质量的钢材中的含碳量(部分夹持装置已略去)。下列有关判断正确的是
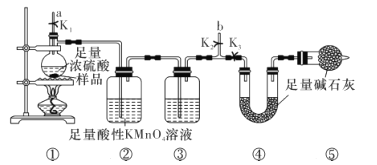
A.实验时,先打开K1、K2,关闭K3,从a处通入N2目的是排出装置中的CO2
B.点燃酒精灯前,需要打开K1、关闭K2,打开K3 ,K1起到平衡气压的作用
C.装置②中的酸性KMnO4溶液吸收H2S,装置③盛有浓硫酸,起到干燥作用
D.实验前后需称取装置④和装置⑤的质量,才能准确地测得钢材的含碳量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com