
【题目】室温下,下列各组离子在指定溶液中能大量共存的是
A.无色透明的溶液:Na+、Cu2+、NO3-、Cl-
B.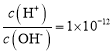 的溶液:K+、Na+、CO32-、NO3-
的溶液:K+、Na+、CO32-、NO3-
C.使甲基橙呈红色的溶液:Ba2+、NH4+、Cl-、ClO-
D.能溶解Al(OH)3的溶液:Na+、NH4+、NO3-、CH3COO-
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列实验现象或图像信息不能充分说明相应的化学反应是放热反应的是
A | B | C | D | |
图示 |
|
|
|
|
相关 信息 | 温度计的水银柱不断上升 | 反应物总能量大于生成物总能量 | 反应开始后,甲处液面低于乙处液面 | 反应开始后,针筒活塞向右移动 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型的电解废水处理技术是以活性炭为电极板和粒子凝胶颗粒填充的电解装置(如图所示)。用该装置电解过程中产生的羟基自由基(OH)氧化能力极强,能氧化苯酚为CO2、H2O。下列说法错误的是
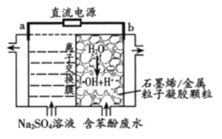
A.阳极电极反应为2H2O—4e-=O2↑+H+
B.H+通过离子交换膜向阴极移动
C.苯酚被氧化的化学方程式为C6H5OH+28OH=6CO2↑+17H2O
D.每转移0.7mole一两极室共产生气体体积为11.2L(标况)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种元素,A的最高正价与其最低负价的绝对值之差为6;A、D次外层都是8个电子,A与D的化合物DA在水溶液中能电离出具有相同电子层结构的阴、阳离子;B有两个电子层,其最高正价与最低负价的代数和为0;C2-与氩原子具有相同的电子层结构。
(1)试写出上述各元素的符号:A______,B______,C______,D______。
(2)画出下列粒子的结构示意图:A:________________,C2-:__________。
(3)元素A、C、D形成简单离子的半径由大到小的顺序是________________。
(4)写出A、D的最高价氧化物对应水化物反应的化学方程式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置及操作均正确的是
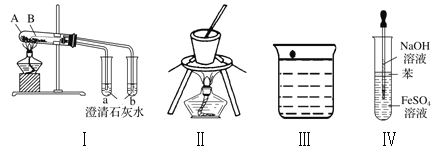
A. 图I中A盛放碳酸氢钠,B盛放碳酸钠,可对比二者的热稳定性
B. 图II可用于在碳酸钠溶液中提取碳酸钠固体
C. 图III为钠与水的反应现象探究实验的装置
D. 图IV为实验室制备观察氢氧化亚铁的装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子的检验方法正确的是
A.某溶液![]() 产生白色沉淀,说明原溶液中有Cl-
产生白色沉淀,说明原溶液中有Cl-
B.某溶液![]() 产生白色沉淀,说明原溶液中有SO42-
产生白色沉淀,说明原溶液中有SO42-
C.某溶液![]() 生成无色气体,说明原溶液中有CO32-
生成无色气体,说明原溶液中有CO32-
D.某溶液![]() 产生蓝色沉淀,说明原溶液中有Cu2+
产生蓝色沉淀,说明原溶液中有Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知浓硫酸和木炭粉在加热条件下可发生化学反应。
(1)上述反应的化学方程式为___________________________________;
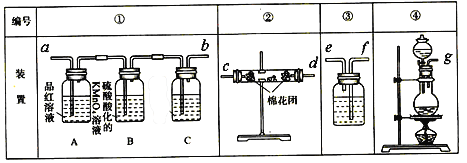
(2)试用下图所列各装置设计一个实验,来验证上述反应所产生的各种产物。
这些装置的连接顺序(按产物气流从左至右的方向)是(填装置中导管口的编号):
____接 ____,____接____,____接 ____。
(3)实验时可观察到装置①中A瓶中的溶液褪色,C瓶中的溶液不褪色。B瓶中的溶液的作用是____________________;C瓶中所加试剂是___________________。
(4)装置②中所加固体药品是无水硫酸铜,装置③中所加试剂是 _____________;装置④中带活塞的仪器名称为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ·mol-1表示。请认真观察如图,然后回答问题。
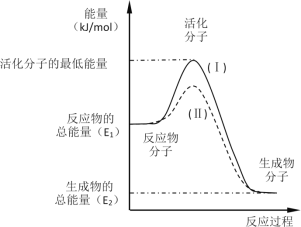
(1)图中所示反应是_________(填“吸热”或“放热”)反应,该反应_________(填“需要”或“不需要”)加热,该反应的△H =___________(用含E1、E2的代数式表示)。
(2)已知热化学方程式:H2(g)+![]() O2(g)=H2O(g);△H =-241.8 kJ·mol-1,该反应的活化能为167.2 kJ·mol-1,则其逆反应的活化能为____________________。
O2(g)=H2O(g);△H =-241.8 kJ·mol-1,该反应的活化能为167.2 kJ·mol-1,则其逆反应的活化能为____________________。
(3)已知4克H2燃烧生成液态水时放热为571.6kJ,试写出表示H2燃烧热的热化学方程式为:_________
(4)碳燃烧的热化学方程式为: C(s)+O2(g)=CO2(g);△H= -393.5kJ/mol试通过计算说明等质量的氢气和碳燃烧时产生热量的比是_____________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】学习了元素周期律后,同学们对第四周期过渡元素氧化物产生了浓厚的兴趣。是否只有二氧化锰能催化氯酸钾受热分解?氧化铁、氧化铜、氧化铬等对氯酸钾的受热分解有没有催化作用?对此他们进行了实验探究。请你根据要求完成下列部分实验报告。
(1)实验仪器及试剂:实验仪器:带铁夹的铁架台、带橡皮塞的导管、量气装置、过滤装置、电子天平、药匙、___、___、___等;
实验试剂:二氧化锰、氧化铁、氧化铜、氧化铬和氯酸钾;
(2)实验步骤:略;
(3)实验数据:
实验编号 | KClO3质量(g) | 氧化物化学式 | 氧化物质量(g) | 氧化物回收率 | 产生气体(mL)(已折算到标况) | 耗时(s) |
1 | 0.60 | 10 | 480 | |||
2 | 0.60 | MnO2 | 0.20 | 90% | 67.2 | 36.5 |
3 | 0.60 | CuO | 0.20 | 90% | 67.2 | 79.5 |
4 | 0.60 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 |
5 | 0.60 | Cr2O3 | 0.20 | 异常 | 67.2 | 188.3 |
(4)实验讨论:
a.在氧化物的回收过程中,要进行过滤操作,所用的玻璃仪器是玻璃棒、____;
b.实验编号3的实验中KClO3的分解率为____%(保留一位小数);
c.在用Cr2O3做研究实验时,发现有黄绿色刺激性气味的气体产生,同时绿色的混合物变成了橘黄色,该刺激性气体是___(填分子式),可用____试纸检验,上述异常现象产生的原因是____;
(5)实验结论:____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com