
【题目】向100mL0.1molL-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1molL-1Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示。下列说法正确的( )
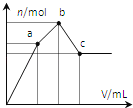
A.a点的溶液呈中性
B.a点沉淀的质量比c点沉淀的质量大
C.b点加入Ba(OH)2溶液的体积为250mL
D.至c点完成反应,反应的离子方程式可表示为:Al3++2SO42-+NH4++2Ba2++5OH-→AlO2-+2BaSO4↓+NH3H2O+2H2O
【答案】D
【解析】
100mL 0.1molL﹣1硫酸铝铵[NH4Al(SO4)2]中NH4Al(SO4)2物质的量为0.01mol.溶液含有NH4+0.01mol,Al3+0.01mol,SO42-0.02mol。
开始滴加时,发生反应为SO42-+Ba2+=BaSO4↓,Al3++3OH- =Al(OH)3↓,当Al3+沉淀完全时需加入0.03mol OH-,即加入0.015mol Ba(OH)2,加入的Ba2+为0.015mol,SO42-未完全沉淀,此时溶液含有硫酸铵、硫酸铝;(开始到a)
再滴加Ba(OH)2,生成BaSO4沉淀,发生反应为SO42-+Ba2+=BaSO4↓,NH4++ OH-=NH3H2O,所以沉淀质量继续增加;当SO42-完全沉淀时,共需加入0.02mol Ba(OH)2,加入0.04mol OH-,Al3+反应掉0.03molOH﹣,生成Al(OH)30.01mol,剩余0.01molOH﹣恰好与NH4+完全反应,此时溶液中NH4+完全反应,此时溶液为氨水溶液;(a到b)
继续滴加Ba(OH)2,Al(OH)3溶解,发生反应Al(OH)3+OH- =AlO2﹣+2H2O,由方程式可知要使0.01mol Al(OH)3完全溶解,需再加入0.005mol Ba(OH)2,此时溶液为氨水与偏铝酸钡溶液.(b到c)
A.由分析可知,从开始到a点,发生反应为SO42﹣+Ba2+=BaSO4↓,Al3++3OH﹣= Al(OH)3↓,a点对应的沉淀为BaSO4和Al(OH)3,溶液中的溶质是(NH4)2SO4,该物质水解溶液呈酸性,A错误;
B.a点沉淀的质量=0.015mol×233g/mol+0.01mol×78g/mol=4.275g,c点为硫酸钡的质量,为0.01mol×2×233g/mol=4.66g,所以质量c点>a点,B错误;
C.当SO42﹣完全沉淀时,共需加入0.02mol Ba(OH)2,则b点消耗氢氧化钡体积=![]() =0.2L=200mL,C错误;
=0.2L=200mL,C错误;
D.至c点完成反应,反应的离子方程式可表示为:Al3++2SO42﹣+NH4++2Ba2++5OH﹣=AlO2﹣+2BaSO4↓+NH3H2O+2H2O,D正确;
故选D。


科目:高中化学 来源: 题型:
【题目】SO2是造成空气污染的主要原因之一。可以用Na2SO3溶液为吸收液除SO2。
(1)反应的离子方程式是___________。
(2)已知NaHSO3溶液显酸性,请结合离子方程式,用盐的水解和电离理论进行解释:_________________。
(3)在Na2SO3稀溶液中各离子浓度从大到小排列顺序是___________________。
(4)往Na2SO3稀溶液中加入少量KOH固体完全溶解后(忽略溶解过程中溶液温度变化)溶液中c(Na+):c(SO32-)的比值________(填“变大”、“变小”或“保持不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是四种盐在不同温度下的溶解度(g/100g水):(假设:盐类共存时不影响各自的溶解度,分离晶体时,溶剂的损耗忽略不计)
NaNO3 | KNO3 | NaCl | KCl | |
10℃ | 80.5 | 21.2 | 35.7 | 31.0 |
100℃ | 175 | 246 | 39.1 | 56.6 |
用物质的量之比为1:1的硝酸钠和氯化钾为原料,制取硝酸钾晶体,其流程如图所示
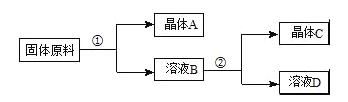
以下说法错误的是( )
A.①和②的实验过程中,都需要控制温度
B.①实验操作依次为:加水溶解、蒸发浓缩结晶、趁热过滤
C.②实验操作依次为:加水溶解、蒸发浓缩结晶、趁热过滤
D.用95%的酒精洗涤所得的硝酸钾晶体比较好
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以甲醇为燃料的电池中,电解质溶液为酸性,则负极反应式为______________,正极反应式为__________________。理想状态下,该燃料电池消耗1mol甲醇所能产生的最大电能为702.1kJ,则该燃料电池的理论效率为________________(燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比,甲醇的燃烧热为ΔH= -726.5kJ/mol)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由下列实验及现象推出的相应结论正确的是
选项 | 实验 | 现象 | 结论 |
A | 2 mL0.01mol·L-1的KI溶液中滴入等体积等浓度的FeCl3溶液,将充分反应后的溶液分三份,一份滴入K3[Fe(CN)6]溶液,第二份滴入KSCN溶液,第三份滴入淀粉溶液 | 滴入K3[Fe(CN)6]溶液后产生蓝色沉淀;滴入KSCN溶夜后变血红色;滴入淀粉溶液后溶液变蓝 | KI溶液和FeCl3溶液发生反应:2Fe3++2I- |
B | 向稀硫酸中加入铜片,然后通入氧气加热 | 先无明显现象,通入氧气加热后溶液变蓝 | 氧化性:稀硫酸>Cu2+ |
C | 向浓度均为0.1 mol·L-1的Na2SO3和Na2SiO3溶液中分别滴加酚酞 | Na2SiO3溶液红色更深 | 非金属性:Si<S |
D | 将几滴等浓度的FeCl3溶液、AlCl3溶液同时滴入足量等浓度的NaOH溶液中 | 只产生红褐色沉淀 | Ksp[Al(OH)3]>K sp[Fe(OH)3] |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛白粉(TiO2)是重要的白色颜料,LiFePO4是锂离子电池的正极材料。一种利用钛铁矿( 主要成分为FeTiO3 和少量Fe2O3 )进行钛白粉和LiFePO4 的联合生产工艺如下图所示:

回答下列问题:
(1) LiFePO4中Fe的化合价是_______________________。
(2)钛铁矿“酸溶”前需要进行粉碎,粉碎的目的是__________________________________。
(3)用离子方程式表示操作I加入铁粉的目的:__________________________。操作II为一系列操作,名称是加热浓缩、冷却结晶、过滤,其中用到的陶瓷仪器的名称是___________。
(4)TiO2+易水解,则其水解的离子方程式为______________________;“转化”利用的是TiO2+的水解过程,需要对溶液加热,加热的目的是________________________________。
(5)“沉铁”的的是使Fe3+生成FePO4,当溶液中c(PO43-)= 1.0×10-17mol/L时可认为Fe3+ 沉淀完全,则溶液中Fe3+沉淀完全时的c(Fe3+)=_______mol/L[已知:该温度下,Ksp(FePO4)=1.0×10-22]。
(6)由“沉铁”到制备LiFePO4的过程中,所需17% H2O2溶液与草酸( H2C2O4)的质量比是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应C(s)+H2O(g)![]() CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
①增加C的量 ②将容器的体积缩小一半 ③保持体积不变,充入N2使体系压强增大 ④保持压强不变,充入N2使容器体积变大
A.①④B.②③C.①③D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取氨气有几种方法。如图是实验室制气体的几种发生装置和吸收装置。
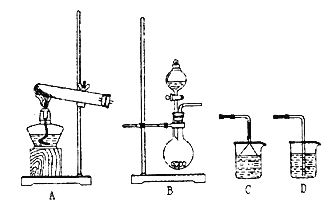
(1)当NH4Cl和Ca(OH)2来制取氨气时应选用的气体发生装置是___(填编号),该反应的化学方程式:___;
(2)①当用浓氨水和NaOH固体来制取氨气时应选用的气体发生装置是___(填编号)。
②欲用蒸馏水吸收氨气,应选择的吸收装置是所给装置中的___(填编号)
某化学课外兴趣小组探究铜跟浓硫酸反应情况。取6.4g铜片和10ml18mol/L浓硫酸放在圆底烧瓶中共热,直至反应完毕,最后发现烧瓶中还有铜片剩余外,同时他们根据科学的化学知识认为还有较多的硫酸剩余。
(3)①请写出铜跟浓硫酸反应的化学方程式:___;
②可以证明有余酸的实验方案是(________)
A.再加入铁粉 B.再滴入BaCl2溶液 C.再加入银粉 D.再滴入NaHCO3
(4)某工厂以Cu与硝酸为原料制取Cu(NO3)2,设计了下列两个方案:
方案A:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
方案B:2Cu+O2=2CuO;CuO+2HNO3=Cu(NO3)2+H2O
回答:①你认为较合理的方案是___(填A或B)。
②选择该方案的原因____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予美国和日本的三位科学家,以表彰他们在锂离子电池领域的贡献。某种锂离子电池的工作原理如图所示,工作原理为:LiCoO2+C6![]() Li1-xCoO2+LixC6
Li1-xCoO2+LixC6
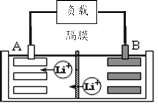
(1)该锂离子电池工作时A为____极,B的电极反应式为____。
(2)废旧锂离子电池的正极材料试样(主要含有LiCoO2及少量Al、Fe等)可通过实验方法回收钴、锂,实现废旧电池的资源化。
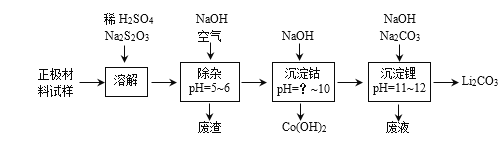
下表列出了几种离子生成氢氧化物沉淀的pH(“开始沉淀”的pH按金属离子浓度为0.1mol·L-1,“沉淀完全”是指溶液中离子浓度低于1.0×10-5 mol·L-1):
Al3+ | Fe3+ | Fe2+ | Co2+ | |
开始沉淀的pH | 4.0 | 2.7 | 7.6 | 7.0 |
沉淀完全的pH | 5.2 | 3.7 | 9.6 | ? |
①在上述溶解过程中,S2O32-被氧化成SO42-,LiCoO2在溶解过程中反应的化学方程式为____。
②除杂过程中,通空气将Fe2+氧化为Fe3+的目的是____。
③沉钴过程中,须调节溶液的pH不低于____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com