
����Ŀ���о�CO��CO2�����öԴٽ���̼���Ĺ���������Ҫ���塣��ش��������⣺
(1)����CO��H2��һ�������¿ɺϳɼ״���������Ӧ�� CO(g)+ 2H2(g)![]() CH3OH(g)�������ַ�Ӧ�����������ı仯������ͼ��a��b��ʾ������˵����ȷ����_____(����ĸ)��
CH3OH(g)�������ַ�Ӧ�����������ı仯������ͼ��a��b��ʾ������˵����ȷ����_____(����ĸ)��
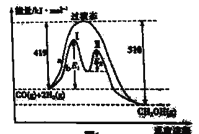
A.������Ӧ�ġ�H= -91 kJ��mol-1
B.�÷�Ӧ�Է����е�����Ϊ����
C. b����ʹ�ô������˷�Ӧ�Ļ�ܺ�H
D. b���̵ķ�Ӧ���ʣ��ڢ�Σ��ڢ��
(2)����ӦCO(g)+2H2(g)![]() CH3OH(g)���¶Ȳ���������㶨Ϊ1L�ܱ������з�������Ӧ�����и����ʵ����ʵ�����ʱ��仯������ʾ��
CH3OH(g)���¶Ȳ���������㶨Ϊ1L�ܱ������з�������Ӧ�����и����ʵ����ʵ�����ʱ��仯������ʾ��
ʱ��/min | 0 | 5 | 10 | 15 |
H2 | 4 | 2 | ||
CO | 2 | 1 | ||
CH3OH(g) | 0 | 0.7 |
�����и�������Ϊ�жϸ÷�Ӧ�ﵽƽ���־����_______(����ĸ)
A.2v��(H2)=v��(CH3OH)
B. CO��CH3OH�����ʵ���֮�ȱ��ֲ���
C.�������ƽ����Է����������ֲ���
D.���������ܶȱ��ֲ���
������ʼѹǿΪP0kPa����Ӧ�������õ�λʱ���ڷ�ѹ�ı仯��ʾ����10 min��H2�ķ�Ӧ����v(H2)=_____kPa/min�����¶��·�Ӧ��ƽ�ⳣ��Kp=______��(��ѹ=��ѹ�����ʵ�������)��
(3)�������������ܱ������������ͬ������м���1 mol CO��2 mol H2�������м���2 mol CO��4 molH2����ò�ͬ�¶���CO��ƽ��ת������ͼ��ʾ����L��M����������ƽ�ⳣ����K(M)_____ K(L)�� ѹǿ��p(M)__2p(L)��(�������<����=��)

(4)������������Ϊ�����缫��ϡ����Ϊ�������Һ����һ��������ͨ��CO2���е�⣬���������Ƶõ��ܶȾ���ϩ(![]() )�����ʱ�������ĵ缫��Ӧʽ��_________��
)�����ʱ�������ĵ缫��Ӧʽ��_________��
���𰸡�AD BC ![]()
![]() kPa-2���ɲ�����λ�� �� �� 2nCO2+12ne��+12nH+=
kPa-2���ɲ�����λ�� �� �� 2nCO2+12ne��+12nH+=![]() +4nH2O
+4nH2O
��������
(1)A.���ڷ�ӦCO(g)+ 2H2(g)![]() CH3OH(g)�����ݷ�Ӧ�����������ı仯ͼ�ɵá�H=����Ӧ�Ļ��-�淴Ӧ�Ļ��=419 kJ��mol-1-510 kJ��mol-1= -91 kJ��mol-1��A����ȷ��
CH3OH(g)�����ݷ�Ӧ�����������ı仯ͼ�ɵá�H=����Ӧ�Ļ��-�淴Ӧ�Ļ��=419 kJ��mol-1-510 kJ��mol-1= -91 kJ��mol-1��A����ȷ��
B.�÷�Ӧ����������������Ŀ��С�ķ�Ӧ�������ؼ����̡�S��0�����ݡ�G=��H-T��S����G��0���Է�����Ҫ���»����ſ����Է���B�����
C.b����ʹ�ô������˷�Ӧ�Ļ�ܣ�����Hֻ�뷴Ӧʼĩ״̬�йأ��뷴Ӧ;���أ�H�ʲ��䣬C�����
D.b�����е�I������Ӧ��ܽϸߣ��ʻ���ӵİٷֺ����ϵͣ���˻�ѧ��Ӧ���ʽ�����b���̵ķ�Ӧ���ʣ���I�Σ��ڢ�Σ�D����ȷ��
��˵����ȷ��ѡAD��
(2) ��A.���ڷ�ӦCO(g)+2H2(g)![]() CH3OH(g)����v��(H2)=2v��(CH3OH)ʱ����Ӧ����ƽ�⣬2v��(H2)=v��(CH3OH)�����淴Ӧ���������ʲ��ɱ�����δ�ﵽƽ�⣬��A�����
CH3OH(g)����v��(H2)=2v��(CH3OH)ʱ����Ӧ����ƽ�⣬2v��(H2)=v��(CH3OH)�����淴Ӧ���������ʲ��ɱ�����δ�ﵽƽ�⣬��A�����
B.��Ӧ��CO��������CH3OH�����ʵ���֮�ȴӿ�ʼ��Ӧ��С�������ֲ������˵���ﵽƽ�⣬B����ȷ��
C.�������ƽ����Է���������ֵ�ϵ���Ħ������M=![]() ����Ϊ�����غ�m���䣬�÷�Ӧ����������������Ŀ��С����n���С��M�����ﵽƽ��֮��M���䣬��C����ȷ��
����Ϊ�����غ�m���䣬�÷�Ӧ����������������Ŀ��С����n���С��M�����ﵽƽ��֮��M���䣬��C����ȷ��
D.���������ܶ�=![]() ��m������������̶�������������ܶ��Ǹ���ֵ��һֱ���䣬������ƽ����ж����ݣ�D�����
��m������������̶�������������ܶ��Ǹ���ֵ��һֱ���䣬������ƽ����ж����ݣ�D�����
������Ϊ�жϸ÷�Ӧ�ﵽƽ���־����BC��
��ͬ��1L�����У���������ʵ�����ѹǿ�����ȣ���ʼ����2 mol CO��4 molH2��������干6mol����ʼѹǿΪP0kPa������ʼ�����ķ�ѹ![]() P0kPa����Ӧ10 min H2�����ʵ���Ϊ2mol����ԭ���������ʵ�����һ�룬��Ӧ10 min H2�ķ�ѹ
P0kPa����Ӧ10 min H2�����ʵ���Ϊ2mol����ԭ���������ʵ�����һ�룬��Ӧ10 min H2�ķ�ѹ![]() P0kPa����10 min��H2�ķ�Ӧ����v(H2)=
P0kPa����10 min��H2�ķ�Ӧ����v(H2)=![]() =
= 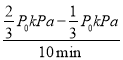 =
=![]() kPa/min����Ӧ10 min H2�����ʵ���Ϊ2mol��CO�����ʵ���Ϊ1mol�����ɵļ״�Ϊ1mol��������干4mol
kPa/min����Ӧ10 min H2�����ʵ���Ϊ2mol��CO�����ʵ���Ϊ1mol�����ɵļ״�Ϊ1mol��������干4mol![]() =
=![]() =
=![]() ����
����![]() =
=![]()
![]() kPa����ƽ��ʱH2�ķ�ѹP
kPa����ƽ��ʱH2�ķ�ѹP![]() =0.5��
=0.5��![]()
![]() =
=![]()
![]() kPa��ͬ��P
kPa��ͬ��P![]() = P
= P![]() =0.25��
=0.25��![]()
![]() =
=![]()
![]() kPa�����¶���ƽ�ⳣ��Kp=
kPa�����¶���ƽ�ⳣ��Kp=![]() =
=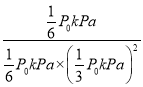 =
=![]() kPa-2��
kPa-2��
(3)����CO��ƽ��ת����-T-Pͼ�����������������䣨�۲�����ң��������¶ȣ�CO��ƽ��ת���ʽ��ͣ�����ƽ���ƶ�ԭ���ÿ��淴Ӧ������Ӧ�Ƿ��ȵģ���Kֵ���¶����߶����ͣ����ڼ������¶Ȳ����ʱ��ƽ�ⳣ������ͬ�ģ���L��M����������ƽ�ⳣ����K(M)��K(L)������м���1 mol CO��2 mol H2�������м���2 mol CO��4 molH2������ͬת���ʵ�����£�ƽ��ʱ���ҵ������ʵ������ڼ������ʵ�����2����������״̬����PV=nRT���¶�Խ�������ѹǿԽ��ѹǿ��p(M)��2p(L)��
(4)ͨ��CO2���������������е�⣬���������Ƶõ��ܶȾ���ϩ(![]() )��2nCO2��
)��2nCO2��![]() ��̼Ԫ�ػ��ϼ۴�+4����-2��ÿ��̼��6�����ӣ�2nCO2����12n�����ӣ��������ĵ缫��Ӧʽ��2nCO2+12ne��+12nH+=
��̼Ԫ�ػ��ϼ۴�+4����-2��ÿ��̼��6�����ӣ�2nCO2����12n�����ӣ��������ĵ缫��Ӧʽ��2nCO2+12ne��+12nH+=![]() +4nH2O��
+4nH2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
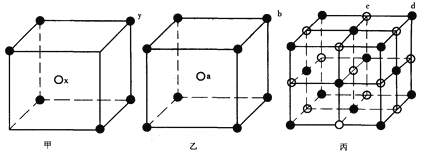
����Ŀ�����мס��ҡ���(����ͼ)���־���ľ���(����x���ھ��������ģ�����a���ھ���������)������֪��������x��y�ĸ�������__________���Ҿ�����a��b�ĸ�������__________������������________��c���ӣ���________��d���ӡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ú���ۺ�������һ��������Ⱦ�����ȼ�������ʵ���Ҫ���⣬�䳣�õķ�������ú��������Һ���Լ�ת��Ϊ�л���Ʒ�ȡ���ش��������⣺
��1����֪��I.C(s)��CO(g)��H2(g)��ȼ��������Ϊ��H1=-393.5kJ��mol-1����H2=-283.0kJ��mol-1����H3=-285.8kJ��mol-1
II.H2O(l)=H2O(g)��H4=��44.0kJ��mol-1
��ú������Ҫ��ӦC(s)��H2O(g)![]() CO(g)��H2(g)�ġ�H=___��
CO(g)��H2(g)�ġ�H=___��
��2������һ���µĸ��������м�������ú����ͨ��1molˮ������������ӦC(s)��H2O(g) ![]() CO(g)��H2(g)��������ָ���ܹ�˵���ѵ���ƽ��״̬����___ (����)��
CO(g)��H2(g)��������ָ���ܹ�˵���ѵ���ƽ��״̬����___ (����)��
��������ܶȱ��ֲ��䣻�ڶ���2molH-O����ͬʱ����1molH-H������CO������������ֲ��䣻�������ƽ��Ħ���������䣻��CO��H2�ı������ֲ��䣻��������ѹǿ���ֲ��䡣
��3��������ˮú��CO��H2����CO(g)��2H2(g)![]() CH3OH(g)�ɵõ��״�������ʵ��ú�ļ��Һ������֪��T��ʱ��������Ӧ����Ϊv��=k����(CO)��c2(H2)���淴Ӧ����Ϊv��=k����c(CH3OH)������kΪ���ʳ���������ֵk��=97.5��k��=39.0������¶��µ�ƽ�ⳣ��K=___������T���£���һ���Ϊ2L�ĸ����ܱ���ϵ��ͨ��3molCO��2molH2��5molCH3OH�����ʱ֤v��___v��(������������С��������������)��
CH3OH(g)�ɵõ��״�������ʵ��ú�ļ��Һ������֪��T��ʱ��������Ӧ����Ϊv��=k����(CO)��c2(H2)���淴Ӧ����Ϊv��=k����c(CH3OH)������kΪ���ʳ���������ֵk��=97.5��k��=39.0������¶��µ�ƽ�ⳣ��K=___������T���£���һ���Ϊ2L�ĸ����ܱ���ϵ��ͨ��3molCO��2molH2��5molCH3OH�����ʱ֤v��___v��(������������С��������������)��
��4������CO(g)��2H2(g)![]() CH3OH(g)������˵����ȷ����___(����ĸ)��
CH3OH(g)������˵����ȷ����___(����ĸ)��
A.��ѹ���������ʼӿ��ƽ��������Ӧ�����ƶ�
B.�״���ƽ�������������CO��H2Ͷ�ϱȵ����������
C.ʹ�ô����ܺõĴ����������H2��ƽ��ת����
D.�ں��º��������´ﵽƽ���ͨ��Ar��ƽ�����淴Ӧ�����ƶ�
E.��֪E[CO(g)��2H2(g)]>E[CH3OH(g)](E��ʾ���ʵ�����)�������������������Ӧ���еij̶�
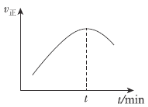
��5����һ����ĺ��������У�����һ������CO(g)��H2(g)��ģ��CO(g)��2H2(g)![]() CH3OH(g)�����v����ʱ��ı仯������ͼ��ʾ����t֮ǰv���������ԭ��Ϊ___��t֮��v������С��ԭ��Ϊ___��
CH3OH(g)�����v����ʱ��ı仯������ͼ��ʾ����t֮ǰv���������ԭ��Ϊ___��t֮��v������С��ԭ��Ϊ___��
��6��ú����һϵ��ת�����ɵõ����ᡣ�����£���ijŨ�ȵIJ�����Һ�м���һ����ijŨ�ȵ�NaOH��Һ��������Һ��c(HC2O4-)=c(C2O42-)�����ʱ��Һ��pH=___(��֪������H2C2O4��Ka1=6��10-2��Ka2=6��10-5��lg6=0.8)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��þ����Һ̬�������ܵ�ع���ԭ������ͼ��ʾ���õ������Һ���ܶȲ�ͬ�������������·�Ϊ���㣬����ʱ�м�������ε���ɼ�Ũ�Ȳ��䡣����˵������ȷ����
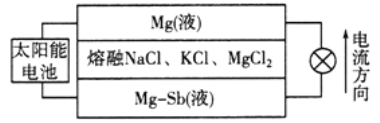
A. �ŵ�ʱ��Mg(Һ)���������С
B. �ŵ�ʱ��������ӦΪ��Mg2++2e===Mg
C. �õ�س��ʱ��Mg��Sb(Һ)�����������
D. �õ�س��ʱ��C1���²㷽���ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������£���һԪ��HA����Һ��KOH��Һ�������ϣ����Ի�Ϻ���Һ������仯����ʵ���������±���
ʵ����� | ��ʼŨ�ȣ���mol��L��1�� | ��Ӧ����Һ��pH | |
c��HA�� | c��KOH�� | ||
�� | 0.1 | 0.1 | 9 |
�� | x | 0.2 | 7 |
��ش�
��1��HA��Һ��KOH��Һ��Ӧ�����ӷ���ʽΪ________��
��2��ʵ��ٷ�Ӧ�����Һ����ˮ�������c��OH������________mol��L��1��x________0.2mol��L��1���������������������
��3�����й���ʵ��ڷ�Ӧ�����Һ˵������ȷ����________������ĸ����
a����Һ��ֻ����������ƽ��
b����Һ�У�c��A������c��HA����0.1mol��L��1
c����Һ�У�c��K������c��A������c��OH������c��H����
����֪2H2��g����O2��g����2H2O��1�� ��H����572kJ��mol��1��ij����ȼ�ϵ�������ɶ��ʯī��Ϊ�缫��KOH��ҺΪ�������Һ��
��4��д���õ�ع���ʱ�����ĵ缫��Ӧʽ________��
��5����������ȼ�ϵ��ÿ�ͷ�228.8kJ����ʱ��������1molҺ̬ˮ����õ�ص�����ת����Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ϸ��ˮƽ������Ч��������״����2019-nCoV�ĸ�Ⱦ���������Է��㻯����A ��������������(![]() )Ϊԭ�Ϻϳ�������୵ĺϳ�·����ͼ��
)Ϊԭ�Ϻϳ�������୵ĺϳ�·����ͼ��
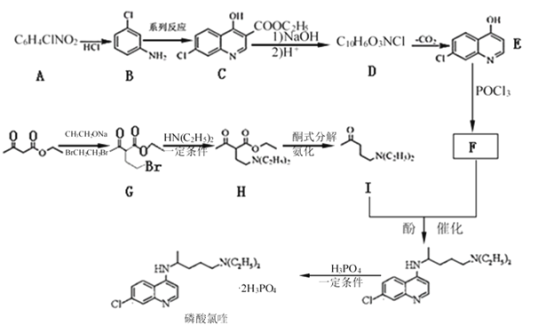
��֪����![]() ��������
��������
��![]()
![]()
![]()
��R1NH2+R2X![]() R1NHR2+HX(X��ʾ±ԭ��)��
R1NHR2+HX(X��ʾ±ԭ��)��
��ش��������⣺
(1) E�к��������ŵ�������________��G��H�ķ�Ӧ������________��
(2)̼ԭ��������4����ͬ��ԭ�ӻ����ʱ����̼��Ϊ����̼��д��B�������������ӳɺ�IJ���M�Ľṹ��ʽ�����Ǻ�(*)���M�е�����̼_________��
(3) F�Ľṹ��ʽ��_______��
(4)д��C��NaOH��Ӧ�Ļ�ѧ����ʽΪ___________��
(5) N��H��ͬ���칹�壬��������������N��ͬ���칹�干��____�֣� д������һ�ֺ˴Ź���������ʾ����ֻ��3��壬�ҷ����֮��Ϊ4��4��1�Ľṹ��ʽ________��
�ٺ��л���![]() ��-N(C2H5)2
��-N(C2H5)2
������ˮ������к�������
����������Ʒ�Ӧ����H2
(6)����������Ϣ�ͺϳ�·�ߣ�������Ա���1��4 -������Ϊԭ�Ϻϳ�![]() �ĺϳ�·��(���Լ���ѡ)____________��
�ĺϳ�·��(���Լ���ѡ)____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ܱպ��������н������з�Ӧ��aA(g)![]() bB(g)����Ӧ�ﵽƽ��״̬�������ݻ�����1��������Ӧ�ﵽ�µ�ƽ��״̬ʱ����Ӧ��A��Ũ����ԭ����46%��������������ȷ���ǣ� ��
bB(g)����Ӧ�ﵽƽ��״̬�������ݻ�����1��������Ӧ�ﵽ�µ�ƽ��״̬ʱ����Ӧ��A��Ũ����ԭ����46%��������������ȷ���ǣ� ��
A.��ѧ������a>b
B.�����ݻ�����ƽ�����淴Ӧ�����ƶ�
C.�����ݻ�����������B��������������
D.�÷�Ӧ������Ӧ�ų�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ҫ��ش��������⣺
�ٸɱ���CO2�� �ڰ�������ף� ��![]() Cl��
Cl��![]() Cl��
Cl��
��Һ������ˮ�� ��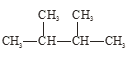 ��
��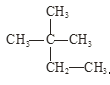 ��
��
����������������
(1)��Ϊͬλ�ص���_____________��
(2)��Ϊͬ�����������__________��
(3)��Ϊͬ���칹�����_________��
(4)����ͬ�����ʵ���_________��������ţ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й��̵Ļ�ѧ���������ȷ����
A.���Ƽ���ˮ�У����������ɣ�2Na + H2O = Na2O��H2��
B.��ϡ����������ʵ�飬���ݷ��⣺ H2O![]() H+��OH-
H+��OH-
C.��Al2��SO4��3��Һ�еμӰ�ˮ�����ɰ�ɫ������Al3+ + 3OH- =Al��OH��3��
D.�õ���ʽ��ʾNaCl���γɹ��̣�![]()
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com