
【题目】关于硫酸工业中的催化氧化反应,叙述正确的是( )
A.是吸热反应B.在常压下进行
C.在沸腾炉中进行D.使用铁触媒作催化剂
科目:高中化学 来源: 题型:
【题目】17克NH3共有mol原子,0.1molH2S共有个氢原子;同质量的NH3和H2S中分子个数比为 . 在标准状况下,35.5g氯气的体积是 L,将其与氢气完全化合,需氢气的物质的量是mol,将生成的气体配制成1L溶液,溶质的物质的量浓度是molL﹣1 , 将此溶液取出20mL加蒸馏水制成200mL溶液,此冲稀后溶液中溶质的物质的量浓度是molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以石英、焦炭为原料的部分化工流程如图所示. 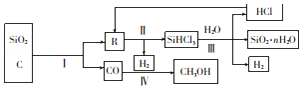
回答下列问题:
(1)反应I在工业上的作用是生产粗硅,为鉴定产品R中是否含有微量的铁单质,取少量R,用稀盐酸溶解,取上层清液后需再加入的试剂是(填字母). a.碘水 b.氯水 c.KSCN溶液 d.NaCl溶液
(2)反应Ⅱ要在干燥环境下迸行,其原因是;经冷凝得到的SiHCl3(沸点为33.0℃)中含有少量SiCl4沸点为57.6℃)和HC1(沸点为﹣84.7℃),则提纯SiHCl3的方法为 .
(3)将水蒸气通过灼热的煤粉可产生水煤气,其主要成分是CO、H2 . 工业上将水煤气液化后制得的CH3OH中含有的化学键类型为(填“离子键”或“共价键”);流程图中的反应Ⅲ为氧化还原反应,其化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸与高锰酸钾在酸性条件下能够发生反应:MnO4+H2C2O4+H+→Mn2++CO2↑+H2O(未配平).甲、乙两个实验小组分别利用酸性KMnO4溶液和H2C2O4溶液的反应来研究外界因素对反应速率的影响.
【实验设计】
甲组方案:通过测定生成CO2气体体积的方法来比较反应速率的大小.实验装置如图所示,25℃时将装置中的A溶液一次性加入B溶液(均已加入等量硫酸酸化)中.
实验编号 | A溶液 | B溶液 |
① | 2mL 0.1mol/LH2C2O4溶液 | 4mL0.0l1mol/L酸性KMnO4溶液 |
② | 2mL 0.2mol/LH2C2O4溶液 | 4mL0.01 mol/L酸性KMnO4溶液 |
(1)该反应中氧化剂和还原剂的物质的量之比为 .
(2)该实验探究的是对反应速率的影响.实现该实验目的还欠缺的仪器: . 比较①、②两组化学反应速率大小的方法是 .
乙组方案:用4mL0.0l1mol/L酸性KMnO4溶液与2mL 0.01mol/LH2C2O4溶液,研究不同条件对化学反应速率的影响.具体实验如下:
实验编号 | 10%硫酸的体积/mL | 温度/℃ | 其他物质 |
Ⅰ | 2 | 20 | ﹣ |
Ⅱ | 2 | 20 | 少量MnSO4粉末 |
Ⅲ | 2 | 30 | ﹣ |
Ⅳ | 1 | 20 | 1mL蒸馏水 |
(3)若要研究催化剂对化学反应速率的影响,则应对比实验(填序号,下同);若要研究温度对化学反应速率的影响,则应对比实验 .
(4)对比实验I和实验Ⅳ,可以研究硫酸的浓度对化学反应速率的影响,实验Ⅳ中加入1mL蒸馏水的目的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电池在通讯,交通及日常生活中有着广泛的应用。
(1)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可以表示为Cd+2NiO(OH)+2H2O![]() 2Ni(OH)2+Cd(OH)2。已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,以下说法中正确的是__________。
2Ni(OH)2+Cd(OH)2。已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,以下说法中正确的是__________。
①以上反应是可逆反应 ②以上反应不是可逆反应
③充电时化学能转变为电能 ④放电时化学能转变为电能
A.①③ B.②④ C.①④ D.②③
(2)废弃的镍镉电池已成为重要的环境污染物,有资料表明一节废镍镉电池可以使一平方米面积的耕地失去使用价值,在酸性土壤中这种污染尤为严重。这是因为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)对金属制品进行抗腐蚀处理,可延长其使用寿命。

①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是____________(用离子方程式表示)。为将碱洗槽液中的铝以沉淀的形式回收,最好向槽液中加入下列试剂中的________。
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为____________________。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极材料的原因是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在由5种基团-CH3、-OH、-CHO、-C6H5、-COOH两两组成的物质中,能与NaOH反应的化合物有( )
A.4种B.5种C.6种D.7种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重量法测定硫酸铜晶体结晶水含量时,会引起测定值偏高的是( )
A.未作恒重操作
B.硫酸铜部分分解
C.硫酸铜晶体未完全失水
D.坩埚放在空气中冷却
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题: 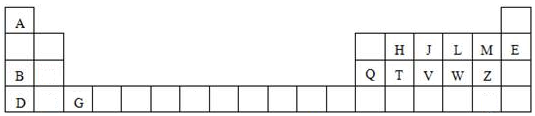
(1)原子半径最大的元素是;在化合物中只有负价的元素是;属于副族元素是;适合作半导体材料的是 , (只用表中的字母填写)
(2)V在周期表中的位置第周期第族.
(3)A与M元素形成的化合物是化合物,D与Z原子形成的化学键是键;
(4)J、H、T三种元素的最高价含氧酸的酸性由强到弱的顺序是;(用化学式表示)
(5)L元素形成的氢化物的在﹣4℃时是晶体(填晶体类型),其密度比对应的液态还小,呈固体而非气体的原因是 .
(6)写出B、Q两种元素的氧化物对应的水化物相互反应的化学方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com