
【题目】CH4超干重整CO2技术可得到富含CO的化工原料。回答下列问题:
(1)CH4超干重整CO2的催化转化如图所示:

①关于上述过程Ⅱ的说法不正确的是________(填序号)。
a.实现了含碳物质与含氢物质的分离
b.可表示为CO2+H2=H2O(g)+CO
c.CO未参与反应
d.Fe3O4、CaO为催化剂,降低了反应的ΔH
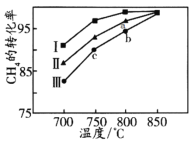
②其他条件不变,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,反应CH4(g)+CO2(g)=2CO(g)+2H2(g)进行相同时间后,CH4的转化率随反应温度的变化如图所示。a点所代表的状态_________(填“是”或“不是”)平衡状态;b点CH4的转化率高于c点,原因是_________________________________________。
(2)在一刚性密闭容器中,加入Ni/α-Al2O3催化剂并加热至1123K,使CH4和CO2发生反应CH4(g)+CO2(g)=2CO(g)+2H2(g),初始时CH4和CO2的分压分别为20kPa、25kPa,研究表明CO的生成速率υ(CO)=1.3×10-2·p(CH4)·p(CO2)mol·g-1·s-1,某时刻测得p(CO)=20kPa,则p(CO2)=________kPa,υ(CO)=________mol·g-1·s-1。
【答案】cd 不是 b和c都未达平衡,b点温度高,反应速率快,相同时间内转化率高 15 1.95
【解析】
(1)①a.过程Ⅱ中,CO、CO2都转化为CO,H2转化为H2O;实现了含碳物质与含氢物质的分离;
b.从起始反应物和产物分析可得,CO2与H2反应生成H2O(g)和CO;
c.从反应过程看,CO先转化为CaCO3,后CaCO3再转化为CO;
d.Fe3O4、CaO起初参加反应,后来又生成,所以为催化剂,催化剂不改变反应物和生成物的总能量。
②催化剂不能改变反应物的平衡转化率,但可改变平衡前的转化率,通过不同催化剂作用下的转化率比较,可判断a、b、c三点的CH4的转化率都小于同温度下的最高转化率,由此可确定反应仍正向进行。
(2)利用阿伏加德罗定律的推论,气体的压强之比等于物质的量之比,所以利用某时刻某物质的压强,可计算出该时刻另一物质的压强,由此可计算出反应速率。
(1)①a.过程Ⅱ中,CO、CO2都转化为CO,H2转化为H2O;实现了含碳物质与含氢物质的分离,a正确;
b.从起始反应物和产物分析可得,CO2与H2反应生成H2O(g)和CO,b正确;
c.从反应过程看,CO先转化为CaCO3,后CaCO3再转化为CO,c不正确;
d.Fe3O4、CaO起初参加反应,后来又生成,所以为催化剂,催化剂不改变反应物和生成物的总能量,所以不能降低反应的ΔH,d不正确;
故选cd。答案为:cd;
②相同温度下,尽管所使用的催化剂不同,但达平衡时CH4的转化率应相同,从图中可以看出,a点CH4的转化率比同温度下的催化剂Ⅰ作用下的转化率低,则表明a点所代表的状态不是平衡状态;从图中可以看出,虽然b点CH4的转化率高,但仍低于同温度下的最高转化率,说明反应仍未达到平衡,b点CH4的转化率高于c点,只能是反应速率快所致,故原因是b和c都未达平衡,b点温度高,反应速率快,相同时间内转化率高。答案为:不是;b和c都未达平衡,b点温度高,反应速率快,相同时间内转化率高;
(2)利用题给数据,我们可建立如下三段式:
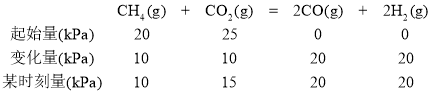
从而得出p(CO2)=15kPa,υ(CO)=1.3×10-2·p(CH4)·p(CO2)mol·g-1·s-1=1.3×10-2×10×15 mol·g-1·s-1=1.95 mol·g-1·s-1。答案为:15;1.95。


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】某混合物甲中含有明矾[KAl(SO4)2·12H2O]、Al2O3和Fe2O3。在一定条件下由甲可实现下图所示的物质之间的转化。
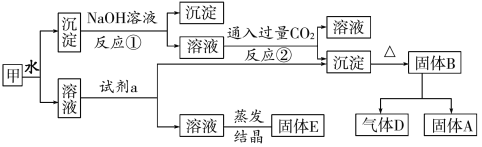
请回答下列问题:
(1)写出A、B、的化学式:A_____________, B_____________。
(2)试剂a最好选用______________。
A、NaOH溶液 B、稀盐酸
C、二氧化碳 D、氨水
(3)写出反应①的离子方程式:____________________。
(4)固体E可以作为复合性的化学肥料,E中所含物质的化学式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。
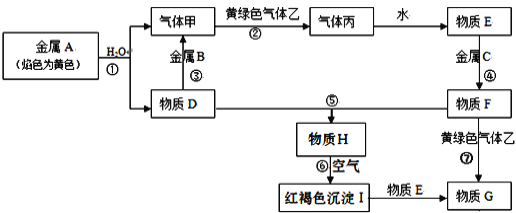
请回答下列问题:
(1)反应③的离子方程式___。
(2)反应⑥化学方程式____。
(3)反应⑦的离子方程式____;物质H在空气中的现象____。
(4)D溶液中加入B的氧化物固体的离子反应方程式为___,向反应后的溶液中通入过量CO2的离子反应方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】兴趣小组在实验室中模拟利用甲烷和氯气发生取代反应制取副产品盐酸,设计如图装置,下列说法错误的是
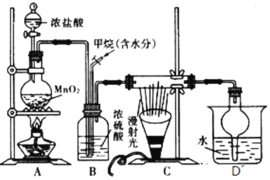
A.实验时先点燃A处酒精灯再通甲烷
B.从D中分离出盐酸的方法为过滤
C.装置C经过一段时间的光照射后,生成的有机物有4种
D.装置B有均匀混合气体、控制气流速度、干燥混合气体等作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴蓝(化学式Al2CoO4)是一种耐热、耐光、耐酸、耐碱腐蚀的蓝色颜料。某企业利用含铝锂钴废料(铝箱、CoO和Co2O3、Li2O)制备钴蓝的工艺流程如下:
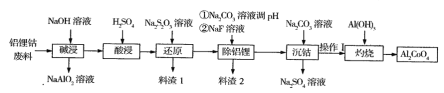
回答下列问题:
(1)碱浸时要有防火、防爆措施,原因是______,操作I的内容是_______。
(2)在实验室模拟工业生产时,也可用盐酸酸浸出钴,但实际工业生产中却不用盐酸,请 从反应原理分析不用盐酸浸出钴的主要原因___。
(3)写出“还原”过程中反应的离子方程式____。
(4)料渣2的主要成分是A1(OH)3 、____,写出灼烧时反应的化学方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了避免NO、NO2、![]() 对大气的污染,常用氢氧化钠溶液进行吸收处理(反应的化学方程式:
对大气的污染,常用氢氧化钠溶液进行吸收处理(反应的化学方程式:![]() =
=![]() ;
;![]() =
=![]() )。现有由amolNO、bmolNO2、cmolN2O4 组成的混合气体恰好被VL氢氧化钠溶液吸收(无气体剩余),则此氢氧化钠溶液的物质的量浓度最小为( )
)。现有由amolNO、bmolNO2、cmolN2O4 组成的混合气体恰好被VL氢氧化钠溶液吸收(无气体剩余),则此氢氧化钠溶液的物质的量浓度最小为( )
A.![]()
B.![]()
C.![]()
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物X是一种免疫调节剂,其结构简式为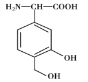 ,下列有关X的说法中错误的是
,下列有关X的说法中错误的是
A.其共平面碳原子最多有9个
B.既能与钠反应也能与NaHCO3溶液反应
C.能发生加成反应
D.X分子间能发生取代反应但分子内不能发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组在实验室用二氧化锰和浓盐酸共热制备并收集纯净、干燥的氯气,并进行氯气性质的探究。
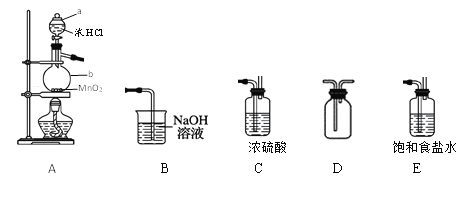
(1)仪器a、b的名称是____。
(2)以上装置A、B、C、D、E从左到右的连接顺序为____________。
(3)如何检查装置A的气密性?____。
(4)装置A中发生反应的离子方程式为____。
(5)装置B的作用是___,有同学觉得此装置不够完善,请你提出改进意见_____。
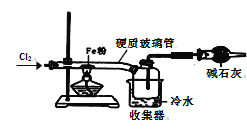
(6)该小组同学设计如图所示装置探究氯气的氧化性。通入氯气时硬质玻璃管中的现象是__,原因是__(用化学方程式解释)。
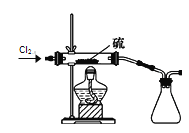
(7)二氯化硫(S2Cl2)在工业上用于橡胶的硫化。为了在实验室合成S2Cl2,该小组用下图装置将干燥的氯气在110~140℃与硫反应,即可得S2Cl2粗品。写出发生反应的化学方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属单质 A、B 和气体甲、乙、丙以及物质 C、D、E、F,它们之间能发生如下反应。(图中有些反应的产物和反应条件没有标出)
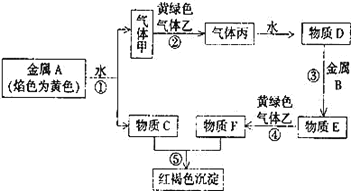
请回答下列问题:
(1) A 的化学式为_____,F 的化学式为_____;
(2) 写出 C 溶液与 Al 反应的离子方程式_____。
(3) 写出 C 溶液与黄绿色气体乙反应的化学方程式_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com