
【题目】一定条件下,反应CO(g)+H2O (g)![]() CO2(g)+H2(g),△H>0,达到平衡状态后,分别改变某个条件,下面四个说法中,条件改变、影响原因、影响结果均正确的是
CO2(g)+H2(g),△H>0,达到平衡状态后,分别改变某个条件,下面四个说法中,条件改变、影响原因、影响结果均正确的是
条件改变 | 影响原因 | 影响结果 | |
A | 适当缩小容器的容积 | 活化分子所占百分比增大,正逆反应速率均同等程度加快 | 平衡不移动 |
B | 适当升高温度 | 活化分子所占百分比增大,正逆反应速率加快,逆反应速率减慢 | 平衡正向移动 |
C | 加入催化剂 | 分子能量增大,活化分子所占百分比增大,正逆反应速率均同等程度加快 | 平衡不移动 |
D | 适当扩大容器的容积 | 活化分子所占百分比不变,但是单位体积内的活化分子数减少,正逆反应速率同等程度减慢 | 平衡不移动 |
A.AB.BC.CD.D
【答案】D
【解析】
A.缩小容器体积,容器内压强增大,活化分子数不变,分子总数不变,活化分子百分比不变,单位体积内活化分子数增加,有效碰撞频率增加,该反应为气体等体积反应,化学平衡不移动,故A错误;
B.升高温度,活化分子数增加,分子总数不变,单位体积内活化分子数增加,有效碰撞频率增加,正逆反应速率均增加,该反应正向为吸热反应,平衡向吸热反应方向移动,故B错误;
C.加入催化剂可降低反应的活化能,活化分子数增加,单位体积内活化分子数增加,有效碰撞频率增加,正逆反应速率同等程度加快,平衡不移动,故C错误;
D.扩大容器体积,容器内压强减小,活化分子数以及分子总数不变,单位体积内活化分子数减小,有效碰撞频率减小,正逆反应速率均减小,该反应为气体等体积反应,平衡不移动,故D正确;
故答案为:D。


科目:高中化学 来源: 题型:
【题目】一定温度下,在3个1.0 L的恒容密闭容器中分别进行反应2X(g)+Y(g)![]() Z(g) ΔH,达到平衡。相关数据如下表。
Z(g) ΔH,达到平衡。相关数据如下表。
容器 | 温度/K | 物质的起始浓度/ mol·L-1 | 物质的平衡浓度/ mol·L-1 | ||
c(X) | c(Y) | c(Z) | c(Z) | ||
I | 400 | 0.20 | 0.10 | 0 | 0.080 |
II | 400 | 0.40 | 0.20 | 0 | a |
III | 500 | 0.20 | 0.10 | 0 | 0.025 |
下列说法不正确的是
A. 平衡时,X的转化率:II>I
B. 平衡常数:K(II)>K(I)
C. 达到平衡所需时间:III<I
D. 反应的ΔH<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,不正确的是
A. 固体表面水膜的酸性很弱或呈中性,发生吸氧腐蚀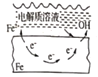
B. 钢铁表面水膜的酸性较强,发生析氢腐蚀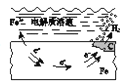
C. 将锌板换成铜板对钢闸门保护效果更好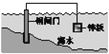
D. 钢闸门作为阴极而受到保护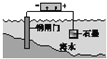
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应2SO2(g)+O2(g)![]() 2SO3(g) △H<0,下列措施中,既能使正反应速率增大又能使平衡正向移动的是
2SO3(g) △H<0,下列措施中,既能使正反应速率增大又能使平衡正向移动的是
A.通入大量的SO2B.增大容积的体积
C.移去部分SO3D.升高体系的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿斯巴甜(Aspartame,结构简式如图)具有清爽的甜味,甜度约为蔗糖的200倍.下列关于阿斯巴甜的错误说法是
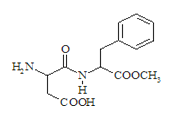
A.在一定条件下能发生取代反应、加成反应
B.酸性条件下的水解产物中有两种氨基酸
C.一定条件下既能与酸反应、又能与碱反应
D.分子式为C14H18N2O3,属于蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3可消除NO的污染,反应方程式为:6NO+4NH3→5N2+6H2O.现有NO与NH3的混合物1mol充分反应,若还原产物比氧化产物多1.4g.则下列判断中正确的是( )
A.产生氮气为5.6 L
B.有0.3 mol NO被还原
C.生成氧化产物2.8 g
D.原混合物中NO与NH3的物质的量之比可能为3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. X、Y、Z、W为按原子序数由小到大排列的四种短周期元素。X可分别与Y、W 形成X2Y、X2Y2、XW等共价化合物;Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物。
(1)Z2Y2的电子式为________。
(2)写出化合物ZX与稀硫酸反应的离子方程式_______。
(3)常温下,实验测得0.lmol/L的X2Y2的水溶液的pH=5.4,则X2Y2在水中的电离方程式为_______。
II.利用电解饱和ZW溶液及CuCl 溶液合成1, 2—二氯乙烷的实验装置如图所示。

(4)离子交换膜X为_________(选填“阴”或“阳”)离子交换膜;该装置总反应的化学方程式为_______。
(5)要生成1 mol ClCH2CH2Cl,则释放出的H2在标准状况下的体积为________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,H3AsO4溶液中各含砷粒子分布分数(平衡时该粒子的浓度与各含砷粒子浓度之和的比)与pH的关系如右图所示。下列说法正确的是
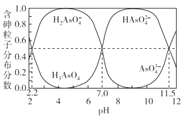
A. H3AsO4的第一步电离常数Ka1>0.01
B. pH=7.0时.溶液中c(AsO43-)=c(H3AsO4)=0
C. 0.1mol·L-1H3AsO4溶液的pH<2
D. pH=12时,c(H+)=3c(AsO43-)+2c(HAsO42-)+c(H2AsO4-)+c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com