
����Ŀ���Ѷ�����һ����Ҫ���л���Ԫ�ᣬ��Ҫ������������66��ά������66��֬����ʵ�����п�ͨ����������������Ӧ���Ʊ�����Ӧԭ����3 ![]() +8HNO3
+8HNO3 ![]() 3HOOC��CH2��4COOH+8NO��+7H2O����Ӧװ�ã����ּг�װ�ú���Դ��ʡ�ԣ���ͼ��ʾ��
3HOOC��CH2��4COOH+8NO��+7H2O����Ӧװ�ã����ּг�װ�ú���Դ��ʡ�ԣ���ͼ��ʾ�� 
ʵ�鲽�裺
����60mL������ƿ�м���16.0mL50%���ᣨ��=1.31gcm��3��������0.01g��ƫ����泥�ƿ�����ڰ�װ�綯������������ڷֱ�װ����a��b��������b�μ�5.3mL����������=0.9624gcm��3�����������ò��������������a��һ��������������װ�ã��ô���Һ��������Һ��
�����Ƚ�ƿ��Һ����ȵ�50�����ң����������������뻷������ʹ��Ӧ������״̬���μ���Ϻ���90������ˮԡ����20���ӣ�����Ӧ��ϣ�
����ȵ���ƿ�л��Һ���ձ��ڣ��ձ����ڱ�ˮԡ�У�������ȴ��������Ʒ�����ˣ���������ˮϴ�ӳ������������أ�
�����ֲ�Ʒ��ˮ�н����ؽᾧ������
��ش��������⣺
��1������a�������� �� ����b��ʹ��ǰӦ ��
��2��ƫ����淋������� ��
��3����Ӧ��ɺ��ȵ�����ӦҺ��Ŀ���� ��
��4����ʵ���м���������۲���Ϊ ��
��5���ô���Һ����β��ʱ��������ػ�ѧ��ӦΪ�� 2NO2+NaCO3�TNaNO2+NaNO3+CO2 ��
NO+NO2+Na2CO3�T2NaNO2+CO2 ��
����1000g��������Ϊ21.2%�Ĵ�������Һ����β����ÿ����22.4L����״���£�CO2ʱ������Һ����������44g��������Һ��NaNO2��NaNO3�����ʵ���֮��Ϊ
���𰸡�
��1�������ܣ�����Ƿ�©ˮ
��2������
��3����Ӧ�ս�����ʱ��ӦҺ������������ȴ�����£��������ᾧ������������������ɲ�Ʒ����ʧ
��4��7.4
��5��5��3
���������⣺��1����ʵ��װ��ͼ��֪��ͼ������a�������������ܣ����в�����������ʹ��ǰ�ü�©��bΪ��Һ©������ʹ��ǰҪ����Ƿ�©ˮ�����Դ��ǣ������ܣ�����Ƿ�©ˮ����2����֪��Ӧԭ��Ϊ��3 ![]() +8HNO3
+8HNO3 ![]() 3HOOC��CH2��4COOH+8NO��+7H2O���÷�Ӧ������ƫ����鱗��μӷ�Ӧ�����������������Դ��ǣ���������3����Ӧ��ɺ�Ҫ���ȵ�����ӦҺ����Ϊ�����᳣����Ϊ���壬�¶Ƚϵ�ʱ�����Һ����������Ӧ�ս�����ʱ��Һ���¶Ƚϸߣ���ӦҺ������������ȴ�����£��������ᾧ������������������ɲ�Ʒ����ʧ�����Դ��ǣ���Ӧ�ս�����ʱ��ӦҺ������������ȴ�����£��������ᾧ������������������ɲ�Ʒ����ʧ����4����������������Ϊ��16.0mL��1.31g/mL��50%=10.5g��������������Ϊ��5.3mL��0.9624g/mL=5.1g����Ӧ����ʽΪ��3
3HOOC��CH2��4COOH+8NO��+7H2O���÷�Ӧ������ƫ����鱗��μӷ�Ӧ�����������������Դ��ǣ���������3����Ӧ��ɺ�Ҫ���ȵ�����ӦҺ����Ϊ�����᳣����Ϊ���壬�¶Ƚϵ�ʱ�����Һ����������Ӧ�ս�����ʱ��Һ���¶Ƚϸߣ���ӦҺ������������ȴ�����£��������ᾧ������������������ɲ�Ʒ����ʧ�����Դ��ǣ���Ӧ�ս�����ʱ��ӦҺ������������ȴ�����£��������ᾧ������������������ɲ�Ʒ����ʧ����4����������������Ϊ��16.0mL��1.31g/mL��50%=10.5g��������������Ϊ��5.3mL��0.9624g/mL=5.1g����Ӧ����ʽΪ��3 ![]() +8HNO3
+8HNO3 ![]() 3HOOC��CH2��4COOH+8NO��+7H2O 3��100 8��63 3��146
3HOOC��CH2��4COOH+8NO��+7H2O 3��100 8��63 3��146
5.1g xg mg
��x= ![]() =8.568g�������������
=8.568g�������������
�����ɵļ�����Ϊmg��
��m= ![]() =7.446��7.4g��
=7.446��7.4g��
���Դ��ǣ�7.4����5����NaNO2�����ʵ���Ϊxmol��NaNO3�����ʵ���Ϊymol��
2NO2+NaCO3�TNaNO2+NaNO3+CO2
2y y y y
NO+NO2 +Na2CO3 �T2NaNO2 +CO2![]()
![]() x��y
x��y ![]()
��֪����22.4L����״���£�CO2 �� ��x+ ![]() =
= ![]()
��Һ���ӵ�����Ϊ��2y46+ ![]() 30+
30+ ![]() 46��
46�� ![]() 44=44��
44=44��
������������ʽ��ã�x��y=5��3��
��������Һ��NaNO2��NaNO3�����ʵ���֮��Ϊ5��3�����Դ��ǣ�5��3��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ش������⣺
��1��C��N��O����Ԫ�صĵ�һ�������ɴ�С��˳���� ��
��2��C��Si��N�ĵ縺���ɴ�С��˳���� ��
��3��������ˮ��Һ�д��ڵ�������֣�
��4�����������仯�����ںϽ�����Լ������ȷ���Ӧ�ù㷺��Ni�Ļ�̬ԭ������������ͬ�ĵ��ӣ��ܶ�����л�����Ni���¿���H2�����ӳɷ�Ӧ�����CH2=CH2����HC��CH���� ![]() ����HCHO������̼ԭ�Ӳ�ȡsp2�ӻ��ķ������������ʱ�ţ���HCHO���ӵ����幹��Ϊ
����HCHO������̼ԭ�Ӳ�ȡsp2�ӻ��ķ������������ʱ�ţ���HCHO���ӵ����幹��Ϊ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾΪ4��̼ԭ�����ϵķ�ʽ��С���ʾ̼ԭ�ӣ�С����ʾ��ѧ��������̼ԭ��������Ļ�ѧ��������ԭ�ӽ�ϡ�
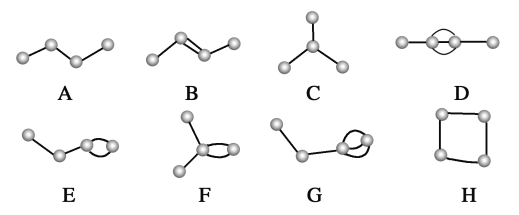
(1)ͼ��������������_____________(����ĸ����ͬ)��
(2)������ͼ��ʾ���л��������У�̼ԭ����̼ԭ��֮�䲻�������γɵ������������γ�_____________��_____________�����������γ�_____________���������γ�̼����
(3)����˫������_____________��������������_____________��
(4)ͼ�л�Ϊͬ���칹����ǣ�A��________��B��________��D��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1967��������������������ĸ���䶨��Ϊ��������仯����ӵ�����ֻ��������ϵĽ���Ԫ�أ���Cu9Al4��Cu5Zn8�ȣ��ش��������⣺ 
��1��ij�ֽ�������������Է��ԣ�ԭ������ά�ռ�����������������У��ý������������������ �塱�Ǿ��塱����
��2����̬ͭԭ������δ�ɶԵ��ӣ�����ͭ���ӵĵ����Ų�ʽΪ �� ��CuSO4��Һ �е��������ˮ���γ���������ɫΪ ��
��3��ͭ������±�أ�SCN��2��Ӧ����Cu��SCN��2 �� 1mol��SCN��2�����к��У�������ĿΪ����±�أ�SCN��2��Ӧ���������֣������������ᣨH��S��C��N���ķе�����������ᣨH��N=C=S���ķе㣬��ԭ���� ��
��4��ZnS�ľ����ṹ��ͼ1��ʾ����ZnS�����У�S2������λ��Ϊ ��
��5��ͭ����γɵĽ���������ṹ��ͼ2���侧���߳�Ϊa nm���ý�����������ܶ�Ϊ���ú���a��NA �Ĵ���ʽ��ʾ��gcm��3 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������������ϢϢ��ء������й�˵������ȷ����
A.С�մ����������θ�����
B.��ԭ���ۿ�����ʳƷ���ڵĿ�������
C.�����Ѵ���������ȡ�����صĹ����а�����ȡ����
D.ī�Ӻ���������ʹ�õ�̫���ܵ�أ�����Ҫ�ɷ�Ϊ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����ĩ������Na2O��Na2O2��Na2CO3��NaHCO3��NaCl�е�һ�ֻ�����ɡ����÷�ĩ�����������ᷴӦ������X�ݳ���Xͨ��������NaOH��Һ�������С(ͬ�¡�ͬѹ�²ⶨ)��ʣ�����塣����ԭ����Ϸ�ĩ�ڿ������þƾ��Ƽ��ȣ�Ҳ������ų�����ʣ��������������ԭ��Ϸ�ĩ�������������ж���ȷ����( )
�ٷ�ĩ��һ����Na2O��Na2O2��NaHCO3
�ڷ�ĩ��һ��������Na2CO3��NaCl
�۷�ĩ��һ��������Na2O��NaCl
�����϶���ĩ���Ƿ���Na2CO3��NaCl
A���٢� B���ڢ� C���ۢ� D���٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ũ���ᷴӦ�������ų���2MnO2+2H2SO4��2MnSO4+O2+2H2O��������������� �ǣ�������
A.Ũ������������
B.�������ǻ�ԭ����
C.�������̼������������ǻ�ԭ��
D.��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڹ�̬��������������У����¹����H2O��CO2��������Ʊ�H2��CO��һ���µ���Դ���÷�ʽ������ԭ����ͼ��ʾ������˵������ȷ���ǣ� �� 
A.X�ǵ�Դ�ĸ���
B.�����ķ�Ӧʽ�ǣ�H2O+2e���TH2+O2�� �� CO2+2e���TCO+O2��
C.�ܷ�Ӧ�ɱ�ʾΪ��H2O+CO2 ![]() H2+CO+O2
H2+CO+O2
D.�������������ɵ���������ʵ���֮����1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������������ء�����˵����ȷ����
A.ͨ����֬��������������ˮ�ⷴӦ�����Ʊ�����
B.���е������������ڶ���ˮ����Ϊ�����ṩ����
C.�������ʿ�������ױƷ�е�����Ҳ������ˮ�ܼ�
D.��ϩ����ʹˮ�����죬�˹��̽������������仯
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com