
【题目】某固体可能含有NH4+、Cu2+、Na+、Cl-、CO32-、SO42-,中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离);
⑴一份固体溶于水得无色透明溶液,加入足量BaCl2溶液,得沉淀4.66g,在沉淀中加入过量稀盐酸,沉淀没变化.
⑵另一份固体与过量NaOH固体混合后充分加热,产生使湿润的红色石蕊试纸变蓝色的气体0.672L(标准状况).
下列说法正确的是( )
A.该固体中一定含有NH4+、SO42-、Na+B.该固体中一定没有Cu2+、Cl-
C.该固体中只含有NH4+、CO32-、SO42-、Cl-D.根据以上实验,无法确定该固体中有Na+
【答案】A
【解析】
(1)一份固体溶于水得无色透明溶液,说明不含Cu2+,加入足量BaCl2溶液,得沉淀4.46g,在沉淀中加入过量稀盐酸,沉淀没变化,说明沉淀不溶于盐酸,一定含有SO42-,一定不含CO32-,且n(SO42-)=n(BaSO4)=![]() =0.02mol;
=0.02mol;
(2)另一份固体与过量NaOH固体混合后充分加热,产生使湿润的红色石蕊试纸变蓝色的气体,该气体为氨气,0.672L即0.03mol(标准状况),所以含有铵根离子0.03mol,以此解答该题。
A.根据分析n(SO42-)=0.02mol,n(NH4+)=0.03mol阴离子所带电荷大于阳离子所带电荷,由电荷守恒可知应还存在Na+,故A正确;
B.因Na+的量不能确定,则不能确定是否含有Cl-,故B错误;
C.由以上分析可知不存在CO32-,Cl-不能确定,故C错误;
D.由A分析可知一定存在Na+,故D错误;
故答案为A。


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
【题目】为测定含镁3%~5%的铝镁合金中镁的质量分数,设计了2种实验方案,说法不正确的是
方案一:镁铝合金加入足量的氢氧化钠溶液中充分反应后过滤,测定剩余固体质量;
方案二:称量m g铝镁合金粉末,放在图中惰性电热板上,通电使其充分灼烧。测得固体质量增重。

A. 方案一中若称取5.4 g合金粉末样品,投入V mL 2.0 mol/L NaOH溶液中反应,则V≥100 mL
B. 方案一中测定剩余固体质量时,过滤后未洗涤固体就干燥、称量,则镁的质量分数偏高
C. 方案二中欲计算镁的质量分数,实验中还需测定灼烧后固体的质量
D. 方案二中若用空气代替O2进行实验,则测定结果偏高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,将![]() 通入水中发生反应,转移的电子数为
通入水中发生反应,转移的电子数为![]()
B.常温常压下,![]() 与
与![]() 混合物含有的氧原子数为
混合物含有的氧原子数为![]()
C.将![]() 与过量
与过量![]() 反应转移的电子数为
反应转移的电子数为![]()
D.标准状况下,![]() 中所含电子数为
中所含电子数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某课外活动小组设计的用化学电池使LED灯发光的装置。下列说法错误的是( )

A.铜表面有气泡生成B.装置中存在“化学能→电能→光能”的转换
C.Zn为负极,Cu为正极D.正极反应为:Zn-2e-=Zn2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语或描述中,不正确的有
①F-的结构示意图:![]()
②氢氧根的电子式:![]()
③HClO的结构式:H—Cl—O
④SO3的水溶液能导电,说明SO3是电解质
⑤NaHSO3在水中的电离方程式:NaHSO3=Na++H++SO32-
⑥同素异形体间的转化和同位素间的转化都是化学变化
A. 1项 B. 2项 C. 5项 D. 6项
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢、氮、氧、铁、铜等元素及其化合物在人们的日常生活中有着广泛的用途。回答下列问题:
(1)写出基态铜原子的价电子排布式__________________
(2)和铜在同一周期中,基态原子未成对电子数为2的元素共有______种。
(3)NH4HF2中HF2-的结构为F-H.......F-,则NH4HF2中含有的化学键有_________
(A)离子键 (B)共价键 (C)金属键 (D)氢键 (E)配位键
(4)写出与NH4+互为等电子体的一种分子的化学式________;
(5)CH3OH分子中C原子的杂化方式为_________,键角:H-C-H_______H-O-C。(填“<”、“>”、“=”)
(6)Cu与Cl形成某种化合物的晶胞如下图所示,Cu的配位数是________,该晶体的密度为ρg·cm-3,晶胞边长为acm,则阿伏加德罗常数为____________(用含ρ、a的代数式表示)。
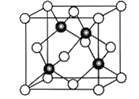
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴酸锂废极片中钴回收的某种工艺流程如下图所示,其中废极片的主要成分为钴酸锂(LiCoO2)和金属铝,最终可得到Co2O3及锂盐。
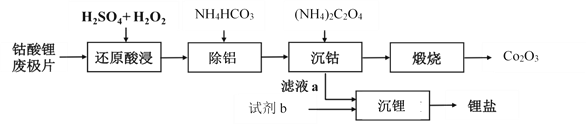
(1) “还原酸浸”过程中,大部分LiCoO2可转化为CoSO4,请将该反应的化学方程式补充完整:2LiCoO2+3H2SO4+□ ![]() □CoSO4+□ +□ + □ 。__________
□CoSO4+□ +□ + □ 。__________
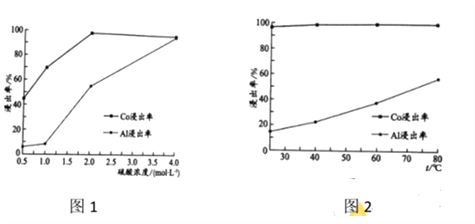
(2) “还原酸浸”过程中,Co、Al浸出率(进入溶液中的某元素质量占固体中该元素总质量的百分数)受硫酸浓度及温度(t)的影响分别如图1和图2所示。工艺流程中所选择的硫酸浓度为2 mol.L-1,温度为80 oC,推测其原因是________。
A. Co的浸出率较高 B. Co和Al浸出的速率较快
C. Al的浸出率较高 D. 双氧水较易分解
(3)加入(NH4)2C2O4后得CoC2O4沉淀。写出CoC2O4沉淀在空气中高温煅烧得到Co2O3的反应的化学方程式:________。
(4)若初始投入钴酸锂废极片的质量为1 kg,煅烧后获得Co2O3的质量为83 g,已知Co的浸出率为90%,则钴酸锂废极片中钴元素的质量分数约为________(小数点后保留两位)。
(5)已知“沉锂”过程中,滤液a中的c(Li+)约为10-1 mol·L-1,部分锂盐的溶解度数据如下表所示。
温度 | Li2SO4 | Li2CO3 |
0 oC | 36.1 g | 1.33 g |
100 oC | 24.0 g | 0.72 g |
结合数据分析,沉锂过程所用的试剂b是________(写化学式),相应的操作方法:向滤液a中加入略过量的试剂b,搅拌,________,洗涤干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,将充满 NO2 和 O2 的试管倒立于水槽中,充分反应后,剩余气体体积为原混合气体体积的![]() ,则原混合气体中 NO2 和O2 的体积之比可能是( )
,则原混合气体中 NO2 和O2 的体积之比可能是( )
①8∶1 ②7∶3 ③7∶1 ④4∶1
A.①②B.①③
C.②③D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意解答
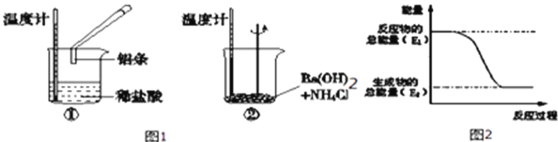
(1)某实验小组同学进行如下实验,以检验化学反应中的能量变化,据实验现象判断①是_________热反应,②是_________热反应.反应过程___(填“①”或“②”)的能量变化可用图2表示.
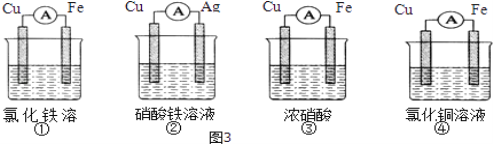
(2)为了验证Fe3+与Cu2+氧化性强弱,下列装置能达到实验目的是_________(填序号).
(3)将H2设计成燃料电池,其利用率更高,装置如图4所示(a、b为多孔碳棒),负极通入_______其电极反应式为________________电池总反应为______________
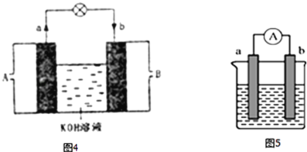

(4)如图5是某化学兴趣小组探究不同条件下化学能转变为电能的装置.
①若两个电极分别是锌、铜,电解质溶液是稀硫酸,正极的电极反应式___________;若电极保持不变,将电解质溶液换成硫酸铜,请将该电池设计为双液原电池画入图6中___________;
②当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠时,该原电池的负极为_______;该原电池的电池总反应为_____________________________.
③若电池的总反应是2FeCl3+Fe![]() 3FeCl2,则可以作正极材料的是________,正极反应式是__________若该电池反应消耗了0.1mol FeCl3,则转移电子的数目为_____。
3FeCl2,则可以作正极材料的是________,正极反应式是__________若该电池反应消耗了0.1mol FeCl3,则转移电子的数目为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com