
【题目】向硫酸铜水溶液中逐滴加入氨水,先形成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液,再向溶液中加入乙醇有深蓝色晶体(化学式为[Cu(NH3)4]SO4·H2O)析出。
(1)写出上述实验前两步反应的离子方程式__________,____________。
(2)铜元素基态原子的电子排布式为_________________,铜单质晶体中的原则堆积模型属于_________堆积(填堆积模型名称)。
(3)在上述深蓝色晶体所含的非金属元素中,电负性最大的是_________(填元素符号),第一电离能最大的是_________(填元素符号)。该晶体中的阴离子的立体构型是_________,阴离子的中心原子的杂化方式为_________。
(4)氨的沸点_________(填“高于”或“低于”)膦(PH2),原因是_____________。

(5)Cu的一种氯化物晶胞结构如图所示,该氯化物的化学式是______________。若该晶体的密度为pg·cm-3,以NA表示阿伏伽德罗常数,则该晶胞的边长为a=_____________nm。
【答案】 Cu2++2NH3·H2O=Cu(OH)2↓+2NH4+ Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH- 1s22s22p63s23p63d104s1或 3d104s1 面心立方最密堆积 O N 正四面体 sp3 高于 因氨分子间存在氢键,膦分子间不存在氢键而只存在范德华力,故氨的沸点高于膦的沸点 CuCl 
【解析】(1)氨水和硫酸铜反应生成氢氧化铜蓝色沉淀,当氨水过量时,氨水和氢氧化铜反应生成可溶性的铜氨络合物,所以难溶物溶解得到深蓝色的透明溶液,涉及的离子方程式为:Cu2++2NH3H2O=Cu(OH)2↓+2NH4+、Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-; 故答案为:Cu2++2NH3H2O=Cu(OH)2↓+2NH4+、Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-;
(2)铜是29号元素,基态原子的电子排布式为1s22s22p63s23p63d104s1,铜单质晶体中的原子堆积模型属于面心立方最密堆积,故答案为:1s22s22p63s23p63d104s1;面心立方最密堆积;
(3)上述深蓝色晶体所含的非金属元素有N、H、O、S,其中O元素的非金属性最强,电负性最大,N的2p为半充满状态,较为稳定,第一电离能最大。[Cu(NH3)4]2+形成4个配位键,具有对称的空间构型,中心原子的杂化方式为sp3,空间结构为正四面体,故答案为:O;N;正四面体;sp3;
(4)氨分子间能够形成氢键,沸点高于膦(PH3),故答案为:高于;因氨分子间存在氢键,膦分子间不存在氢键而只存在范德华力,故氨的沸点高于膦的沸点。
(5)晶胞中Cu位于顶点、面心,晶胞中Cu原子为8×![]() +6×
+6×![]() =4,Cl原子位于晶胞内部,晶胞中Cl原子数目为4,故该晶体化学式为CuCl;1mol晶胞的质量为4×
=4,Cl原子位于晶胞内部,晶胞中Cl原子数目为4,故该晶体化学式为CuCl;1mol晶胞的质量为4×![]() g,1mol晶胞的体积为a3 cm3,该晶体的密度为ρg·cm-3,因此a3 cm3×ρg·cm-3=4×
g,1mol晶胞的体积为a3 cm3,该晶体的密度为ρg·cm-3,因此a3 cm3×ρg·cm-3=4×![]() g,解得a=
g,解得a= cm=
cm= ×107 nm,故答案为:CuCl;
×107 nm,故答案为:CuCl;  ×107。
×107。
【题型】填空题
【结束】
12
【题目】有机物J是我国自主成功研发的一类新药,它属于酯类,分子中除苯环外还含有一个五元环。合成J的一种路线如下:

已知:
回答下列问题:
(1)A→B的反应类型为_______________。C中的官能团名称为_____________________。
(2)D生成E的化学方程式为__________________________________。
(3)J的结构简式是_____________________。在一定条件下,H 自身缩聚生成高分子化合物的化学方程式为_______________________________________。
(4) 根据C![]()
![]() X,x的分子式为_____________________。X有多种同分异构体,其中满足下列条件的同分异构体共有___________种(已知:碳碳叁键或碳碳双键不能与羟基直接相连)。
X,x的分子式为_____________________。X有多种同分异构体,其中满足下列条件的同分异构体共有___________种(已知:碳碳叁键或碳碳双键不能与羟基直接相连)。
A.除苯环外无其他环,且无-O-O-键
B.能与FeCl3溶液发生显色反应
C.苯环上一氯代物只有两种
(5)利用题中信息和所学知识,写出以乙烯和甲苯为原料,合成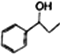 的路线流程图(其它试剂自选):__________________________________。
的路线流程图(其它试剂自选):__________________________________。
【答案】 取代反应 醛基、溴原子 


![]() 4
4 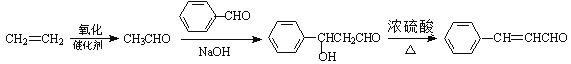
【解析】试题分析: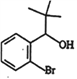
![]() H,根据
H,根据 可知H是
可知H是
,H脱水生成J,J属于酯类,除苯环外还含有一个五元环,所以J是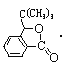 ;根据
;根据 中溴原子的位置,
中溴原子的位置, 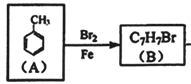 ,则B是
,则B是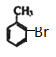 、C是
、C是![]() ;E是
;E是![]() 、F是
、F是![]() 。
。
解析:根据以上分析,(1)![]() 与液溴反应生成
与液溴反应生成 的反应类型为取代反应。
的反应类型为取代反应。![]() 中的官能团名称为醛基、溴原子。
中的官能团名称为醛基、溴原子。
(2)![]() 与HBr发生加成反应生成
与HBr发生加成反应生成![]() 的化学方程式为
的化学方程式为 ;
;
(3)J的结构简式是 ;在一定条件下,H是
;在一定条件下,H是 ,自身缩聚生成高分子化合物的化学方程式为
,自身缩聚生成高分子化合物的化学方程式为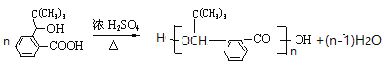 ;
;
(4)根据![]()
![]() X,x是
X,x是 ,分子式为
,分子式为![]() 。X有多种同分异构体,其中A.除苯环外无其他环,且无-O-O-键; B.能与FeCl3溶液发生显色反应,说明含有酚羟基; C.苯环上一氯代物只有两种,满足条件的同分异构体共有
。X有多种同分异构体,其中A.除苯环外无其他环,且无-O-O-键; B.能与FeCl3溶液发生显色反应,说明含有酚羟基; C.苯环上一氯代物只有两种,满足条件的同分异构体共有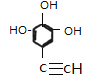 、
、 、
、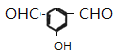 、
、![]() 共4种。
共4种。
(5)根据题中信息,甲苯![]()
![]()
![]() ;乙烯与溴化氢发生加成反应生成溴乙烷,溴乙烷在
;乙烯与溴化氢发生加成反应生成溴乙烷,溴乙烷在![]() 条件下生成
条件下生成![]() ,
,![]() 与
与![]() 反应生成
反应生成 ;合成路线流程图:
;合成路线流程图: ;
;


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 新制的氯水在光照条件下颜色变浅
B. 合成氨工业中使用铁触媒作催化剂
C. 红棕色的NO2气体,加压后颜色先变深后变浅
D. 工业生产硫酸的过程中,通入过量的空气以提高二氧化硫的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某溶液中存在较多的H+、SO42+ 、NO3-,则溶液中还可能大量存在的离子组成( )
A. Al3+、CH3COO-、Cl- B. Na+、NH4+、Cl-
C. Mg2+、Cl-、Fe2+ D. Mg2+、Ba2+、Br-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】糯米中含大量淀粉,下列有关说法正确的是( )
A.淀粉能与银氨溶液反应产生银镜
B.淀粉是否水解完全可以用碘水来检验
C.淀粉在碱性条件下能发生水解生成葡萄糖
D.糖尿病病人不宜吃粽子,因为糯米中含大量的葡萄糖会使血糖升高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.蒸发是为了除去溶剂得到晶体,蒸馏是为了得到液体成分
B.金属氧化物一定是碱性氧化物
C.酸性氧化物一定是非金属氧化物
D.物质的量是七个基本物理量之一,是用于描述一定粒子数目的物理量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在溶液中能大量共存,加入强碱溶液有沉淀析出,加入强酸有气体放出的是( )
A.Na+、Cu2+、Cl﹣、SO42﹣
B.Fe3+、K+、SO42﹣、NO3﹣
C.K+、Al3+、Cl﹣、CO32﹣
D.Na+、Ca2+、Cl﹣、HCO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中各微粒的浓度关系正确的是
A. 0.2 mol·L-1的Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3)
B. pH相等的NaF与CH3COOK溶液:[c(Na+)-c(F-)]>[c(K+)-c(CH3COO-)]
C. pH相等的①NH4Cl ②(NH4)2SO4 ③NH4HSO4溶液,NH4+大小顺序为①=②>③
D. 0.2 mol·L-1HCl与0.1 mol·L-1NaAlO2溶液等体积混合:c(Cl-)>c(Na+)>c(H+)>c(Al3+)>c(OH-)
【答案】C
【解析】根据质子守恒,0.2 mol·L-1的Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3),故A错误;根据电荷守恒,NaF溶液中[c(Na+)-c(F-)]= [c(OH-)-c(H+)],CH3COOK溶液[c(K+)-c(CH3COO-)]= [c(OH-)-c(H+)],PH相等,所以[c(Na+)-c(F-)]=[c(K+)-c(CH3COO-)],故B错误; NH4Cl、(NH4)2SO4由于NH4+水解溶液呈酸性,pH相等,所以NH4+浓度相等,NH4HSO4溶液主要由于NH4HSO4电离呈酸性,所以NH4HSO4溶液中NH4+浓度最小,故C正确;0.2 mol·L-1HCl与0.1 mol·L-1NaAlO2溶液等体积混,完全反应生成氯化钠、氯化铝、氢氧化铝,所以c(Cl-)>c(Na+)>c(Al3+)>c(H+)>c(OH-),故D错误。
【题型】单选题
【结束】
8
【题目】直接排放含SO2的烟气会形成酸雨,危害环境。某化学兴趣小组进行如下有关SO2性质和含量测定的探究活动。

(1)装置A中仪器a的名称为________。写出A中发生反应的离子方程式_________________________。若利用装置A中产生的气体证明+4价的硫元素具有氧化性,试用化学方程式表示该实验方案的反应原理_______________________________________。
(2)选用图中的装置和药品探究亚硫酸与次氯酸的酸性强弱:
①甲同学认为按A→C→F→尾气处理顺序连接装置可以证明亚硫酸和次氯酸的酸性强弱,乙同学认为该方案不合理,其理由是__________________________________。
②丙同学设计的合理实验方案为:按照A→C→______→F→尾气处理(填字母)顺序连接装置。证明亚硫酸的酸性强于次氯酸的酸性的实验现象是____________________________。
③其中裝置C的作用是____________________________。
(3)为了测定装置A残液中SO2的含量,量取10.00mL残液于圆底烧瓶中,加热使SO2全部蒸出,用20.00mL0.0500mol·L-1的KMnO4溶液吸收。充分反应后,再用0.2000 mol·L-1的KI标准溶液滴定过量的KMnO4,消耗KI溶液20.00mL。
已知:5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+ 10I-+2MnO4-+16H+=2Mn2++5I2+8H2O
①残液中SO2的含量为____g·L-1。
②若滴定前读数时平视,滴定终点读数时俯视则测定结果________(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于胶体和溶液的本质区别,下列叙述中正确的( )
A. 溶液呈电中性,胶体带电荷
B. 溶液中通过一束光线出现明显光路,胶体中通过一束光线没有特殊现象
C. 溶液中溶质粒子能通过滤纸,胶体中分散质粒子不能通过滤纸
D. 溶液与胶体的本质区别在于分散质微粒直径大小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是

A. 加入Na2SO4可使溶液由a点变到b点
B. 通过蒸发可以使溶液由d点变到c点
C. d点无BaSO4沉淀生成
D. a点对应的Ksp大于c点对应的Ksp
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com