
【题目】下列金属中,通常用热分解法冶炼的是
A.钠B.铁C.铝D.银
 天天向上一本好卷系列答案
天天向上一本好卷系列答案科目:高中化学 来源: 题型:
【题目】298 K时,在20.0 mL 0.10 mol·L-1氨水中滴入0.10 mol·L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10 mol·L-1氨水的电离度为1.32%,下列有关叙述不正确的是( )

A. 该滴定过程应选择甲基橙作为指示剂
B. M点对应的盐酸体积小于20.0 mL
C. M点: c(NH4+)+ c(NH3·H2O) =c(Cl-)
D. M点处的溶液中c(NH4+)=c(Cl-)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)2·6H2O的流程如下:

已知:
①卤块的主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质
②四种化合物的溶解度(S)随温度(T)变化的曲线如图所示。

回答下列问题:
(1)过滤所需要的主要玻璃仪器有______________________。
(2)加入BaCl2溶液的目的是______________________,加MgO后过滤所得滤渣的主要成分为___________(写化学式)
(3)加入NaClO3饱和溶液后发生反应的化学方程式为_______________________。再进一步制取Mg(ClO3)2·6H2O的实验步骤依次为:①蒸发结晶,②_______________,③将滤液冷却结晶,④过滤、洗涤。
(4)产品中Mg(ClO3)2·6H2O含量的测定[已知Mg(ClO3)2·6H2O的摩尔质量为299g·mol-1]。
步骤1:准确称量3.50g产品配成100mL溶液。
步骤2:取出10.00mL溶液于锥形瓶中,加入10.00mL稀硫酸和21.00mL.1.000mol·L-1的FeSO4溶液,微热。
步骤3:冷却至室温,用0.100mol·L-1K2Cr2O7溶液滴定剩余的Fe2+至终点[发生的反应为Cr2O72-+Fe2++H+→Cr3++Fe3++H2O(未配平)]
步骤4:将步骤2、3重复两次,平均消耗K2Cr2O7溶液15.00mL
步骤2中发生反应的离子方程式为_____________________________。该样品中Mg(ClO3)2·6H2O的纯度为___________(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量):
|
|
|
|
根据以上规律判断,下列结论正确的是( )
A. 反应Ⅰ:ΔH>0,P2>P1 B. 反应Ⅱ:ΔH<0,T1<T2
C. 反应Ⅲ:ΔH>0,T2>T1;或ΔH<0,T2<T1 D. 反应Ⅳ:ΔH<0,T2>T1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辉铜矿(Cu2S)可发生反应2Cu2S+2H2SO4+5O2=4CuSO4+2H2O,该反应的还原剂是____,当1 mol O2发生反应时,还原剂所失电子的物质的量为_____mol, 其中被S 元素还原的O2的物质的的量为__________mol 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辣椒素酯是辣椒的活性成分,有降血压和胆固醇的作用。辣椒素酯类化合物的结构可以表示为 (R为烃基)。图27为一种辣椒素酯J的合成路线:
(R为烃基)。图27为一种辣椒素酯J的合成路线:

回答下列问题:
(1)A的名称是___________,G含有的官能团名称是___________。
(2)F和I生成J的反应类型是___________。
(3)E的结构简式为____________________。
(4)C生成D的化学方程式为_________________________________;H生成I的第①步反应的化学方程式为_________________________________。
(5)G的同分异构体中,苯环上的一氯代物只有一种,且核磁共振氢谱显示2组峰的是___________(写结构简式)。
(6)参照上述路线,设计一条以苯甲醛和乙醇为原料(无机试剂任选)合成肉桂酸
(![]() )的合成路线。___________________
)的合成路线。___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究性学习小组对某硫酸亚铁晶体(FeSO4·xH2O)热分解研究,该小组同学称取ag硫酸亚铁晶体样品按图1高温加热,使其完全分解,对所得产物进行探究,并通过称量装置B质量测出x的值。
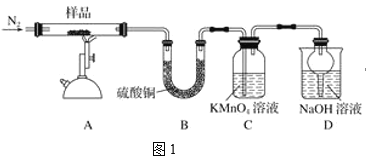

(1)装置B中硫酸铜粉末变蓝,质量增加12.6g,说明产物中有水。
(2)硫酸亚铁晶体完全分解后装置A中还残留红棕色固体氧化铁。
(3)装置C中高锰酸钾溶液褪色,说明产物中存在气体______。
(4)实验中要持续通入氮气,否则测出的x会_____(填“偏大”、“偏小”或“不变”)。
(5)从理论上分析得出硫酸亚铁分解还生成另一物质三氧化硫,写出硫酸亚铁分解的化学方程式________。
(6)某研究所利用SDTQ600热分析仪对硫酸亚铁晶体(FeSO4·xH2O)进行热分解,获得相关数据,绘制成固体质量分解温度的关系如图2,根据图2中有关数据,可计算出FeSO4·xH2O中的x=______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是实验室常用的部分仪器,请回答下列问题:
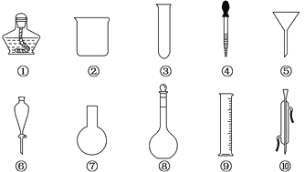
(1)序号为⑧和⑩的仪器的名称分别为______、_______。
(2)在分液操作中,必须用到上述仪器中的__________(填序号)。
(3)能作反应容器且可直接加热的仪器是上述中的__________(填名称)。
(4)配制一定物质的量浓度的溶液时要用到的仪器是____________(填序号)。
(5)如图是温度计、量筒、滴定管的一部分,下述读数(虚线对应刻度)及说法正确的是_________。

A.①是量筒,读数为 2.5 mL B.②是量筒,读数为 2.5 mL
C.③是滴定管,读数为 2.5 mL D.②是温度计,读数为 2.5 ℃
(6)除去氧化钙中的碳酸钙可用什么方法?______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中属于离子化合物是( )
①MgF2 ②Na2O2 ③KOH ④CO2 ⑤NaClO ⑥H2SO4
A. ②③⑤B. ②③④⑤C. ①②③⑤D. ①③⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com