
【题目】(I)为了证明NH3·H2O是弱电解质,甲、乙、丙三人分别选用下列试剂进行实验。0.010mol·L-1氨水、0.1mol·L-1NH4Cl溶液、NH4Cl晶体、酚酞溶液、pH试纸、蒸馏水。
①甲用pH试纸测出0.010mol·L-1氨水的pH为10,则认定NH3·H2O是弱电解质,你认为这一方法________(填“正确”或“不正确”),并说明理由:__________________________________。
②乙取出10mL0.010mol·L-1氨水,用pH试纸测其pH=a,然后用蒸馏水稀释至1000mL,再用pH试纸测其pH=b,若要确认NH3·H2O是弱电解质,则a、b值应满足的关系是_____。
(II)(1)常温下,在pH=6的CH3COOH与CH3COONa的混合溶液中水电离出来的c(OH-)=________。
(2)氨气的水溶液称为氨水,其中存在的主要溶质微粒是NH3·H2O。
已知:a.常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5;
b.CH3COOH+NaHCO3===CH3COONa+CO2↑+H2O。
则CH3COONH4溶液呈________性(填“酸”、“碱”或“中”,下同),NH4HCO3溶液呈________性,NH4HCO3溶液中物质的量浓度最大的离子是________(填化学式)。
【答案】 正确 若是强电解质,则0.010 mol·L-1氨水中c(OH-)应为0.010 mol·L-1,pH=12 a-2<b<a 1×10-8 mol·L-1 中 碱 NH![]()
【解析】(I)①假设现有0.010 mol·L-1氢氧化钠溶液,c(OH-)=0.01 mol·L-1, c(H+)=10-12 mol·L-1,用pH试纸测出pH为12,现用pH试纸测出0.010 mol·L-1氨水的pH为10,所以NH3·H2O是弱电解质,正确;正确答案: 正确; 若是强电解质,则0.010 mol·L-1氨水中c(OH-)应为0.010 mol·L-1,pH=12 。
②假设氨水为强碱,0.010 mol·L-1氨水pH=a,用蒸馏水稀释至100倍,其pH=b=a-2,现确认NH3·H2O是弱电解质,存在电离平衡,所以a-2<b<a ;正确选项:a-2<b<a。
(II) (1)在pH=6的CH3COOH与CH3COONa的混合溶液中,c(H+)=10-6 mol/L,c(OH-)=10-14/10-6= 1×10-8 mol·L-1,正确答案:1×10-8 mol·L-1。
(2)醋酸和NH3·H2O的电离平衡常数均为1.74×10-5,电离能力相同,所以CH3COONH4溶液中两种离子水解能力相同,溶液呈中性;由CH3COOH+NaHCO3===CH3COONa+CO2↑+H2O反应可知醋酸的酸性大于碳酸的酸性,NH4HCO3溶液中,HCO3-水解能力大于NH4+水解能力,所以溶液显碱性,离子浓度最大为NH4+;正确答案:中; 碱 ; NH![]() 。
。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】对氨基水杨酸钠(PAS-Na)是抑制结核杆茵最有效的药物。某同学设计的合成PAS-Na的两种路线如下:
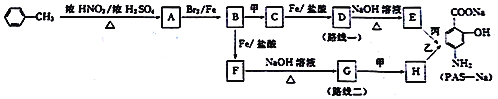
已知以下信息:
①甲、乙、丙为常用的无机试剂;
②![]()
③![]() (苯胺,易被氧化)。
(苯胺,易被氧化)。
回答下列问题:
(1)甲和丙的名称分别是_________________、____________________。
(2)E的结构简式是______________________。
(3)A→B的化学方程式是______________________________________,反应类型是______。
(4)A的同分异构体中氨基(一NH2)与苯环直接相连并且能发生银镜反应的有____种,其中核磁共振氢谱为4组峰且面积之比为2:2:2:1的结构简式为___________。
(5)有同学认为“路线二”不合理,不能制备PAS-Na,你的观点及理由是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列不属于配位化合物的是( )
A.六氟合铝酸钠:Na3[AlF6]
B.氢氧化二氨合银:[Ag(NH3)2]OH
C.六氟合铁酸钾:K3[FeF6]
D.十二水硫酸铝钾:KAl(SO4)2·12H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是向MgCl2、AlCl3混合溶液中,开始滴加试剂A,之后改滴试剂B,所得沉淀ymol 与试剂体积V(mL)间的关系。请回答
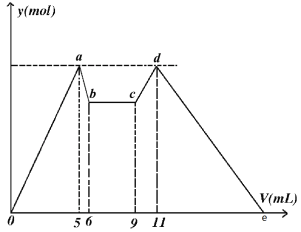
(1)写出c~d段发生反应的离子方程式______________________________________
(2)原溶液中Mg2+、Al3+、Cl的物质的量浓度之比为:_______________________
(3)如果A和B为一元强酸或一元强碱,则c(A):c(B)=_____________________
(4)图中e点处V=_______________(填数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备苯甲醇和苯甲酸的化学原理是
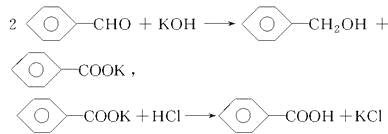
已知苯甲醛易被空气氧化,苯甲醇的沸点为205.3 ℃,苯甲酸的熔点为121.7 ℃,沸点为249 ℃,溶解度为0.34 g;乙醚的沸点为34.8 ℃,难溶于水。制备苯甲醇和苯甲酸的主要过程如下所示:
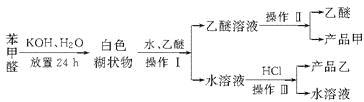
试根据上述信息,判断以下说法错误的是( )
A. 操作Ⅰ是萃取分液
B. 乙醚溶液中所溶解的主要成分是苯甲醇
C. 操作Ⅱ蒸馏所得产品甲是苯甲醇
D. 操作Ⅲ过滤得到产品乙是苯甲酸钾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁苯酞是我国自主研发的一类用于治疗急性缺血性脑卒的新药。合成丁苯酞(J)的一种路线如图所示:
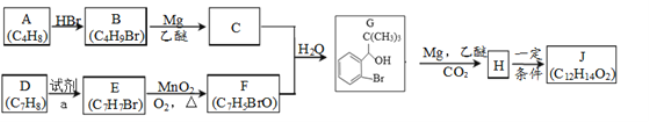
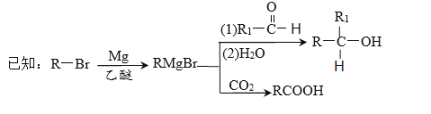
(1)A的名称是_______,E到F的反应类型是___________。
(2)试剂a是________,F中官能团名称是_______。
(3)M组成比F多1个CH2,M的分子式为C8H7BrO,M的同分异构体中:①能发生银镜反应;②含有苯环;③不含甲基。满足上述条件的M的同分异构体共有______种。
(4)J是一种酯,分子中除苯环外还含有一个五元环,J的结构简式为__________。H在一定条件下还能生成高分子化合物K,H生成K的化学方程式为________。
(5)利用题中信息写出以乙醛和苯为原料,合成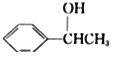 的路线流程图(其它试剂自选)。________。
的路线流程图(其它试剂自选)。________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。回答下列问题:
![]()
(1)为尽量少引入杂质,试剂①应选用___(填标号)。
A.HCl溶液 | B.H2SO4溶液 | C.氨水 | D.NaOH溶液 |
(2)易拉罐溶解过程中主要反应的化学方程式为________。
(3)沉淀B的化学式为________;将少量明矾溶于水,溶液呈弱酸性,其原因是__________。
(4)已知:Kw=1.0×10-14,Al(OH)3![]() AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于_________。
AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是
A. 向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中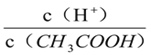 减小
减小
B. 将CH3COONa溶液从20℃升温至30℃,溶液中![]() 增大
增大
C. 向盐酸中加入氨水至中性,溶液中![]() >1
>1
D. 向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中不![]() 变
变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com