
【题目】已知NA是阿伏加德罗常数的值,下列说法错误的是( )
A.标况下,16gCH4含有分子数目为NA个
B.0.1 mol·L1氯化钠溶液含有的Na+数目为0.1NA
C.1 molH2O中含有质子数为10NA个
D.标况下,22.4L空气中含有分子总数为NA个
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】根据碘与氢气反应的热化学方程式 (i)I2(g)+H2(g)![]() 2HI(g) △H=" -" 9.48kJ/mol ,(ii) I2(s)+H2(g)
2HI(g) △H=" -" 9.48kJ/mol ,(ii) I2(s)+H2(g)![]() 2HI(g) △H=" +" 26.48kJ/mol,下列判断正确的是
2HI(g) △H=" +" 26.48kJ/mol,下列判断正确的是
A. 254g I2(g)中通入2g H2(g),反应放热9.48 kJ
B. 1 mol固态碘与1mol气态碘所含的能量相差l7.00 kJ
C. 反应(i)的产物比反应(ii)的产物稳定
D. 反应(i) 拆开1mol I-I键与1mol H-H键需要的总能量小于拆开2mol H-I键需要的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体在体积为2 L的密闭容器中混合,并在一定条件下发生反应:2A(g)+B(g) ![]() xC(g),若经2 s后测得A的物质的量为2.8 mol,C的物质的量浓度为0.6 mol/L。求:
xC(g),若经2 s后测得A的物质的量为2.8 mol,C的物质的量浓度为0.6 mol/L。求:
①2 s内用物质A表示的平均反应速率为________________。
②2 s内用物质B表示的平均反应速率为__________________________。
③2 s时物质B的转化率为______________________。
④x=________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,将仪器A中的浓盐酸滴加到盛有MnO2的烧瓶中,加热后产生的气体依次通过装置B和C,然后再通过加热的石英玻璃管D (放置有铁粉 )。请回答:
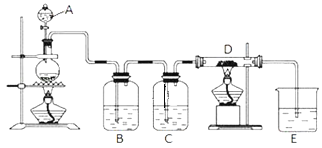
(1)烧瓶中反应的化学方程式是_____;
(2)装置B中盛放液体是_____,气体通过装置B的目的是_____;装置C中盛放的液体是_____,气体通过装置C的目的是_____;
(3)烧杯E中盛放的液体是_____;
(4)资料表明D中产物有以下性质:①受热易升华,冷却后易凝华;②遇H2O (g )剧烈反应;为收集D中产物,在D与E之间,除增加收集装置外,还需要增加_____装置;
(5)当电子转移的数目为6.02×1023个时生成的氯气的物质的量为_____mol,生成的氯气需用0.5mol/L的NaOH溶液_____L完全吸收。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种芳纶纤的拉伸强度比钢丝还高,广泛用作防护材料。其结构片段如下图所示:
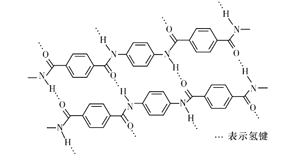
下列关于该高分子的说法不正确的是
A. 芳纶纤维可用作航天、航空、国防等高科技领域的重要基础材料
B. 完全水解产物的单个分子中,含有官能团一COOH或一NH2
C. 氢键对该高分子的性能有影响
D. 结构简式为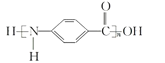
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作规范且能达到目的的是( )
目的 | 操作 | |
A | 配制480mL0.1mol/LCuSO4溶液 | 称取8.0g无水硫酸铜放在烧杯中,加入480mL的蒸馏水,用玻璃棒搅拌。 |
B | 除去氯化钠固体中少量的碳酸钙 | 加水稀盐酸、然后加热蒸干。 |
C | 提取碘水中的碘 | 用量筒量取一定量的碘水,倒入分液漏斗,注入四氯化碳,振荡、静置后分液。 |
D | 除去N2气体中的少量O2 | 点燃,然后将混合气体通入澄清石灰水 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中蕴藏着丰富的资源,某学习小组在实验室模拟从海水提取氯化钠晶体,其实验流程如下:

通过查阅资料可知:粗盐中含有CaCl2、MgCl2、Na2SO4等杂质。该学习小组通过讨论,设计实验在从粗盐精制得到食盐水的过程为:
①取一定量的粗盐溶解;
②向粗盐水中依次加入过量的Na2CO3溶液、加入过量的NaOH、加入过量的BaCl2溶液;
③过滤;
④向滤液中加入适量盐酸。
回答:
(1)溶解时需要的仪器有________。
(2)加入过量的Na2CO3溶液时观察到的现象是________;反应的化学方程式为_______________________________。
(3)实验后,通过进一步反复论证,向老师求证,发现在粗盐精制得到食盐水的设计方案中________(“有”或“没有”)不妥之处,理由是______________________。
(4)该学习小组同学要从食盐水得到氯化钠晶体时,还要进行________、______、过滤。
(5)该学习小组同学用实验得到的晶体配制1mol·L-1的NaCl溶液500mL,在配制过程中,下列操作会引起浓度偏高的是________。
①没有洗涤烧杯和玻璃棒
②容量瓶不干燥,含有少量蒸馏水
③定容时仰视刻度线
④定容时俯视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】填空
(1)1.7gNH3与标况下_________LH2S中的氢原子数相同
(2)在标准状况((___________)℃ 、_____________KPa)下,CO和CO2的混合气体共4.48L,质量为7.2g。则两种气体的物质的量之和为____________mol,该混合气体的平均相对分子质量为___________,其中CO2为___________g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在配合物Fe(SCN)2+中,提供空轨道接受孤对电子的微粒是__,画出配合物离子[Cu(NH3)4]2+中的配位键__.
(2)根据VSEPR模型,H3O+的分子立体结构为__,BCl3的立体结构为__.
(3)按要求写出由第二周期元素为中心原子,通过sp3杂化形成中性分子的化学式(各写一种)
正四面体分子__,三角锥形分子__,V形分子______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com