
取一定量的Fe、Cu的混合物粉末,平均分成五等份,分别向每一份中加入一定量的稀硝酸,假设反应的还原产物只有NO,若实验中生成的NO气体体积及所得剩余固体的质量记录如下(所有体积均在标准状况下测定):
| 实验序号 | 1 | 2 | 3 | 4 | 5 |
| 硝酸溶液体积 | 100 mL | 200 mL | 300 mL | 400 mL | 500 mL |
| 剩余固体的质量 | 17.2 g | 8 .0g | 0 g | 0 g | 0 g |
| 气体体积 | 2.24 L | 4.48 L | 6.72 L | 7.84 L | 7.84 L |
(1)该实验中所用稀硝酸的物质的量浓度为4 .0mol/L;
(2)实验中每次所取混合物粉末中铜的质量为14.4g。(其它合理解法,同样给分)
解析试题分析:根据表中数据分析:实验1后剩余的17.2g固体只可能为Cu或Fe、Cu;实验5中金属完全反应,生成n(NO)=7.84L÷22.4L/mol=0.35mol,反应后溶液含有Fe(NO3)3、Cu(NO3)2和过量HNO3。
(1)假设实验1剩余的17.2g固体全部为Cu,实验1生成NO:n(NO)=2.24L÷22.4L/mol=0.1mol
由于实验2剩余8.0g固体,且比实验1多生成2.24LNO,即多生成0.1molNO则根据实验2多消耗的9.2g铜生成的NO小于0.1mol可知,假设实验1剩余的17.2g固体全部为Cu不成立。
所以实验1后剩余的17.2g固体只可能为Fe、Cu,实验1后溶液中只有Fe(NO3)2(2分)
2n (Fe参与反应)="3n(NO)=" 3×0.1mol
n (Fe参与反应)=0.15mol
每一份固体的质量为0.15mol×56g/mol+17.2g=25.6g
∴c(HNO3)=" 4n(NO)/0.1L=4.0mol/L"
(2)设每一份固体(25.6g)中含有的Fe、Cu物质的量分别为x、y
56x+64y="25.6g"
3x+2y=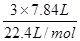
联立求解,解得x=0.2mol、y="0.225mol"
其中含铜:m(Cu)=" 0.225mol×64g/mol=14.4g"
考点:考查了氧化还原的计算。


科目:高中化学 来源: 题型:计算题
(7分)欲测定某生铁(主要成分是铁,还含有少量的碳)的组成,进行了如下实验:称取粉末状样品8.50克,加入某浓度的盐酸100 mL ,充分反应后,收集到标准状况下气体2.24 L ;然后,继续往样品中加入同浓度的盐酸100mL ,充分反应后又收集到标准状况下气体1.12 L 。
试求:(写出具体计算过程)
(1)所取盐酸的物质的量浓度。(2)该生铁样品中碳的质量分数(保留3位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
已知一定量的氢气在氯气中燃烧,所得混合物用100 mL 3.00 mol/L的NaOH溶液(密度为1.12 g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500 mol。
(1)原NaOH溶液的质量分数为_______
(2)所得溶液中Cl-的物质的量为________mol
(3)所用氯气和参加反应的氢气的物质的量之比n(Cl2):n(H2)=______________。
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
将一定量的PH3和H2的混合气体,依次通过两支加热的硬质玻璃管,第一支装有足量的铜屑,第二支装有足量的CuO。第一支玻璃管中因发生反应:2PH3+3Cu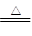 Cu3P2+3H2而增重4.96 g;第二支玻璃管反应后质量减轻了5.76 g。
Cu3P2+3H2而增重4.96 g;第二支玻璃管反应后质量减轻了5.76 g。
试求:原混合气体中PH3与H2的体积比。
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
从100 mL某种待测浓度的 H2SO4溶液中取出25 mL,加入10 mL 0.5 mol·L-1 BaCl2溶液,恰好完全反应。求:
①得到 BaSO4沉淀多少克 ?
②待测 H2SO4溶液中溶质的物质的量浓度是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
某厂平均每天产生约600 m3废氨水(NH3的浓度为153 mg·L-1,密度为1 g·cm—3。
(1)该废氨水中氨的物质的量浓度为 。
(2)对废氨水进行加热蒸发得到NH3,使废氨水中的NH3 的浓度降为17 mg·L-1。忽略蒸发前后废氨水体积变化,则上述体积的废氨水蒸发出来的NH3的物质的量为 。(以下计算结果均保留两位小数)
(3)蒸发得到的NH3可用于制备NO。4NH3+5O2 →4NO+6H2O;(不考虑NO与氧气的反应),设空气中氧气的体积分数为0.20,氮气体积分数为0.80。
①为使NH3恰好完全氧化为NO,氨—空气混合物中氨的体积分数为________。
②氨催化氧化制取NO同时会发生副反应:4NH3+3O2 →2N2+6H2O。将1L NH3混合10L空气后通入反应器,反应完成后,测得混合气体中不含NH3,而O2和N2的物质的量之比为1∶10,试求参加主反应的氨占原料氨的体积百分含量。
(4)废氨水可用于脱除烟气中的SO2。氨水吸收烟气中SO2经氧化后生成(NH4)2SO4和NH4HSO4混合物。现称取不同质量的混合物进行实验,结果如下:
| NaOH 溶液体积/mL | 40.00 | 40.00 | 40.00 |
| 样品质量/g | 7.75 | 15.50 | 23.25 |
| 氨气质量/g | 1.87 | 1.87 | 1.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
欲测定烟雾中的SO2含量,可做下列实验:取100 L该空气(标准状况),通过盛放100 mL过氧化氢(H2O2)水溶液的吸收瓶,使烟雾中的SO2完全吸收,生成硫酸。在反应后的水溶液中加入足量BaCl2溶液,生成白色沉淀,经测定其质量为11.65g(烟雾中其他成分对测定结果无影响)。
(1)写出SO2和H2O2反应的离子方程式。
(2)写出H2SO4与BaCl2反应的离子方程式。
(3)求100 L空气中SO2的体积分数。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
德国著名行业杂志《应用化学》上刊登文章介绍:某中德联合研究小组设计制造了一种“水瓶”,用富勒烯(C60)的球形笼子作“瓶体”,一种磷酸盐作“瓶盖”,恰好可将一个水分子关在里面。下列说法正确的是 ( )
| A.水、双氧水、水玻璃都是纯净物 |
| B.石墨和C60互称为同位素 |
| C.磷酸钙是可溶性强电解质 |
| D.一定条件下石墨转化为C60是化学变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com