
技术的发展与创新永无止境,我国化学家侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如图K39-4:

图K39-4
(1)向沉淀池中要通入CO2和氨气,应选通入______ (填化学式)。原因是_________________________________________。
(2)沉淀池中发生反应的化学方程式是__________________________________。
(3)母液中的溶质主要是________。向母液中通氨气加入细小食盐颗粒,冷却析出副产品,通入氨气的作用是_____________________________________________。
(4)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了________(填上述流程中的编号)的循环,物质X是__________,从沉淀池中提取沉淀的操作是__________ 。
(5)写出煅烧炉中发生反应的化学方程式_____________________________。
(6)这样制得的产品碳酸钠中可能含有的杂质是____________(填化学式),为检验该杂 质的存在,具体操作是__________________________________________。
科目:高中化学 来源: 题型:
为确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验。
(1)若取a g样品,向其中加入足量的NaOH溶液,测得生成的气体(标准状况,下同)体积为b L。
反应的化学方程式是__________________________________;样品中铝的质量是_______________g。
(2)若取a g样品将其点燃,恰好完全反应,该反应的化学方程式是:
_________________________,氧化铁与铝的质量比是_____________。
(3)待(2)中反应产物冷却后,加入足量盐酸,测得生成的气体体积为c L,该气体与(1)中所得气体的体积比c∶b=________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸钠(Na2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强、无二次污染的绿色水处理剂。工业制高铁酸钠的方法有如下两种:
湿法制备的主要离子反应为:2Fe(OH)3 +3ClO—+4OH— =2FeO42— +3Cl— +5H2O ,
干法制备的主要反应方程为:2FeSO4 +6Na2O2 = 2Na2FeO4 +2Na2O +2Na2SO4 +O2↑
则下列有关说法不正确的是( )
A.高铁酸钠中铁显+6价 B.湿法中FeO42—是氧化产物
C.干法中每生成1mol Na2FeO4 转移4mol电子
D.K2FeO4可氧化水中的H2S、NH3,生成的Fe(OH)3胶体还能吸附悬浮杂质
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是( )
(1)纯铁比碳素钢易生锈 (2)用氨水除去试管上的银镜
(3)硅是制作光导纤维和制造太阳能电池的主要原料
(4)可用稀盐酸、碳酸钠溶液、硅酸钠溶液设计实验来验证元素的非金属性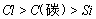
(5)催化剂只能改变反应的活化能,不能改变反应的热效应
(6)用氢氟酸雕刻玻璃是利用氢氟酸能与二氧化硅反应的性质
(7)同主族元素的简单阴离子还原性越强,水解程度越大
(8)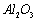 在工业上用于制作耐高温材料,也用于电解法治炼铝
在工业上用于制作耐高温材料,也用于电解法治炼铝
(9)丁达尔效应可用于区别溶液与胶体,云、雾均能产生丁达尔效应
(10)明矾可用于水的消毒、杀菌;碳酸钡可用于钡餐透视
A.(1)(4)(6)(7) B.(4)(6)(9)(10)
C.(3)(5)(6)(8) D.(5)(6)(8)(9)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法正确的是( )
A.将0.2mol/L的NH3·H2O与0.1mol/L的HCl溶液等体积混合后PH >7,
则c(Cl-)>c(NH4+)>c(OH-)>c(H+)
B.已知MgCO3的Ksp=6.82×10-6,则所有含有固体MgCO3的溶液中,都有
C(Mg2+)=C(CO32-) ,且C(Mg2+)·C(CO32-)==6.82×10-6 mol•L—1
C. 0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液等体积混合:
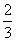 c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
D.用惰性电极电解Na2SO4溶液,阳阴两极产物的物质的量之比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.需要加热方能发生的反应不一定是吸热反应
B.反应是吸热还是放热取决于反应物和生成物所具有的总能量的相对大小
C.测定中和反应的反应热时,酸碱中和之后应读取体系达到的最高温度
D.硫在氧气中燃烧,该反应反应产物的总焓大于反应物的总焓
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解硫酸铜溶液一段时间后,向电解池中加入0.2molCu(OH)2恰好恢复为电解
前的浓度,则电解过程中转移电子的物质的量为
A.0.8 mol B.0.4 mol C.0.2mol D.0.6mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列中心原子的杂化轨道类型和分子几何构型不正确的是
A.PCl3中P原子sp3杂化,为三角锥形 B.BCl3中B原子sp2杂化,为平面三角形
C.CS2中C原子sp杂化,为直线形 D.H2S分子中,S为sp杂化,为直线形
查看答案和解析>>
科目:高中化学 来源: 题型:
10g不纯的碳酸钙样品与足量的稀盐酸反应后共得到4.6g二氧化碳,则不纯的碳酸
钙中所含的一种杂质可能是( )
A. MgCO3 B.Na2C03 C.K2C03 D.ZnC03
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com