
【题目】![]() 水溶液中
水溶液中![]() 、
、![]() 和
和![]() 三种形态的粒子的分布分数
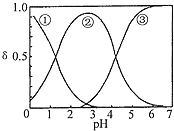
三种形态的粒子的分布分数![]() 随溶液pH变化的关系如图所示
随溶液pH变化的关系如图所示![]() 已知
已知![]() 。下列说法正确的是
。下列说法正确的是
A.曲线![]() 代表的粒子是
代表的粒子是![]()
B.![]() 溶液中:
溶液中:![]()
C.![]() 时,溶液中主要含碳物质浓度大小关系为:
时,溶液中主要含碳物质浓度大小关系为:![]()
D.一定温度下,往![]() 饱和溶液中加入少量
饱和溶液中加入少量![]() 固体,
固体,![]() 将减小,
将减小,![]() 不变
不变
【答案】B
【解析】
![]() 在溶液的电离为:
在溶液的电离为:![]() ,随着pH逐渐增大,平衡右移。在此认识基础上分析图可知:粒子
,随着pH逐渐增大,平衡右移。在此认识基础上分析图可知:粒子![]() 随pH增大而减少,应为
随pH增大而减少,应为![]() ,粒子
,粒子![]() 随pH增大先减少后增多,应为
随pH增大先减少后增多,应为![]() ,粒子③随pH增大而减少,应为
,粒子③随pH增大而减少,应为![]() 。
。
A. ![]() 、
、![]() 和
和![]() 三种粒子中,只有
三种粒子中,只有![]() 随pH增大只减不增,所以曲线①代表的粒子是
随pH增大只减不增,所以曲线①代表的粒子是![]() ,故A错误;
,故A错误;
B. 由图可知![]() 溶液显示酸性,阴离子
溶液显示酸性,阴离子![]() 的电离程度大于其水解程度,所以
的电离程度大于其水解程度,所以![]() ,故B正确;
,故B正确;
C. 直接由图可看出,![]() 时,溶液中主要含碳物质浓度大小关系为:③>②>①,即
时,溶液中主要含碳物质浓度大小关系为:③>②>①,即![]() ,故C错误;
,故C错误;
D. 一定温度下,在![]() 饱和溶液中,存在
饱和溶液中,存在![]() 平衡,加入少量
平衡,加入少量![]() 固体,
固体,![]() 增大,平衡逆向移动,析出
增大,平衡逆向移动,析出![]() 固体,
固体,![]() 将减小,由于
将减小,由于![]() 不变,且溶液饱和,所以最终
不变,且溶液饱和,所以最终![]() 仍比原溶液的大,故D错误;
仍比原溶液的大,故D错误;
答案选B。


 互动英语系列答案
互动英语系列答案科目:高中化学 来源: 题型:
【题目】某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净,再用待测溶液润洗后,注入待测溶液,然后调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;
②将酸式滴定管用蒸馏水洗净,再用标准酸液润洗后,向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;
③用蒸馏水将锥形瓶洗净后,从碱式滴定管中放入20.00mL待测溶液,滴入甲基橙作指示剂,然后用标准盐酸进行滴定。滴定至指示剂刚好变色,且半分钟内颜色不再改变为止,测得所耗盐酸的体积为V1mL;
④重复以上过程,测得所耗盐酸的体积为V2mL。
试回答下列问题:
(1)锥形瓶中溶液的颜色从_________色变为___________色时,停止滴定。
(2)下图中,第②步“调节滴定管的尖嘴部分充满溶液”方法正确的是_________,如果滴定前有气泡,滴定后气泡消失,由此对测定结果形成的影响是___________(填“偏高”、“偏低”或“无影响”)
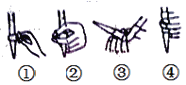
(3)图中是某次滴定时的滴定管中的液面,其读数为__________mL。
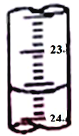
(4)根据下列数据:
滴定次数 | 待测液体积 | 标准盐酸体积(mL) | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 20.00 | 0.20 | 24.10 |
第二次 | 20.00 | 3.00 | 27.10 |
请计算待测烧碱溶液的浓度为____________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对复杂的有机物结构可用“键线式”表示。如苯丙烯酸1—丙烯酯:
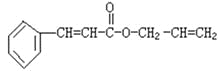 可简化为
可简化为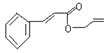 ,杀虫剂“阿乐丹”的结构表示为
,杀虫剂“阿乐丹”的结构表示为 ,若它在稀酸作用下能发生水解反应生成两种有机物,则此两种有机物具有的共同性质是( )
,若它在稀酸作用下能发生水解反应生成两种有机物,则此两种有机物具有的共同性质是( )
A.遇FeCl3溶液均显紫色B.均能发生银镜反应
C.均能与溴水发生反应D.均能与NaHCO3溶液发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
A.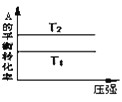 由图可以判断:若
由图可以判断:若![]() ,反应
,反应![]() 的
的![]()
B. 图表示压强对可逆反应
图表示压强对可逆反应![]() 的影响,乙的压强比甲大
的影响,乙的压强比甲大
C.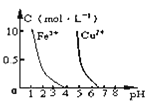 根据图,若除去
根据图,若除去![]() 溶液中的
溶液中的![]() ,可向溶液中加入适量NaOH溶液,调节
,可向溶液中加入适量NaOH溶液,调节![]()
D.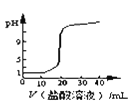 图表示用
图表示用![]() 的盐酸滴定20mL
的盐酸滴定20mL![]() 溶液,pH随加入盐酸体积的变化
溶液,pH随加入盐酸体积的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以高硫铝土矿(主要成分为Al2O3、Fe2O3,还含有少量FeS2)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如图所示,下列叙述错误的是
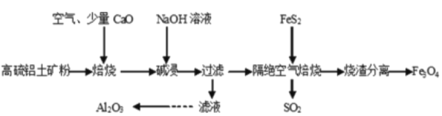
A.加入CaO可以减少SO2的排放同时生成建筑材料CaSO4
B.为了确保得到氧化铝通常向滤液中通入CO2要过量
C.残渣分离可以选择用磁铁将烧渣中的Fe3O4分离出来
D.向滤液中通入过量CO2、过滤、洗涤可制得Al2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向一定体积![]() 醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中
醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中![]()
![]() 与pH的变化关系如图所示,则
与pH的变化关系如图所示,则
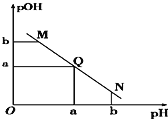
A.M点所示溶液导电能力强于Q点
B.N点所示溶液中![]()
C.M点和N点所示溶液中水的电离程度不相同
D.Q点消耗NaOH溶液的体积小于醋酸溶液的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用NaOH调节0.1molL-1 H2C2O4溶液的pH,假设不同pH下均有![]() ,使用数字传感器测得溶液中各含碳微粒的物质的量浓度随pH的变化曲线如图。下列有关分析正确的是( )
,使用数字传感器测得溶液中各含碳微粒的物质的量浓度随pH的变化曲线如图。下列有关分析正确的是( )
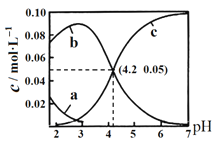
A.曲线b代表H2C2O4浓度随pH的变化
B.HC2O4- ![]() C2O42-+ H+ K = 1×10-4.2
C2O42-+ H+ K = 1×10-4.2
C.pH从4到6时主要发生反应的离子方程式为2OH- + H2C2O4 = 2H2O + C2O42-
D.当溶液pH = 7 时:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向碳酸溶液中滴加NaOH溶液,测得碳酸中含碳微粒的物质的量分数随pH变化如下图所示,下列说法不正确的是
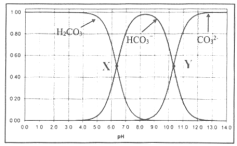
A.人体血液的![]() ,其中含碳微粒以
,其中含碳微粒以![]() 、
、![]() 为主
为主
B.除去NaCl溶液中![]() 的方法是向其中加入盐酸至
的方法是向其中加入盐酸至![]()
C.![]() 的溶液中
的溶液中![]()
![]()
D.将![]() 通入NaOH溶液制取
通入NaOH溶液制取![]() ,应大约控制
,应大约控制![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列各组离子在指定溶液中一定能大量共存的有几组( )
①pH=0的溶液:Na+、I-、NO3-、SO42-
②pH=12的溶液中:CO32-、Na+、NO3-、S2-、SO32-
③水电离的H+浓度10-12molL-1的溶液中:Cl-、CO32-、NO3-、NH4+、SO32-
④加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、K+、SO42-
⑤使石蕊变红的溶液中:Fe2+、MnO4-、NO3-、Na+、SO42-
⑥中性溶液中:Fe3+、Al3+、NO3-、Cl-
A.1组B.2组C.3组D.4组
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com