
 ��3molCu��Ӧת��6mol���ӣ���1.5molCu�����˷�Ӧ����ת�Ƶĵ��ӵĸ�����1.806��1024��3NA��
��3molCu��Ӧת��6mol���ӣ���1.5molCu�����˷�Ӧ����ת�Ƶĵ��ӵĸ�����1.806��1024��3NA�� ��1.806��1024��3NA��
��1.806��1024��3NA��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������ˮ�����c��OH-��Ϊ1��10-10 mol/L����Һ�У�AlO2-��CO32-��K+��Na+ |
| B����������Һ�е�c�� H+��Ϊ1��10-5 mol/L����Һ�У�S2-��SO42-��S2O32-��K+ |
| C���ں���Fe3+��Cl-����Һ�У�HCO3-��I-��NH4+��Mg2+ |
| D���ں���KNO3��NaHSO4����Һ�У�Fe2+��Ca2+��Al3+��Cl-��Br- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.1 mol Fe���������ᷴӦ��ת�Ƶĵ�����Ϊ0.3NA |
| B��0.1 mol/L Na2SO4��Һ�У�����SO42- ��Ϊ0.1NA |
| C������£�22.4L���͵ķ�����ΪNA |
| D�����³�ѹ�£�36.5g HCl����ˮ�γ�1L��Һ�������ʵ���Ũ��Ϊ1 mol?L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| A��3��5 | B��5��3 |
| C��5��2 | D��1��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 50 |
| 1 |
| 50 |
| �¶�/�� | 400 | 500 | 830 | 1000 |
| ƽ�ⳣ��K | 10 | 9 | 1 | 0.6 |
| A | B | C | D | |
| n��CO2�� | 3 | 1 | 0 | 1 |
| n��H2�� | 2 | 1 | 0 | 1 |
| n��CO�� | 1 | 2 | 3 | 0.5 |
| n��H2O�� | 5 | 2 | 3 | 2 |
| ���� |
Ͷ�ϱ�[
|
500K | 600K | 700K | 800K | ||
| 1.5 | 45% | 33% | 20% | 12% | ||
| 2.0 | 60% | 43% | 28% | 15% | ||
| 3.0 | 83% | 62% | 37% | 22% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
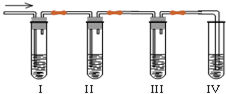 ��ѧ������ȤС��ѧ����ʵ��������ȡ����ϩ�г����������Ķ���������ʦ�������Dz��������Լ��������ͼʵ��ͼ��ȷ�������������������ϩ�Ͷ������ش��������⣺
��ѧ������ȤС��ѧ����ʵ��������ȡ����ϩ�г����������Ķ���������ʦ�������Dz��������Լ��������ͼʵ��ͼ��ȷ�������������������ϩ�Ͷ������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

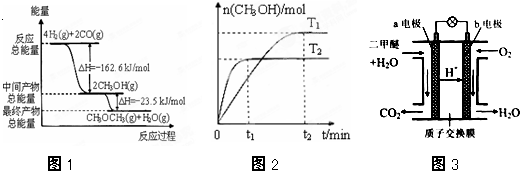
| A����ͼ����ʾʵ��ɱȽ���̼��������Ԫ�صķǽ�����ǿ�� |
| B����ͼ����ʾʵ��װ���ſ������ռ�H2���� |
| C��ͼ�۱�ʾ���淴Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g����Ϊ���ȷ�Ӧ |
| D��ͼ������װ����ͨ�����ߵĵ�������ͬʱ���������ϲ�����������ʵ���Ҳ��ͬ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com